Relações fonte/dreno associado à hidrólise <strong>de</strong> ATP e transporte <strong>de</strong> H + /Ca 2+ (BETHKE et al., 1995). O Ca 2+ também controla os outros ca<strong>na</strong>is iônicos, <strong>de</strong> K + e <strong>de</strong> ânions, como o <strong>de</strong> Cl - e o <strong>de</strong> malato, mo<strong>de</strong>lo bem conhecido para o controle da abertura estomática (Fig. 11 e Fotos 3, 4, 5 e 6). O aumento do nível <strong>de</strong> Ca 2+ no citosol das células guardas, causa o fechamento estomático (COUSSON et al., 1995). O Ca 2+ parece controlar também o transporte <strong>de</strong> célula a célula via plasmo<strong>de</strong>smata , abrindo ou fechando o plasmo<strong>de</strong>smo em um sistema do tipo “gap junctions”, como é conhecido em animais (LEW, 1995). Variações <strong>de</strong> pH - A concentração <strong>de</strong> H + no citosol funcio<strong>na</strong> como outro mensageiro intracelular, afetando o potencial membra<strong>na</strong>r e os ca<strong>na</strong>is <strong>de</strong> Ca 2+ , K + e <strong>de</strong> Cl - . O efeito do ABA causando o fechamento estomático, por exemplo, é <strong>de</strong>pen<strong>de</strong>nte do pH da célula guarda (WARD et al. 1995), assim como o gradiente <strong>de</strong> pH <strong>na</strong> rizosfera é responsável pela distribuição <strong>de</strong> ABA <strong>na</strong> planta. A acidificação da rizosfera <strong>de</strong> pH 6 para 4 aumenta a concentração <strong>de</strong> ABA no xilema em 70% (DAETER et al., 1993). O controle do pH citoplasmático é mediado por um tipo <strong>de</strong> proteí<strong>na</strong> integral <strong>de</strong> membra<strong>na</strong>s, as ATPases-H + da plasmalema (“PMHA”), também existente no tonoplasto. Essas são as proteí<strong>na</strong>s integrais <strong>de</strong> membra<strong>na</strong>s mais bem estudadas, controladas por uma família <strong>de</strong> genes, e no caso da plasmalema, com 5% da superfície exposta para o apoplasto, e 70% para o citoplasma. Essa proteí<strong>na</strong> consome energia química do ATP para transferir prótons para fora do citoplasma. Ela é chamada também <strong>de</strong> bomba <strong>de</strong> H + , e também requer uma interação com os fosfolipí<strong>de</strong>os membra<strong>na</strong>res para a sua ativação. Portanto, o transporte <strong>de</strong> prótons é <strong>de</strong>pen<strong>de</strong>nte <strong>de</strong>stes fosfolipí<strong>de</strong>os membra<strong>na</strong>res, que modulam a ativida<strong>de</strong> da ATPase-H + (KASAMO & SAKAKIBARA, 1995). A extrusão <strong>de</strong> prótons, via ATPase, vai alterar a concentração <strong>de</strong> H + em <strong>de</strong>termi<strong>na</strong>dos locais da plasmalema e do apoplasto (Fig, 10) afetando assim o potencial transmembra<strong>na</strong>r local (STOECKEL & TAKEDA, 1990). Tal processo vai regular a polarização da plasmalema e a ativida<strong>de</strong> <strong>de</strong>ssa bomba <strong>de</strong> H + é aumentada pela presença <strong>de</strong> luz, causando a hiperpolarização <strong>na</strong>s células guardas e conseqüente influxo <strong>de</strong> K + , <strong>na</strong> abertura estomática, por exemplo (Fig. 11). A <strong>de</strong>spolarização da membra<strong>na</strong>, no escuro, vai causar o fechamento estomático pelo processo inverso (COUSSON et al., 1995). O transporte <strong>de</strong> muitos solutos (íons, metabólitos, etc...) para <strong>de</strong>ntro e fora da célula é mediado por transportadores secundários, cuja habilida<strong>de</strong> para o funcio<strong>na</strong>mento é <strong>de</strong>pen<strong>de</strong>nte da força próton-motiva, criada pela ATPase-H + (MICHELET & BOUTRY, 1995). Para a síntese <strong>de</strong> 1 mol <strong>de</strong> ATP são requeridos <strong>de</strong> 2 a 3 moles <strong>de</strong> H + (KRÖMER, 1995). 78
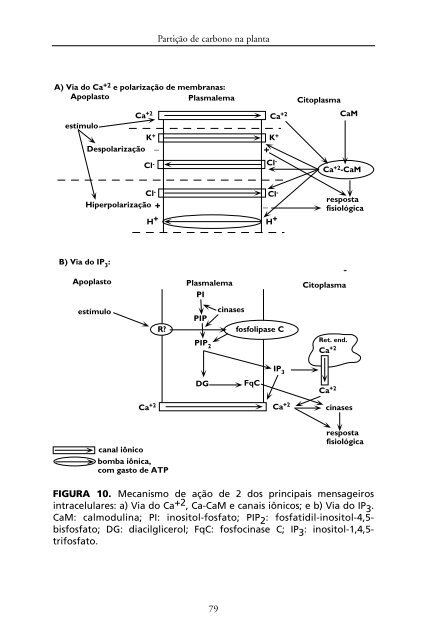
A) Via do Ca +2 e polarização <strong>de</strong> membra<strong>na</strong>s: Ca +2 Ca +2 CaM K Despolarização _ + + K + Apoplasto Plasmalema Citoplasma estímulo Cl- Cl- Hiperpolarização + _ B) Via do IP 3 : Apoplasto estímulo ca<strong>na</strong>l iônico bomba iônica, com gasto <strong>de</strong> ATP Partição <strong>de</strong> carbono <strong>na</strong> planta Cl- Cl- H + H + Plasmalema PI ci<strong>na</strong>ses PIP R? fosfolipase C PIP2 DG FqC 79 IP 3 Ca +2 Ca +2 Ca +2 -CaM resposta fisiológica Citoplasma Ca +2 Ret. end. Ca +2 ci<strong>na</strong>ses resposta fisiológica FIGURA 10. Mecanismo <strong>de</strong> ação <strong>de</strong> 2 dos principais mensageiros intracelulares: a) Via do Ca +2 , Ca-CaM e ca<strong>na</strong>is iônicos; e b) Via do IP 3 . CaM: calmoduli<strong>na</strong>; PI: inositol-fosfato; PIP 2 : fosfatidil-inositol-4,5bisfosfato; DG: diacilglicerol; FqC: fosfoci<strong>na</strong>se C; IP 3 : inositol-1,4,5trifosfato.
- Page 1 and 2:
METABOLISMO DE CARBONO NA AGRICULTU
- Page 3 and 4:
METABOLISMO DE CARBONO NA AGRICULTU
- Page 5 and 6:
Verde que te quiero verde. Verde vi
- Page 7 and 8:
PREFÁCIO A fisiologia vegetal é u
- Page 9 and 10:
SUMÁRIO INTRODUÇÃO Capítulo 1.
- Page 11 and 12:
INTRODUÇÃO A agricultura em zona
- Page 13 and 14:
Assimilação de carbono Capítulo
- Page 15 and 16:
NADP NADPH 2 ADP ATP NADP NADPH 2 N
- Page 17 and 18:
As reações luminosas Foto 1B. clo
- Page 19 and 20:
Fotossistema I Fotossistema II -0.8
- Page 21 and 22:
1.B. AS REAÇÕES ESCURAS As reaç
- Page 23 and 24:
As reações escuras FOTO 2. Bainha
- Page 25 and 26: FOTORRESPIRAÇÃO (CICLO EM C2) CIC
- Page 27 and 28: As reações escuras b) A fotorresp
- Page 29 and 30: HCO3 - PEP-case PEP OXA ATP ADP NAD
- Page 31 and 32: As reações escuras 1.B.3.2. Os tr
- Page 33 and 34: As reações escuras fotorrespirat
- Page 35 and 36: DIA FEP Citoplasma Citoplasma HCO3
- Page 37 and 38: Ecofisiologia de plantas C 3 , C 4
- Page 39 and 40: Ecofisiologia de plantas C 3 , C 4
- Page 41 and 42: Ecofisiologia de plantas C 3 , C 4
- Page 43 and 44: Ecofisiologia de plantas C 3 , C 4
- Page 45 and 46: Ecofisiologia de plantas C 3 , C 4
- Page 47 and 48: Ecofisiologia de plantas C 3 , C 4
- Page 49 and 50: Capítulo 2 RELAÇÕES FONTE/DRENO
- Page 51 and 52: Carboidratos de reserva e estrutura
- Page 53 and 54: Partição de carbono na planta flo
- Page 55 and 56: Partição de carbono na planta flo
- Page 57 and 58: Citocininas (-) Lipases (+) Sistema
- Page 59 and 60: Partição de carbono na planta Em
- Page 61 and 62: Partição de carbono na planta que
- Page 63 and 64: Partição de carbono na planta mer
- Page 65 and 66: Estímulo: genoma, ambiente (compri
- Page 67 and 68: Partição de carbono na planta oco
- Page 69 and 70: Partição de carbono na planta Tab
- Page 71 and 72: Partição de carbono na planta ao
- Page 73 and 74: Partição de carbono na planta seu
- Page 75: Luz, água, CO2, UR%, estímulos f
- Page 79 and 80: A) Fechamento estomático: ABA Luz,
- Page 81 and 82: Partição de carbono na planta FOT
- Page 83 and 84: Partição de carbono na planta FOT
- Page 85 and 86: Partição de carbono na planta con
- Page 87 and 88: Partição de carbono na planta A a
- Page 89 and 90: Partição de carbono na planta res
- Page 91 and 92: Folha (fonte) Célula guarda CO2 at
- Page 93 and 94: Alocação de carbono na planta A s
- Page 95 and 96: Alocação de carbono na planta red
- Page 97 and 98: Alocação de carbono na planta 2.B
- Page 99 and 100: Alocação de carbono na planta rel
- Page 101 and 102: Balanço de carbono e os fatores am
- Page 103 and 104: Introdução Tabela 6. Componentes
- Page 105 and 106: Falta de água e o metabolismo de c
- Page 107 and 108: Falta de água e o metabolismo de c
- Page 109 and 110: Falta de água e o metabolismo de c
- Page 111 and 112: Fotossíntese (A: µmol . m -2 . s
- Page 113 and 114: Falta de água e o metabolismo de c
- Page 115 and 116: Falta de água e o metabolismo de c
- Page 117 and 118: Falta de água e o metabolismo de c
- Page 119 and 120: Temperaturas altas e o metabolismo
- Page 121 and 122: µmol CO 2 . m -2 . s -1 Temperatur
- Page 123 and 124: Temperaturas altas e o metabolismo
- Page 125 and 126: Eficiência no uso de nutrientes e
- Page 127 and 128:
Eficiência no uso de nutrientes e
- Page 129 and 130:
Eficiência no uso de nutrientes e
- Page 131 and 132:
Eficiência no uso de nutrientes e
- Page 133 and 134:
NAD(P)H + H + NAD(P) + 2e - absorç
- Page 135 and 136:
Eficiência no uso de nutrientes e
- Page 137 and 138:
xilema floema Eficiência no uso de
- Page 139 and 140:
REFERÊNCIAS ALBERTS, B., BRAY, D.,
- Page 141 and 142:
BRODL, M. R. 1990. Biochemistry of
- Page 143 and 144:
DUBEY, R. S. 1994. Protein synthesi
- Page 145 and 146:
GOMBOS, Z., WADA, H. HIDEG, E. & MU
- Page 147 and 148:
KELLY, C. K. & WOODWARD, F. I. 1995
- Page 149 and 150:
MADORE, M. A. 1994. Carbohidrate sy
- Page 151 and 152:
OSMOND, C. B., & HOLTUM, J. A. M. 1
- Page 153 and 154:
PUGNAIRE, F. I., ENDOLZ L. S. & PAR
- Page 155 and 156:
SLATYER, R. O. 1970. Comparative ph
- Page 157 and 158:
WALDREN, R. P. 1983. Corn. In: Crop