samopoczucie badanego, a więc wyższy wynik testu), dlatego też test tenwykonuje się kilka minut po pomiarze drżenia [16].Poprawa stanu pacjentów powinna się zatem wyrażać zarówno w poprawieparametrów fizjologicznych mierzonych testem Webstera jaki zmniejszoną mocą drżenia. W trakcie badań, prowadzonych w ramach wieloośrodkowegozespołu badawczego podjęliśmy próbę powiązania wymienionychwyżej płaszczyzn. Wykonywano równocześnie ilościowe badaniastanu fizycznego pacjenta: klinicznie oceny drżenia, parametrów chemicznych:stężenie L-dopy w surowicy i pomiaru CPA oraz parametrów fizjologicznych(trudności w wykonywaniu podstawowych czynności, objawy patologicznefunkcjonowania organizmu itp.). Pomiary w zakresie wymienionychwskaźników były wykonywane równolegle (rys. 8). Pozwoliło to określić korelacjemiedzy nimi. Wyniki eksperymentalnych badań dowodzą, że występujeefekt przesunięcia w czasie maksymalnego zmniejszenia mocy drżeniaw odniesieniu do czasu uzyskania maksymalnego stężenia L-dopy w surowicy.Przesunięcie to wynika z faktu metabolizmu (absorbcji w układzie trawiennym,przekraczanie bariery krew- mózg i jej konwersji do dopaminy)L-dopy i upływu czasu, po którym L-dopa wywiera swój terapeutyczny efekt(rys. 2). W przypadku korelacji między testem Webstera, mocą drżeniai CPA badania wykazały, że podobnie jak w przypadku L-dopy występujeefekt przesunięcia między osiąganym maksymalnym CPA a poprawą parametrówfizjologicznych i mocą drżenia. Przesunięcie to spowodowane jesttakże metabolizmem L-dopy. Uzyskanie efektu terapeutycznego w postaciuzupełnienia deficytu dopaminy, poprawy samopoczucia pacjentów i zmniejszeniemocy drżenia jest wynikiem działania farmakologicznego L-dopyi wymaga upływu czasu. Nie stwierdzono natomiast korelacji pomiędzy CPA,a pozostałymi parametrami. Brak korelacji wynika z braku zależności pomiędzyzmianami CPA, a stężeniem L-dopy w surowicy.c L-dopy [μM]0,60,50,40,30,20,100 1 2 3 4 5czas od podania L-dopy [h]0,00040,00030,00020,00010moc drżenia [W]Rys. 8. Dynamika zmian stężenia L-dopy i mocy drżenia u pacjentów z chorobą Parkinsona26
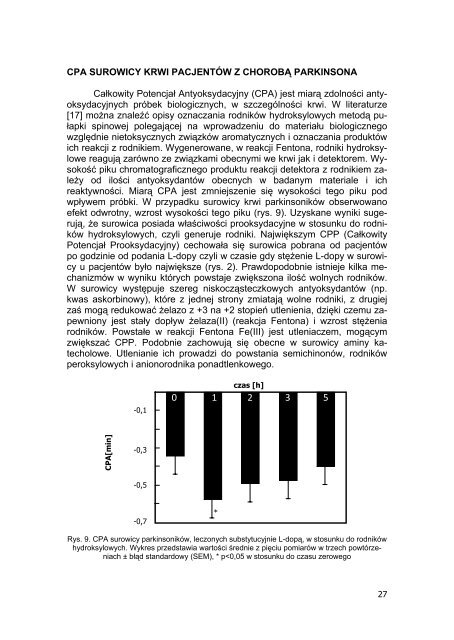
CPA SUROWICY KRWI PACJENTÓW Z CHOROBĄ PARKINSONACałkowity Potencjał Antyoksydacyjny (CPA) jest miarą zdolności antyoksydacyjnychpróbek biologicznych, w szczególności krwi. W literaturze[17] można znaleźć opisy oznaczania rodników hydroksylowych metodą pułapkispinowej polegającej na wprowadzeniu do materiału biologicznegowzględnie nietoksycznych związków aromatycznych i oznaczania produktówich reakcji z rodnikiem. Wygenerowane, w reakcji Fentona, rodniki hydroksylowereagują zarówno ze związkami obecnymi we krwi jak i detektorem. Wysokośćpiku chromatograficznego produktu reakcji detektora z rodnikiem zależyod ilości antyoksydantów obecnych w badanym materiale i ichreaktywności. Miarą CPA jest zmniejszenie się wysokości tego piku podwpływem próbki. W przypadku surowicy krwi parkinsoników obserwowanoefekt odwrotny, wzrost wysokości tego piku (rys. 9). Uzyskane wyniki sugerują,że surowica posiada właściwości prooksydacyjne w stosunku do rodnikówhydroksylowych, czyli generuje rodniki. Największym CPP (CałkowityPotencjał Prooksydacyjny) cechowała się surowica pobrana od pacjentówpo godzinie od podania L-dopy czyli w czasie gdy stężenie L-dopy w surowicyu pacjentów było największe (rys. 2). Prawdopodobnie istnieje kilka mechanizmóww wyniku których powstaje zwiększona ilość wolnych rodników.W surowicy występuje szereg niskocząsteczkowych antyoksydantów (np.kwas askorbinowy), które z jednej strony zmiatają wolne rodniki, z drugiejzaś mogą redukować żelazo z +3 na +2 stopień utlenienia, dzięki czemu zapewnionyjest stały dopływ żelaza(II) (reakcja Fentona) i wzrost stężeniarodników. Powstałe w reakcji Fentona Fe(III) jest utleniaczem, mogącymzwiększać CPP. Podobnie zachowują się obecne w surowicy aminy katecholowe.Utlenianie ich prowadzi do powstania semichinonów, rodnikówperoksylowych i anionorodnika ponadtlenkowego.-0,1czas [h]0 1 2 3 5CPA[min]-0,3-0,5-0,7*Rys. 9. CPA surowicy parkinsoników, leczonych substytucyjnie L-dopą, w stosunku do rodnikówhydroksylowych. Wykres przedstawia wartości średnie z pięciu pomiarów w trzech powtórzeniach± błąd standardowy (SEM), * p
- Page 1 and 2: POSTĘPY CHROMATOGRAFIIPraca zbioro
- Page 3: SPIS TREŚCIPrzedmowa..............
- Page 7 and 8: Piotr M. SŁOMKIEWICZ 1 , Zygfryd W
- Page 9 and 10: W komorze 2 znajduje się pojemnik
- Page 11 and 12: czyna przypływać przez komorę 2
- Page 13 and 14: 4Cnapięcie [mV]3Rys. 6. Chromatogr
- Page 15 and 16: Bronisław K. GŁÓD 1 , Paweł PIS
- Page 17 and 18: Rys. 1. Metabolizm dopaminyL-dopa p
- Page 19 and 20: Dopamina, której niedobór w czę
- Page 21 and 22: katecholowej oraz kompleksowaniu ż
- Page 23 and 24: typu skonstruowano w Instytucie Ele
- Page 25: takich jak zmęczenie czy stres. Dr
- Page 29 and 30: mo wyższych stężeń w surowicy e
- Page 31: LITERATURA1. C. Courderot-masuyer,
- Page 34 and 35: dopuszczające leki jak np. FDA nie
- Page 36 and 37: W przypadku przeprowadzania analizy
- Page 38 and 39: pompaHPLCkolumna chiralnakolumnarea
- Page 40 and 41: 25. K. Lorenz, E. Yashima, Y. Okamo
- Page 42 and 43: Tlen, chociaż jest konieczny do ż
- Page 44 and 45: σ2∗pπ * 2pπ 2pσ 2psingletowy
- Page 46 and 47: Rozpuszczalność tlenku azotu w wo
- Page 48 and 49: nia wolnych rodników. Dlatego nie
- Page 50 and 51: na do nich również poliaminy biog
- Page 52 and 53: trwały rodnik, możliwy do oznacze
- Page 54 and 55: cej zmiany stężenia detektora lub
- Page 56 and 57: Rodniki hydroksylowe są wyjątkowo
- Page 58 and 59: COOHOCOCH3aspirynahydrolizaCOOHCOC
- Page 60 and 61: W statycznej, chromatograficznej me
- Page 62 and 63: sowej. Warto zwrócić w tym przypa
- Page 64 and 65: 35. W. Pakszys, B.K. Głód, P.P. L
- Page 66 and 67: 95. A. Ghiselli, M. Serafini, F. Na
- Page 68 and 69: nych umożliwiających oznaczanie f
- Page 70 and 71: W monitoringu wód powierzchniowych
- Page 72: RT: 4.01 - 19.97IntensityIntensity1
- Page 75 and 76: Ciekawą rolę pełnią zbiorniki w
- Page 77:
Stosowana w badaniach procedura ana
- Page 80 and 81:
wania substancji, zwłaszcza, w ska
- Page 82 and 83:
- Kolumnowa, elucyjna chromatografi
- Page 84 and 85:
Przykłady a, a’, b, b’, c, c
- Page 86 and 87:
ZJAWISKA PRZEŁADOWANIA KOLUMNY (PO
- Page 88 and 89:
ZASADY OPTYMALNEGO STOSOWANIA PREPA
- Page 90 and 91:
- przeładowanie objętościoweW ch
- Page 92 and 93:
Średnica kolumnyNajbardziej celowe
- Page 94 and 95:
Średnica ziaren wypełnienia kolum
- Page 96 and 97:
RetencjaSilna retencja składników
- Page 98 and 99:
OPERACJE JEDNOSTKOWE I TECHNOLOGIA
- Page 100 and 101:
Rys. 10. Schemat ideowy chromatogra
- Page 102 and 103:
Na rys. 13 pokazano kilka chromatog
- Page 104 and 105:
fizycznych i hydrodynamicznych w ko
- Page 106 and 107:
Nie opanowany do końca problem sta
- Page 108 and 109:
Rys. 18. Przykłady reprezentowanyc
- Page 110 and 111:
LITERATURA UZUPEŁNIAJĄCA (pozycje
- Page 112 and 113:
14. Hupe K.P. and Lauer H.H., J. Ch
- Page 114 and 115:
stość izolowanych substancji. Pep
- Page 116 and 117:
(SEC). Ostatnio, do tego celu wykor
- Page 118 and 119:
51243678 90 2 4 6 8 10 12 14 16Rys.
- Page 120 and 121:
jące długie łańcuchy alkilowe,
- Page 122 and 123:
Tabela 2. Modyfikatory fazy ruchome
- Page 124 and 125:
nowymiennych, równorzędnie kation
- Page 126 and 127:
UKŁADY ADSORPCYJNE I ADSORPCYJNO-J
- Page 128 and 129:
CHROMATOGRAFIA ŻELOWAChromatografi
- Page 130 and 131:
CHROMATOGRAFIA ODDZIAŁYWAŃ HYDROF
- Page 132 and 133:
związków. Połączenie elektrofor
- Page 134 and 135:
METODY DETEKCJI W CHROMATOGRAFII PE
- Page 136 and 137:
[25] S.U. Sane, S.M. Cramer, T.M. P