Fakultät für Physik und Astronomie Ruprecht-Karls-Universität ...
Fakultät für Physik und Astronomie Ruprecht-Karls-Universität ...
Fakultät für Physik und Astronomie Ruprecht-Karls-Universität ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
3.1. TITAN ALS GETTERMATERIAL 37<br />
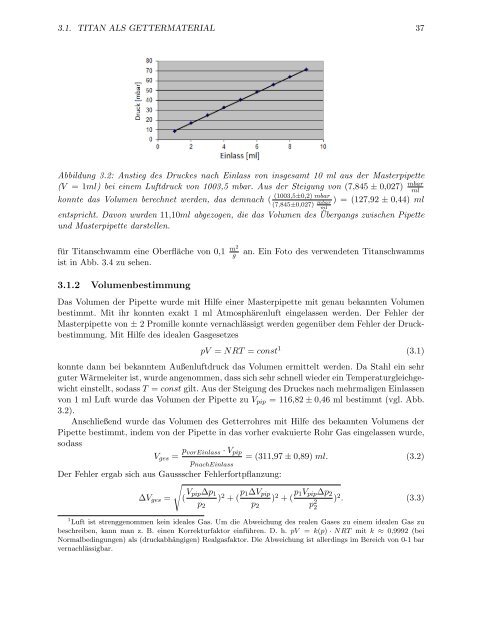
Abbildung 3.2: Anstieg des Druckes nach Einlass von insgesamt 10 ml aus der Masterpipette<br />
(V = 1ml) bei einem Luftdruck von 1003,5 mbar. Aus der Steigung von (7,845 ± 0,027) mbar<br />
konnte das Volumen berechnet werden, das demnach (<br />
(1003,5±0,2) mbar<br />
(7,845±0,027) mbar<br />
ml<br />
ml<br />
) = (127,92 ± 0,44) ml<br />
entspricht. Davon wurden 11,10ml abgezogen, die das Volumen des Übergangs zwischen Pipette<br />
<strong>und</strong> Masterpipette darstellen.<br />
<strong>für</strong> Titanschwamm eine Oberfläche von 0,1 m2<br />
g an. Ein Foto des verwendeten Titanschwamms<br />
ist in Abb. 3.4 zu sehen.<br />
3.1.2 Volumenbestimmung<br />
Das Volumen der Pipette wurde mit Hilfe einer Masterpipette mit genau bekannten Volumen<br />
bestimmt. Mit ihr konnten exakt 1 ml Atmosphärenluft eingelassen werden. Der Fehler der<br />
Masterpipette von ± 2 Promille konnte vernachlässigt werden gegenüber dem Fehler der Druckbestimmung.<br />
Mit Hilfe des idealen Gasgesetzes<br />
pV = NRT = const 1 (3.1)<br />
konnte dann bei bekanntem Außenluftdruck das Volumen ermittelt werden. Da Stahl ein sehr<br />
guter Wärmeleiter ist, wurde angenommen, dass sich sehr schnell wieder ein Temperaturgleichgewicht<br />
einstellt, sodass T = const gilt. Aus der Steigung des Druckes nach mehrmaligen Einlassen<br />
von 1 ml Luft wurde das Volumen der Pipette zu Vpip = 116,82 ± 0,46 ml bestimmt (vgl. Abb.<br />
3.2).<br />
Anschließend wurde das Volumen des Getterrohres mit Hilfe des bekannten Volumens der<br />
Pipette bestimmt, indem von der Pipette in das vorher evakuierte Rohr Gas eingelassen wurde,<br />
sodass<br />
Vges = pvorEinlass · Vpip<br />
= (311,97 ± 0,89) ml. (3.2)<br />
pnachEinlass<br />
Der Fehler ergab sich aus Gaussscher Fehlerfortpflanzung:<br />
<br />
∆Vges =<br />
( Vpip∆p1<br />
p2<br />
) 2 + ( p1∆Vpip<br />
p2<br />
) 2 + ( p1Vpip∆p2<br />
p2 )<br />
2<br />
2 . (3.3)<br />
1 Luft ist strenggenommen kein ideales Gas. Um die Abweichung des realen Gases zu einem idealen Gas zu<br />
beschreiben, kann man z. B. einen Korrekturfaktor einführen. D. h. pV = k(p) · NRT mit k ≈ 0,9992 (bei<br />
Normalbedingungen) als (druckabhängigen) Realgasfaktor. Die Abweichung ist allerdings im Bereich von 0-1 bar<br />
vernachlässigbar.