390Anna Wawrocka, Maciej Krawczyńskidowej, jednak duży przyrost liczby powtórzeń podczaspojedynczej mejozy może być skutkiem wielokrotnej wymianysiostrzanych chromatyd. Wraz z wydłużaniem sięciągu powtórzeń obniża się wiek wystąpienia pierwszychobjawów choroby w kolejnych pokoleniach, ponadto chorobama cięższy przebieg. Zjawisko to nosi nazwę antycypacjii występuje w większości przypadków chorób związanychz ekspansją powtórzeń trójnukleotydowych [3]. Wyjątekstanowi ataksja rdzeniowo-móżdżkowa typu 8 SCA8, wktórej allele zawierające średniej długości trakty powtórzeńsą patogenne. Prawdopodobieństwa wystąpienia mutacji wnastępnym pokoleniu nie można dokładnie określić. U częścigenów występują zmiany premutacyjne, które nie prowadząbezpośrednio do choroby, ale zwiększają prawdopodobieństwojej wystąpienia w kolejnym pokoleniu [4].Choroby związane z ekspansją powtórzeń trójnukleotydowychmożna podzielić ze względu na miejsce występowaniapowtórzeń:1. Trójnukleotydowe powtórzenia zlokalizowane wregionie ulegającym translacji. Do tej grupy choróbzalicza się:pląsawicę Huntingtona – HD, ataksję rdzeniowomóż-dżkowątypu pierwszego – SCA1, ataksję rdzeniowo-móżdżkowątypu drugiego – SCA2, ataksję rdzeniowo-móżdżkowątypu trzeciego – SCA3, ataksję rdzeniowo-móżdżkowątypu szóstego – SCA6, ataksjęrdzeniowo-móżdżkową typu siódmego – SCA7, ataksjęrdzeniowo-móżdżkową typu siedemnastego – SCA17,zwyrodnienie zębato-czerwienne DRPLA, rdzeniowoopuszkowyzanik mięśni typu Kennedy`ego – SBMA,dystrofię mięśniową oczno-gardzielową – OPMD,achondroplazję rzekomą – COMP.2. Trójnukleotydowe powtórzenia zlokalizowane wregionie nie ulegającym translacji oraz w intronie. Do tejgrupy chorób zalicza się:zespół łamliwego chromosomu X – FRAXA, upośledzenieumysłowe związane z FRAXE, dystrofię miotoniczną– DM, ataksję rdzeniowo-móżdżkową typuósmego – SCA8, ataksję móżdżkowo-rdzeniową typudwunastego – SCA12, ataksję Friedreicha – FRDA.Charakterystkę wymienionych chorób przedstawionow tabeli 1.TRANSKRYPCJATRANSLACJAZespół łamliwegochromosomu X (CGG)Opóźnienie umysłowezwiązane z FRAXE (GCC)SCA 12 (CAG)nnnAtaksjaFriedreicha(GAA) nPląsawicaHuntingtonaSCA 1, SCA 2SCA 3, SCA 7,DRPLA(CAG)Dystrofiamiotoniczna(CAG)SCA 8(CTG)5’UTR INTRON ORF 3’UTRm RNABiałkoRyc. 2. Lokalizacja trójnukleotydowych powtórzeń w genie, wprzypadku chorób związanych z ekspansją powtórzeń mikrosatelitarnych.Krzyżyk oznacza zahamowanie procesu transkrypcjispowodowanego ekspansją powtórzeń trójnukleotydowych.Mechanizm ekspansji powtórzeń trójnukleotydowychMechanizm ekspansji powtórzeń trójnukleotydowychzwiązany jest z błędami w czasie replikacji DNA,wywołanymi „poślizgiem” polimerazy na matrycy DNA.Uważa się jednak, że mechanizm dużych ekspansji różnisię od mechanizmów powodujących niewielką niestabilnośćgenetyczną. Duże ekspansje wywołane są „poślizgiem”polimerazy na DNA z wytworzeniem tzw. struktury„spinki do włosów” (zdolność do tworzenia tejstruktury posiadają fragmenty jednoniciowe; mogą oneulegać wybrzuszeniu tworząc w efekcie fragment dwuniciowejhelisy przypominającej „spinkę do włosów”,stabilizowanej dużą obecnością par GC). Natomiast wydłużanieo kilka powtórzeń wynika z niewielkiego „poślizgu”polimerazy DNA powodującego powstanie niesparowańpomiędzy dwoma komplementarnymi nićmiDNA w regionie sekwencji powtarzającej się. W takiejsytuacji w helisie DNA naprzeciw siebie występują innepary zasad niż G i C lub A i T, które tworzą ze sobąwiązania wodorowe [5]. Znanych jest kilka mechanizmówpowodujących „poślizg” polimerazy. Najważniejszez nich to: oddysocjowanie polimerazy DNA od matrycyw trakcie replikacji, zatrzymanie polimerazy DNAw trakcie replikacji sekwencji mikrosatelitarnej oraz„poślizg” końca 5’ i/lub 3’ fragmentów Okazaki.Zgodnie z pierwszym mechanizmem oddysocjowaniepolimerazy DNA od matrycy w trakcie replikacjimoże powodować, że koniec 3’ nici potomnej po rozerwaniuwiązań wodorowych łączących go z nicią macierzystąutworzy stabilną strukturę „spinki do włosów”.Kolejny mechanizm to zatrzymanie polimerazy DNA wtrakcie replikacji sekwencji mikrosatelitarnej. Zatrzymaniepolimerazy na sekwencji powtórzeń trójnukleotydowychmoże prowadzić do ciągłego przesuwania nicipotomnej w kierunku końca 5’ i ponownej syntezy DNAna tym samym fragmencie nici macierzystej. Oba opisanemechanizmy mogą działać zarówno na nici wiodącej,jak i opóźnionej widełek replikacyjnych. W przeciwieństwiedo tych mechanizmów „poślizg” końca 5’ i/lub 3’fragmentów Okazaki dotyczy wyłącznie nici opóźnionej(fragmenty Okazaki to część nowo zsyntetyzowanegoDNA występującego w postaci krótkich fragmentów ok.1000 nt., które podczas replikacji łączone są przez enzymligazę DNA w jedną nić potomną). Zgodnie z tymmodelem początkowa długość regionu sekwencji powtarzającejsię decyduje o rozmiarze ekspansji.Patogeneza chorób spowodowanych ekspansją sekwencjitrójnukleotydowychMutacje odpowiedzialne za choroby dziedzicznemogą powodować :– inaktywację jednego z etapów ekspresji genu, czyliutratę jego funkcji (LOF – loss of function)– powstanie produktu o innych właściwościach niżprodukt genu bez mutacji (GOF – gain of function).Badania, które zostały przeprowadzone nad chorobamipowstałymi w wyniku wydłużania ciągów powtórzeń złożonychz tripletów CAG kodujących poliglutaminę, suge-
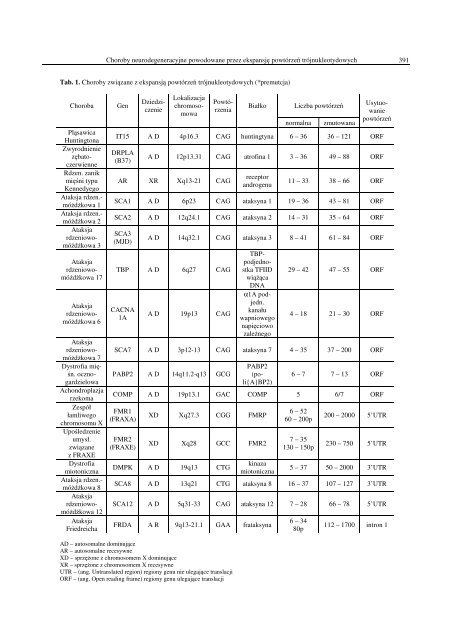
Choroby neurodegeneracyjne powodowane przez ekspansję powtórzeń trójnukleotydowych 391Tab. 1. Choroby związane z ekspansją powtórzeń trójnukleotydowych (*premutcja)ChorobaPląsawicaHuntingtonaZwyrodnieniezębatoczerwienneRdzen. zanikmięśni typuKennedyegoAtaksja rdzen.-móżdżkowa 1Ataksja rdzen.-móżdżkowa 2Ataksjardzeniowomóżdżkowa3Ataksjardzeniowomóżdżkowa17Ataksjardzeniowomóżdżkowa6Ataksjardzeniowomóżdżkowa7Dystrofia mięśn.ocznogardzielowaAchondroplazjarzekomaZespółłamliwegochromosomu XUpośledzenieumysł.związanez FRAXEDystrofiamiotonicznaAtaksja rdzen.-móżdżkowa 8Ataksjardzeniowomóżdżkowa12AtaksjaFriedreichaGenDziedziczenieLokalizacjachromosomowaBiałkoLiczba powtórzeńnormalnazmutowanaPowtórzeniaUsytuowaniepowtórzeńIT15 A D 4p16.3 CAG huntingtyna 6 – 36 36 – 121 ORFDRPLA(B37)A D 12p13.31 CAG atrofina 1 3 – 36 49 – 88 ORFAR XR Xq13-21 CAGreceptorandrogenu11 – 33 38 – 66 ORFSCA1 A D 6p23 CAG ataksyna 1 19 – 36 43 – 81 ORFSCA2 A D 12q24.1 CAG ataksyna 2 14 – 31 35 – 64 ORFSCA3(MJD)A D 14q32.1 CAG ataksyna 3 8 – 41 61 – 84 ORFTBP A D 6q27 CAGCACNA1AA D 19p13 CAGTBPpodjednostkaTFIIDwiążącaDNAα1A podjedn.kanałuwapniowegonapięciowozależnego29 – 42 47 – 55 ORF4 – 18 21 – 30 ORFSCA7 A D 3p12-13 CAG ataksyna 7 4 – 35 37 – 200 ORFPABP2 A D 14q11.2-q13 GCGPABP2(poli{A}BP2)6 – 7 7 – 13 ORFCOMP A D 19p13.1 GAC COMP 5 6/7 ORFFMR1(FRAXA)FMR2(FRAXE)XD Xq27.3 CGG FMRPXD Xq28 GCC FMR2DMPK A D 19q13 CTGkinazamiotoniczna6 – 5260 – 200p7 – 35130 – 150p200 – 2000 5’UTR230 – 750 5’UTR5 – 37 50 – 2000 3’UTRSCA8 A D 13q21 CTG ataksyna 8 16 – 37 107 – 127 3’UTRSCA12 A D 5q31-33 CAG ataksyna 12 7 – 28 66 – 78 5’UTRFRDA A R 9q13-21.1 GAA frataksyna6 – 3480p112 – 1700 intron 1AD – autosomalne dominująceAR – autosomalne recesywneXD – sprzężone z chromosomem X dominująceXR – sprzężone z chromosomem X recesywneUTR – (ang. Untranslated region) regiony genu nie ulegające translacjiORF – (ang. Open reading frame) regiony genu ulegające translacji
- Page 2 and 3:
REDAKTOR NACZELNYEDITOR IN CHIEFpro
- Page 4 and 5:
312Bartosz Sokół i innipodpotylic
- Page 8 and 9:
316Anna Bryl i inniNadmierna stymul
- Page 10 and 11:
318Anna Bryl i inniTab. 1. Wskaźni
- Page 12 and 13:
Nowiny Lekarskie 2006, 75, 4, 320-3
- Page 14 and 15:
322Łukasz Bartkowiak i innikrotnie
- Page 16 and 17:
324Patrycja Gula, Wojmir Ziętkowia
- Page 18 and 19:
326Patrycja Gula, Wojmir Ziętkowia
- Page 20 and 21:
Nowiny Lekarskie 2006, 75, 4, 328-3
- Page 22 and 23:
330Krystyna Przybyłowska i inniWyk
- Page 24 and 25:
332Krystyna Przybyłowska i inniBre
- Page 26 and 27: Nowiny Lekarskie 2006, 75, 4, 334-3
- Page 28 and 29: 336Teresa Seidler, Milena GryzaTabe
- Page 30 and 31: 338Teresa Seidler, Milena Gryzaspo
- Page 32 and 33: Nowiny Lekarskie 2006, 75, 4, 340-3
- Page 34 and 35: 342Barbara Stawińska-Witoszyńska
- Page 36 and 37: Nowiny Lekarskie 2006, 75, 4, 344-3
- Page 38 and 39: 346Irena Maniecka-Bryła, Marek Bry
- Page 40 and 41: 348Irena Maniecka-Bryła, Marek Bry
- Page 42 and 43: 350Irena Maniecka-Bryła, Marek Bry
- Page 44 and 45: 352Wojciech Kapała, Jerzy Skrobisz
- Page 46 and 47: 354Wojciech Kapała, Jerzy Skrobisz
- Page 48 and 49: 356Wojciech Kapała, Jerzy Skrobisz
- Page 50 and 51: 358Wojciech Kapała, Jerzy Skrobisz
- Page 52 and 53: 368Wiesław Kalupanych nie przejawi
- Page 54 and 55: 370Wiesław Kalupa20018016014012010
- Page 56 and 57: 372Teresa Kosicka, Hanna Kara-PerzI
- Page 58 and 59: 374Teresa Kosicka, Hanna Kara-Perz
- Page 60 and 61: 376Teresa Kosicka, Hanna Kara-Perzn
- Page 62 and 63: 2Teresa Kosicka, Hanna Kara-Perz
- Page 64 and 65: Nowiny Lekarskie 2006, 75, 4, 378-3
- Page 66 and 67: Agnieszka Wyrwińska i inni 380minu
- Page 68 and 69: Nowiny Lekarskie 2006, 75, 4, 382-3
- Page 70 and 71: Beata Kosińska 384ocena endoskopow
- Page 72 and 73: Beata Kosińska 386ty białek osocz
- Page 74 and 75: Beata Kosińska 38821. Frewin R.J.,
- Page 78 and 79: 392Anna Wawrocka, Maciej Krawczyńs
- Page 80 and 81: Nowiny Lekarskie 2006, 75, 4, 394-3
- Page 82 and 83: Ewa Zeyland-Malawka, Elżbieta Prę
- Page 84 and 85: Ewa Zeyland-Malawka, Elżbieta Prę
- Page 86 and 87: 400Aleksandra Kuligowska, Grażyna
- Page 88 and 89: 402Aleksandra Kuligowska, Grażyna
- Page 90 and 91: Nowiny Lekarskie 2006, 75, 4, 404-4
- Page 92 and 93: Dominik Dytfeld i inni 406skopii (M
- Page 94 and 95: 408Marcin Wieczorek i inniratykę p
- Page 96 and 97: 410Marcin Wieczorek i inniTab. 1. S
- Page 98 and 99: 412Marcin Wieczorek i inniSchisandr
- Page 101 and 102: Nowiny Lekarskie 2006, 75, 4, 407-4
- Page 103 and 104: INSTRUCTIONS TO AUTHORSGeneral1. No