Chemie im Download - schule.erzbistum-koeln.de
Chemie im Download - schule.erzbistum-koeln.de
Chemie im Download - schule.erzbistum-koeln.de
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
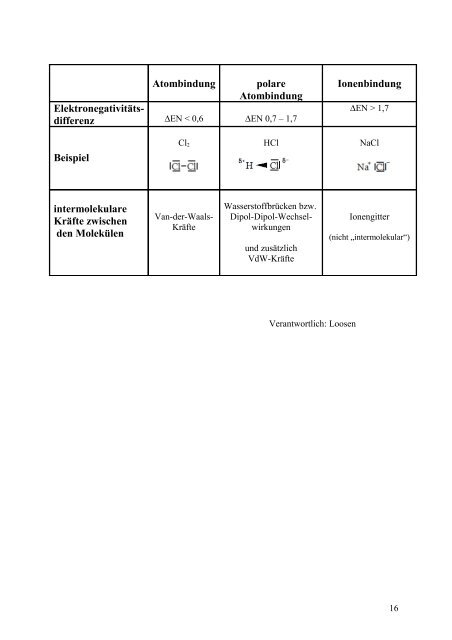
Atombindung polare<br />
Atombindung<br />
Elektronegativitätsdifferenz<br />
∆EN < 0,6 ∆EN 0,7 – 1,7<br />
Ionenbindung<br />
∆EN > 1,7<br />
Beispiel<br />
Cl 2 HCl NaCl<br />
intermolekulare<br />
Kräfte zwischen<br />
<strong>de</strong>n Molekülen<br />
Van-<strong>de</strong>r-Waals-<br />
Kräfte<br />
Wasserstoffbrücken bzw.<br />
Dipol-Dipol-Wechselwirkungen<br />
und zusätzlich<br />
VdW-Kräfte<br />
Ionengitter<br />
(nicht „intermolekular“)<br />
Verantwortlich: Loosen<br />
16