160 Ziegler, Seib, Knoevenagel, Herte und Andreas,Die Untersuchung erstreckt sich über einen Temperaturbereichvon 40®. Dies ist das größte Intervall, über das bisher<strong>der</strong>artige Messungen ausgeführt werden konnten. (Die früherenMessungen von K. Z ie g le r und K. W eber am Hexaphenyläthanerstreckten sich nur über 30®.) Die höchste und dieniedrigste <strong>der</strong> gemessenen Halbwertszeiten verhalten sich wie170:1, ein Zeichen für die Elastizität des Meßverfahrens. Diefür je 10® Temperaturdifferenz berechneten Aktivierungsenergienzeigen keinen systematischen Gang mehr m it <strong>der</strong>Temperatur. Sie schwanken lediglich etwas um den Mittelwert.Diese bemerkenswert scharfe Gültigkeit <strong>der</strong> A rrhenius-Gleichung ist ein Beweis dafür, daß die vermessenen Zerfallskonstantenbzw. Halbwertszeiten keine wesentlichen Fehlermehr aufweisen können. Das über 40® Temperaturdifferenzberechnete E = 25,0 Gal dürfte auf wenige Zehntel-Caloriongenau sein. Hiernach ist es kaum zweifelhaft, daß die weitervom und früher gefundene leichte Temperaturabhängigkeit<strong>der</strong> Aktivierungsenergie bei Hexaaryläthanen nicht real ist^).Die Neu Vermessung dieser Substanzen nach dem verbessertenVerfahren steht aber noch aus. Vermutlich sind jedoch wesentlicheKorrekturen <strong>der</strong> bisher ermittelten Werte von ihr nichtzu erwarten.W ir geben nun im folgenden eine tibersicht über alle vonuns vermessenen Tetraphenyldialphyläthane. Das Hexaphenyläthanist zum Vergleich m it aufgenommen (vgl. Tab. 7).Die Tabelle demonstriert zunächst die Son<strong>der</strong>stellung, diedas Tetraphenyl-dimethyläthan unter seinen sämtlichen Analogeneinnimmt. Diese Son<strong>der</strong>stellung macht sich schon reinqualitativ in <strong>der</strong> bereits vor 18 Jahren beobachteten erhöhtenthermischen Beständigkeit dieses Äthans bemerkbar. DasVerhältnis <strong>der</strong> Zerfallsgeschwindigkeiten von Tetraphenyldimethyläthan(Nr. 1), Tetraphenyldiäthyl- (Nr. 2) und Hexaphenyläthan(Nr. 9) ist 1; 4000 : 60000 (0,00025 : 1: 15). Die*) E . H ü c k e l folgert aus theoretischen Betrachtungen [Z. f. P hysik8 8 , 648 (1933)], daB eine Abnahme <strong>der</strong> Aktivierungsenergie m it steigen<strong>der</strong>Temperatur erfolgen müsse und sieht unsere früheren Ergebnisse alsBestätigung hierfür an. Diese tJbereinstimmung zwischen Theorie undExperiment war, wie jetzt feststeht, nur eine scheinbare.
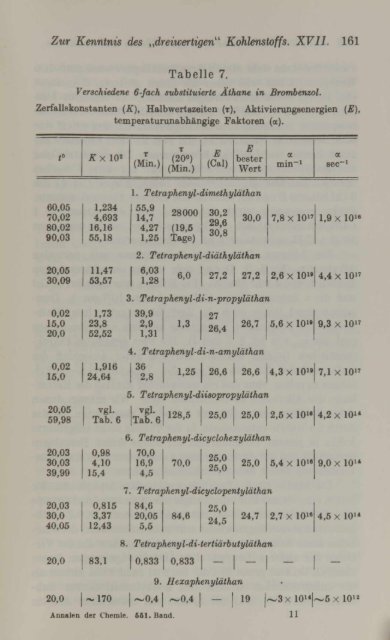
Zur Kenntnis des „dreiwertigen" Kohlenstoffs. X V II. 161T abelle 7.Verschiedene 6-fach aiibstituierte Äthane in Brombemol.Zerfallskonstanten {K), Halbwertszeiten (t ),60,0570.0280.0290,0320,0530,090,0215.020.00,0215,020,0559,9820.0330.0339,9920,0330,040,05Aktivierungsenergien (E),temperaturunabh&ngige Faktoren (a).KxlO*(mL .)1,2344,69316,1655,1811,4763,571,7323,862,521,91624,64vgl.Tab. 60,984,1015,40,8153,3712,43T(2 0 «)(Min.)E(Cal)EbesterWert1. Teir, iphenyl-idimethyläthan56,914,74,271,2628000(19,6Tage)30,229,630,82. Tetraphenyl-diäthyläthan6,031,28amin“ *30,0 7,8 X 10"6,0 27,2 27,2 2,6 X 10“3. Tetraphenyl-di-n-propyläthan39,92,91,311,312726,44. Tetraphenyl-di-n-amyläthan362,81asec-il,9 x 1 0 >'26,7 6,6 X 10>» 9,3 X 10>'1,25 26,6 26,6 4,3 X 10>» 7,1 X 10”5. Tetraphenyl-diisopropyläthanvgl.Tab. 6128,5 25,0 25,0 2,6 X 10“6. Tetraphenyl-dicyclohexyläthan70,016,94,670,026,026,07. Tetraphenyl-dicyclopentyläthan84.620.066,584,625,024,58. Tetraphenyl-di-tertiärbutyläthan20.0 83,1 10,833 0,833 — —9. Hexaphenyläthan •25,0 6,4 X 10'» 9,0 X 10“24,7 2.7 X 10>* 4,5 X 10“20.0 ~170 ~ 0 ,4 ~ 0,4 1 — 19 1~ 3 x 10“ .Annalen <strong>der</strong> Chemie. 661. BttDd. 114,4 X 101’4,2 X 10“