Tratamiento antirretroviral de la infección por el VIH - libdoc.who.int
Tratamiento antirretroviral de la infección por el VIH - libdoc.who.int
Tratamiento antirretroviral de la infección por el VIH - libdoc.who.int
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
105<br />
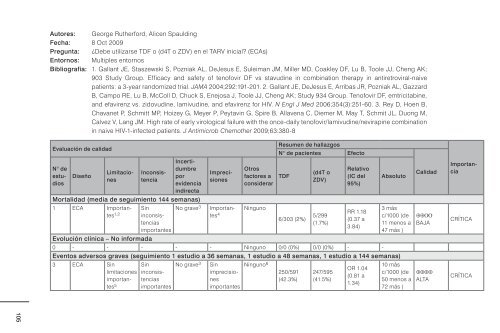
Autores: George Rutherford, Alicen Spaulding<br />
Fecha: 8 Oct 2009<br />
Pregunta: ¿Debe utilizarse TDF o (d4T o ZDV) en <strong>el</strong> TARV inicial? (ECAs)<br />
Entornos: Multiples entornos<br />
Bibliografia: 1. Gal<strong>la</strong>nt JE, Staszewski S, Pozniak AL, DeJesus E, Suleiman JM, Miller MD, Coakley DF, Lu B, Toole JJ, Cheng AK;<br />
903 Study Group. Efficacy and safety of tenofovir DF vs stavudine in combination therapy in antiretroviral-naive<br />
patients: a 3-year randomized trial. JAMA 2004;292:191-201. 2. Gal<strong>la</strong>nt JE, DeJesus E, Arribas JR, Pozniak AL, Gazzard<br />
B, Campo RE, Lu B, McColl D, Chuck S, Enejosa J, Toole JJ, Cheng AK; Study 934 Group. Tenofovir DF, emtricitabine,<br />
and efavirenz vs. zidovudine, <strong>la</strong>mivudine, and efavirenz for HIV. N Engl J Med 2006;354(3):251-60. 3. Rey D, Hoen B,<br />
Chavanet P, Schmitt MP, Hoizey G, Meyer P, Peytavin G, Spire B, Al<strong>la</strong>vena C, Diemer M, May T, Schmit JL, Duong M,<br />
Calvez V, Lang JM. High rate of early virological failure with the once-daily tenofovir/<strong>la</strong>mivudine/nevirapine combination<br />
in naive HIV-1-infected patients. J Antimicrob Chemother 2009;63:380-8<br />
Evaluación <strong>de</strong> calidad<br />
N° <strong>de</strong><br />
estudios<br />
Diseño<br />
Limitaciones<br />
Inconsistencia<br />
Incertidumbre<br />
<strong>por</strong><br />
evi<strong>de</strong>ncia<br />
indirecta<br />
Mortalidad (media <strong>de</strong> seguimiento 144 semanas)<br />
1 ECA Im<strong>por</strong>tantes<br />
1,2<br />
Sin<br />
inconsistencias<br />
im<strong>por</strong>tantes<br />
Imprecisiones<br />
No grave 3 Im<strong>por</strong>tantes<br />
4<br />
Otros<br />
factores a<br />
consi<strong>de</strong>rar<br />
Ninguno<br />
Resumen <strong>de</strong> hal<strong>la</strong>zgos<br />
N° <strong>de</strong> pacientes Efecto<br />
TDF<br />
6/303 (2%)<br />
(d4T o<br />
ZDV)<br />
5/299<br />
(1.7%)<br />
Re<strong>la</strong>tivo<br />
(IC <strong>de</strong>l<br />
95%)<br />
RR 1.18<br />
(0.37 a<br />
3.84)<br />
Absoluto<br />
3 más<br />
c/1000 (<strong>de</strong><br />
11 menos a<br />
47 más )<br />
Evolución clínica – No informada<br />
0 - - - - - Ninguno 0/0 (0%) 0/0 (0%) - -<br />
Eventos adversos graves (seguimiento 1 estudio a 36 semanas, 1 estudio a 48 semanas, 1 estudio a 144 semanas)<br />
3 ECA Sin<br />
limitaciones<br />
im<strong>por</strong>tantes<br />
5<br />
Sin<br />
inconsistencias<br />
im<strong>por</strong>tantes<br />
No grave 3 Sin<br />
imprecisiones<br />
im<strong>por</strong>tantes<br />
Ninguno 6<br />
250/591<br />
(42.3%)<br />
247/595<br />
(41.5%)<br />
OR 1.04<br />
(0.81 a<br />
1.34)<br />
10 más<br />
c/1000 (<strong>de</strong><br />
50 menos a<br />
72 más )<br />
Calidad<br />
⊕⊕OO<br />
BAJA<br />
⊕⊕⊕⊕<br />
ALTA<br />
Im<strong>por</strong>tancia<br />
CRÍTICA<br />
CRÍTICA