DISPENSE DEL CORSO DI LABORATORIO DI CHIMICA – FISICA 1
DISPENSE DEL CORSO DI LABORATORIO DI CHIMICA – FISICA 1
DISPENSE DEL CORSO DI LABORATORIO DI CHIMICA – FISICA 1
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
immaginare di prelevare ogni volta un’aliquota di fase vapore all’equilibrio con la fase<br />
liquida di partenza, condensarla in un recipiente separato, portarla nuovamente<br />
all’equilibrio liquido-vapore, procedere con un nuovo prelievo e via dicendo. Poiché ogni<br />
volta si ottiene una fase vapore più ricca del componente più volatile, dopo un certo<br />
numero di processi elementari di evaporazione<strong>–</strong>condensazione si ottiene virtualmente una<br />
frazione che contiene il componente più volatile allo stato puro. Tale procedura è alla base<br />
del processo di distillazione frazionata (o rettifica) che è costituita da una sequenza di<br />
distillazioni semplici, laddove per distillazione semplice si intende il singolo passaggio<br />
evaporazione<strong>–</strong>condensazione. Poiché il processo è in genere realizzato in condizioni<br />
isobare, si presta ad essere rappresentato proprio mediante un grafico isobaro come quello<br />
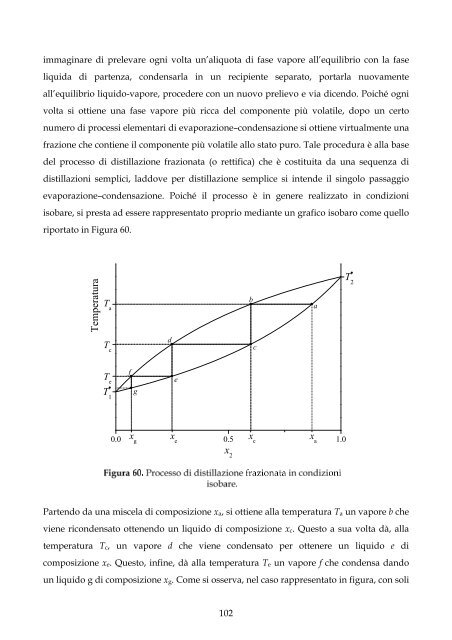
riportato in Figura 60.<br />
Temperatura<br />
T a<br />
T c<br />
Te T •<br />
1<br />
f<br />
g<br />
d<br />
e<br />
0.0 x x g 0.5 x x e c<br />
a 1.0<br />
x 2<br />
Partendo da una miscela di composizione xa, si ottiene alla temperatura Ta un vapore b che<br />
viene ricondensato ottenendo un liquido di composizione xc. Questo a sua volta dà, alla<br />
temperatura Tc, un vapore d che viene condensato per ottenere un liquido e di<br />
composizione xe. Questo, infine, dà alla temperatura Te un vapore f che condensa dando<br />
un liquido g di composizione xg. Come si osserva, nel caso rappresentato in figura, con soli<br />
102<br />
b<br />
c<br />
a<br />
T •<br />
2