Untersuchung von Cyclodextrinkomplexen - OPUS - Universität ...
Untersuchung von Cyclodextrinkomplexen - OPUS - Universität ...
Untersuchung von Cyclodextrinkomplexen - OPUS - Universität ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
100 Ergebnisse und Diskussion<br />
Auch hier zeigt sich, dass das gesamte Molekül in der<br />
Kavität eingeschlossen ist. Die C-C-Streckschwingungen<br />
des Aromaten und die N-H-Streckschwingungen der<br />
Sulfonamidgruppe sind stark abgeschwächt. An den<br />
Banden der S-O-Valenzschwingungen ist der wachsende<br />
Anteil an eingeschlossenem Wirkstoff sehr deutlich zu<br />
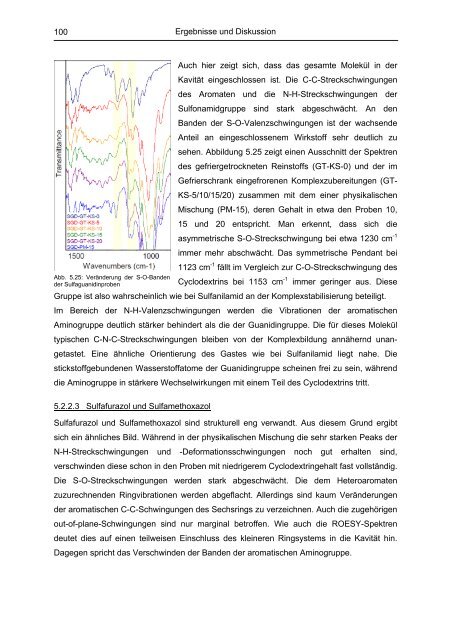
sehen. Abbildung 5.25 zeigt einen Ausschnitt der Spektren<br />
des gefriergetrockneten Reinstoffs (GT-KS-0) und der im<br />
Gefrierschrank eingefrorenen Komplexzubereitungen (GT-<br />
KS-5/10/15/20) zusammen mit dem einer physikalischen<br />
Mischung (PM-15), deren Gehalt in etwa den Proben 10,<br />
15 und 20 entspricht. Man erkennt, dass sich die<br />
asymmetrische S-O-Streckschwingung bei etwa 1230 cm -1<br />
immer mehr abschwächt. Das symmetrische Pendant bei<br />
1123 cm -1 fällt im Vergleich zur C-O-Streckschwingung des<br />
Cyclodextrins bei 1153 cm -1 Abb. 5.25: Veränderung der S-O-Banden<br />
der Sulfaguanidinproben<br />
immer geringer aus. Diese<br />
Gruppe ist also wahrscheinlich wie bei Sulfanilamid an der Komplexstabilisierung beteiligt.<br />
Im Bereich der N-H-Valenzschwingungen werden die Vibrationen der aromatischen<br />
Aminogruppe deutlich stärker behindert als die der Guanidingruppe. Die für dieses Molekül<br />
typischen C-N-C-Streckschwingungen bleiben <strong>von</strong> der Komplexbildung annähernd unangetastet.<br />
Eine ähnliche Orientierung des Gastes wie bei Sulfanilamid liegt nahe. Die<br />
stickstoffgebundenen Wasserstoffatome der Guanidingruppe scheinen frei zu sein, während<br />
die Aminogruppe in stärkere Wechselwirkungen mit einem Teil des Cyclodextrins tritt.<br />
5.2.2.3 Sulfafurazol und Sulfamethoxazol<br />
Sulfafurazol und Sulfamethoxazol sind strukturell eng verwandt. Aus diesem Grund ergibt<br />
sich ein ähnliches Bild. Während in der physikalischen Mischung die sehr starken Peaks der<br />
N-H-Streckschwingungen und -Deformationsschwingungen noch gut erhalten sind,<br />
verschwinden diese schon in den Proben mit niedrigerem Cyclodextringehalt fast vollständig.<br />
Die S-O-Streckschwingungen werden stark abgeschwächt. Die dem Heteroaromaten<br />
zuzurechnenden Ringvibrationen werden abgeflacht. Allerdings sind kaum Veränderungen<br />
der aromatischen C-C-Schwingungen des Sechsrings zu verzeichnen. Auch die zugehörigen<br />
out-of-plane-Schwingungen sind nur marginal betroffen. Wie auch die ROESY-Spektren<br />
deutet dies auf einen teilweisen Einschluss des kleineren Ringsystems in die Kavität hin.<br />
Dagegen spricht das Verschwinden der Banden der aromatischen Aminogruppe.