m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
6.2 Untersuchungen zum Abbruch der Produktion während des Prozesses<br />
ungefähr 30 g/l Biomasse gebildet werden konnten.<br />
Zur Identifizierung einer möglichen Phosphatlimitierung im Medium wurde eine Fermentation<br />
mit kontinuierlicher Phosphatzugabe durchgeführt. Dazu wurden ab t = 12 h<br />
0,75 g/h KH2PO4 dosiert. Die insgesamt dosierte Phosphatmenge entsprach 110 % des am<br />
Anfang der Fermentation vorgelegten Phosphats. Für das Experiment wurde der Stamm<br />
E. <strong>coli</strong> 4pF69 verwendet, der die Gene aroF, pheA* und aroL plasmidkodiert enthielt.<br />
Der Stamm E. <strong>coli</strong> 4pF81, bei dem durch zusätzliche Überexpressions des Gens aroB kein<br />
DAH(P), ein Intermediat der Aromatenbiosynthese, gebildet wurde, stand zum Zeitpunkt<br />
des Experiments noch nicht zur Verfügung 1 . Für die Online-Glucosemessung wurde das<br />
System mit Filtrationsumlauf und OLGA verwendet. Die Phosphatkonzentration in den<br />
Proben wurde mittels eines Schnelltest gemessen (siehe Abschnitt A.3.1).<br />
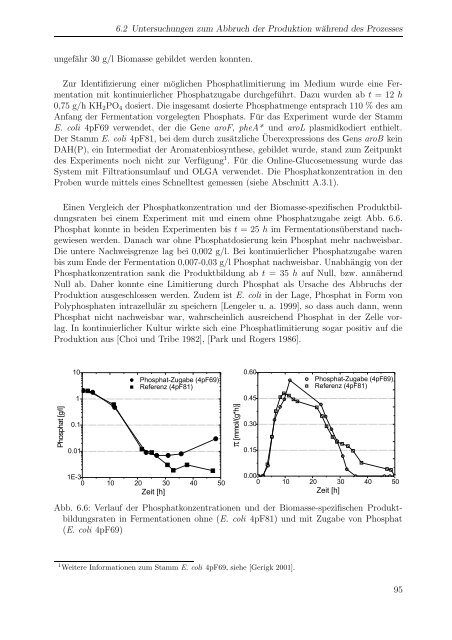
Einen Vergleich der Phosphatkonzentration und der Biomasse-spezifischen Produktbildungsraten<br />
bei einem Experiment mit und einem ohne Phosphatzugabe zeigt Abb. 6.6.<br />
Phosphat konnte in beiden Experimenten bis t = 25 h im Fermentationsüberstand nachgewiesen<br />
werden. Danach war ohne Phosphatdosierung kein Phosphat mehr nachweisbar.<br />
Die untere Nachweisgrenze lag bei 0,002 g/l. Bei kontinuierlicher Phosphatzugabe waren<br />
bis zum Ende der Fermentation 0,007-0,03 g/l Phosphat nachweisbar. Unabhängig von der<br />
Phosphatkonzentration sank die Produktbildung ab t = 35 h auf Null, bzw. annähernd<br />
Null ab. Daher konnte eine Limitierung durch Phosphat als Ursache des Abbruchs der<br />
Produktion ausgeschlossen werden. Zudem ist E. <strong>coli</strong> in der Lage, Phosphat in Form von<br />
Polyphosphaten intrazellulär zu speichern [Lengeler u. a. 1999], so dass auch dann, wenn<br />
Phosphat nicht nachweisbar war, wahrscheinlich ausreichend Phosphat in der Zelle vorlag.<br />
In kontinuierlicher Kultur wirkte sich eine Phosphatlimitierung sogar positiv auf die<br />
Produktion aus [Choi und Tribe 1982], [Park und Rogers 1986].<br />
Phosphat [g/l]<br />
10<br />
1<br />
0.1<br />
0.01<br />
Phosphat-Zugabe (4pF69)<br />
Referenz (4pF81)<br />
1E-3<br />
0 10 20 30 40 50<br />
Zeit [h]<br />
� [mmol/(g*h)]<br />
0.60<br />
0.45<br />
0.30<br />
0.15<br />
Phosphat-Zugabe (4pF69)<br />
Referenz (4pF81)<br />
0.00<br />
0 10 20 30 40 50<br />
Zeit [h]<br />
Abb. 6.6: Verlauf der Phosphatkonzentrationen und der Biomasse-spezifischen Produktbildungsraten<br />
in Fermentationen ohne (E. <strong>coli</strong> 4pF81) und mit Zugabe von Phosphat<br />
(E. <strong>coli</strong> 4pF69)<br />
1 Weitere Informationen zum Stamm E. <strong>coli</strong> 4pF69, siehe [Gerigk 2001].<br />
95