m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Int. Y L-Phe/Gluc [mol/mol %]<br />
16<br />
12<br />
8<br />
4<br />
0<br />
t Prozess =13,5 h<br />
10 25<br />
IPTG [µM]<br />
50<br />
5.3 Vergleich der Produktion mit verschiedenen Stämmen<br />
Int. Y L-Phe/Gluc [mol/mol %]<br />
16<br />
12<br />
8<br />
4<br />
0<br />
t Prozess =49,5 h<br />
10 25<br />
IPTG [µM]<br />
50<br />
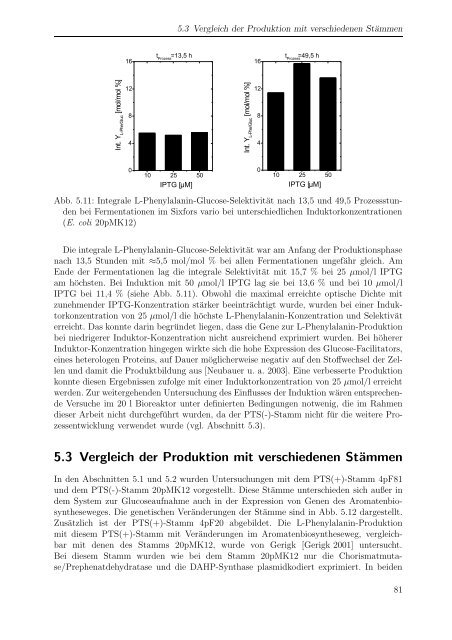
Abb. 5.11: Integrale L-Phenylalanin-Glucose-Selektivität nach 13,5 und 49,5 Prozessstunden<br />
bei Fermentationen im Sixfors vario bei unterschiedlichen Induktorkonzentrationen<br />
(E. <strong>coli</strong> 20pMK12)<br />
Die integrale L-Phenylalanin-Glucose-Selektivität war am Anfang der Produktionsphase<br />
nach 13,5 Stunden mit ≈5,5 mol/mol % bei allen Fermentationen ungefähr gleich. Am<br />
Ende der Fermentationen lag die integrale Selektivität mit 15,7 % bei 25 µmol/l IPTG<br />
am höchsten. Bei Induktion mit 50 µmol/l IPTG lag sie bei 13,6 % und bei 10 µmol/l<br />
IPTG bei 11,4 % (siehe Abb. 5.11). Obwohl die maximal erreichte optische Dichte mit<br />
zunehmender IPTG-Konzentration stärker beeinträchtigt wurde, wurden bei einer Induktorkonzentration<br />
von 25 µmol/l die höchste L-Phenylalanin-Konzentration und Selektivät<br />
erreicht. Das konnte darin begründet liegen, dass die Gene zur L-Phenylalanin-Produktion<br />
bei niedrigerer Induktor-Konzentration nicht ausreichend exprimiert wurden. Bei höherer<br />
Induktor-Konzentration hingegen wirkte sich die hohe Expression des Glucose-Facilitators,<br />
eines heterologen Proteins, auf Dauer möglicherweise negativ auf den Stoffwechsel der Zellen<br />
und damit die Produktbildung aus [Neubauer u. a. 2003]. Eine verbesserte Produktion<br />
konnte diesen Ergebnissen zufolge mit einer Induktorkonzentration von 25 µmol/l erreicht<br />
werden. Zur weitergehenden Untersuchung des Einflusses der Induktion wären entsprechende<br />
Versuche im 20 l Bioreaktor unter definierten Bedingungen notwenig, die im Rahmen<br />
dieser Arbeit nicht durchgeführt wurden, da der PTS(-)-Stamm nicht für die weitere Prozessentwicklung<br />
verwendet wurde (vgl. Abschnitt 5.3).<br />
5.3 Vergleich der Produktion mit verschiedenen Stämmen<br />
In den Abschnitten 5.1 und 5.2 wurden Untersuchungen mit dem PTS(+)-Stamm 4pF81<br />
und dem PTS(-)-Stamm 20pMK12 vorgestellt. Diese Stämme unterschieden sich außer in<br />
dem System zur Glucoseaufnahme auch in der Expression von Genen des Aromatenbiosyntheseweges.<br />
Die genetischen Veränderungen der Stämme sind in Abb. 5.12 dargestellt.<br />
Zusätzlich ist der PTS(+)-Stamm 4pF20 abgebildet. Die L-Phenylalanin-Produktion<br />
mit diesem PTS(+)-Stamm mit Veränderungen im Aromatenbiosyntheseweg, vergleichbar<br />
mit denen des Stamms 20pMK12, wurde von Gerigk [Gerigk 2001] untersucht.<br />
Bei diesem Stamm wurden wie bei dem Stamm 20pMK12 nur die Chorismatmutase/Prephenatdehydratase<br />
und die DAHP-Synthase plasmidkodiert exprimiert. In beiden<br />
81