m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
4.2 Fermentationen im Zulaufverfahren im Sixfors vario<br />
gründen nicht autoklaviert werden durften, wurde über eine Sterilfiltrationsstrecke (Sterilfilter:<br />
Sartobran, Sartorius AG, Göttingen) in die Reaktoren gebracht (Medium, siehe<br />
Abschnitt A.2.1). Das vorgelegte Fermentationsmedium wurde mit 10 % (v/v) Vorkultur<br />
beimpft, so dass 1,5 l erreicht wurden. Die Sauerstoffkonzentration wurde auf 30 % geregelt,<br />
da E. <strong>coli</strong> bei Sauerstofflimitierung unter anaeroben Bedingungen Produkte wie z.B. Acetat<br />
bildet [Schlegel 1992]. Bei Erreichen einer OD620 = 10 − 14 nach 7–10 Stunden wurde<br />
die L-Phenylalanin-Produktion durch Zugabe von IPTG induziert. Die Zufuhr der Substrate<br />
Glucose und L-Tyrosin wurde zum gleichen Zeitpunkt gestartet, da die vorgelegten<br />
Substratmengen annähernd aufgebraucht waren. Die Glucoselösung hatte eine Konzentration<br />
von 454 g/l, die L-Tyrosin-Lösung eine Konzentration von 25 g/l in 5 %iger Ammoniaklösung.<br />
L-Tyrosin-Lösung wurde linear ansteigend nach einem festen Profil bis zum<br />
Erreichen einer festgelegten Gesamtmenge zugegeben. Damit wurde eine OD620 = 40 − 50<br />
erreicht. Danach wurde die Zugabe gestoppt und damit das Wachstum der L-Tyrosinauxotrophen<br />
Stämme. Für die Produktion wurde Glucose mit 0,05–1,0 ml/min zudosiert.<br />
Die Glucosekonzentration wurde manuell mit einem amperometrischen Test überprüft. Entsprechend<br />
dieser Messung wurden die Dosierraten manuell an den Verbrauch im jeweiligen<br />
Bioreaktor angepasst. Der Sollwert lag bei 5 g/l Glucose. Eine zweite Induktion erfolgte<br />
nach 28-30 Stunden, um trotz Verdünnung der Fermentationsbrühe eine ausreichende Induktorkonzentration<br />
zu gewährleisten. Antischaum wurde bei Bedarf manuell zudosiert.<br />
Probenahmen erfolgten über die Fermentationsdauer im Abstand von 1,5–2 Stunden. Die<br />
Offline-Analytik beinhaltete die Messung von Glucose, optischer Dichte, Biotrockenmassekonzentration<br />
und HPLC-Analysen zur Bestimmung von Aminosäuren, Ammonium und<br />
organischen Säuren (siehe Abschnitt A.3.1). Beendet wurden die Fermentationen nach<br />
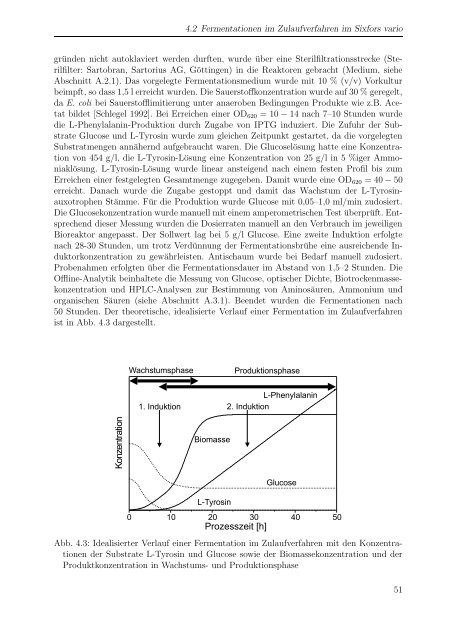
50 Stunden. Der theoretische, idealisierte Verlauf einer Fermentation im Zulaufverfahren<br />
ist in Abb. 4.3 dargestellt.<br />
Konzentration<br />
Wachstumsphase Produktionsphase<br />
1. Induktion<br />
Biomasse<br />
L-Tyrosin<br />
L-Phenylalanin<br />
2. Induktion<br />
Glucose<br />
0 10 20 30 40 50<br />
Prozesszeit [h]<br />
Abb. 4.3: Idealisierter Verlauf einer Fermentation im Zulaufverfahren mit den Konzentrationen<br />
der Substrate L-Tyrosin und Glucose sowie der Biomassekonzentration und der<br />
Produktkonzentration in Wachstums- und Produktionsphase<br />
51