m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
5 Einfluss von Glucoseaufnahmesystemen auf die Produktion<br />
In dieser Darstellung ist zu erkennen, dass bei höherer Glucosekonzentration insgesamt<br />
mehr Glucose aufgenommen wurde. Die Glucoseaufnahme über den Glucose-Facilitator<br />
wurde durch den Substratgradienten angetrieben. Demzufolge sollte die Glucoseaufnahme<br />
bei einer höheren Glucosekonzentration höher sein. Die gebildeten Mengen Biomasse<br />
und L-Phenylalanin waren im Rahmen der Messungenauigkeiten bei beiden Fermentationen<br />
gleich (vgl. Abschnitt A.1). Die sich ergebende integrale L-Phenylalanin-Glucose-<br />
Selektivität der Fermentationen mit Glucoseüberschuss lag nach 50 h bei 11,9 mol/mol %<br />
(5 g/l) und 10,3 mol/mol % (30 g/l). Die Menge an gebildetem Kohlendioxid hingegen<br />
war bei 30 g/l Glucose höher als bei 5 g/l Glucose. Diesen Ergebnissen zufolge nahmen<br />
die Zellen bei höherer Glucosekonzentration etwas mehr Glucose auf. Diese zusätzliche<br />
Menge wurde aber nicht in L-Phenylalanin umgesetzt, sondern in Kohlendioxid. Es war<br />
anzunehmen, dass die dabei gewonnene Energie in anderen, nicht Wachstums-assoziierten<br />
Prozessen verwendet wurde [Neidhardt 1996].<br />
5.2.2 Einfluss der Induktion<br />
Versuche zur Induktion in Schüttelkolben hatten ergeben, dass eine Induktorkonzentration<br />
von 10 µmol/l zu gutem Wachstum führte, eine Induktorkonzentration von 100 µmol/l<br />
jedoch negative Auswirkungen hatte [Sprenger 2001]. Zur weitergehenden Untersuchung<br />
des Einflusses der Induktorkonzentration auf Wachstum und L-Phenylalanin-Produktion<br />
wurden Fermentationen im Zulaufverfahren im Sixfors vario durchgeführt. Damit waren<br />
höhere Biomassekonzentrationen erreichbar als im Schüttelkolben. Der Fermentationsprozess<br />
wurde durchgeführt wie in Abschnitt 4.2.3 beschrieben. Induziert wurde mit<br />
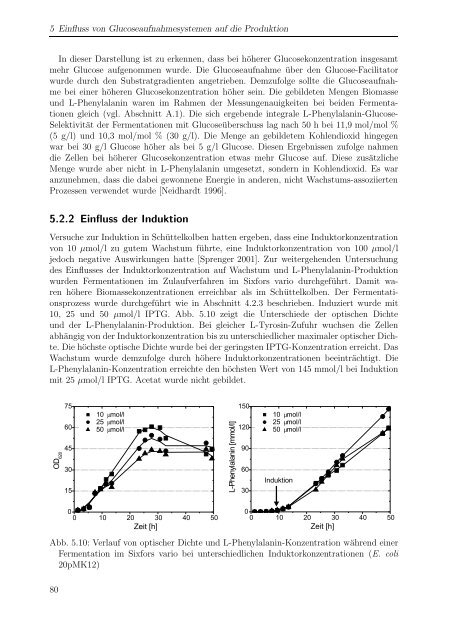
10, 25 und 50 µmol/l IPTG. Abb. 5.10 zeigt die Unterschiede der optischen Dichte<br />
und der L-Phenylalanin-Produktion. Bei gleicher L-Tyrosin-Zufuhr wuchsen die Zellen<br />
abhängig von der Induktorkonzentration bis zu unterschiedlicher maximaler optischer Dichte.<br />
Die höchste optische Dichte wurde bei der geringsten IPTG-Konzentration erreicht. Das<br />
Wachstum wurde demzufolge durch höhere Induktorkonzentrationen beeinträchtigt. Die<br />
L-Phenylalanin-Konzentration erreichte den höchsten Wert von 145 mmol/l bei Induktion<br />
mit 25 µmol/l IPTG. Acetat wurde nicht gebildet.<br />
OD 620<br />
75<br />
60<br />
45<br />
30<br />
15<br />
10 �mol/l<br />
25 �mol/l<br />
50 �mol/l<br />
0<br />
0 10 20 30 40 50<br />
Zeit [h]<br />
L-Phenylalanin [mmol/l]<br />
150<br />
120<br />
90<br />
60<br />
30<br />
10 �mol/l<br />
25 �mol/l<br />
50 �mol/l<br />
Induktion<br />
0<br />
0 10 20 30 40 50<br />
Zeit [h]<br />
Abb. 5.10: Verlauf von optischer Dichte und L-Phenylalanin-Konzentration während einer<br />
Fermentation im Sixfors vario bei unterschiedlichen Induktorkonzentrationen (E. <strong>coli</strong><br />
20pMK12)<br />
80