m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
m i t Escherichia coli - Forschungszentrum Jülich
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
7 Integration der Reaktivextraktion in den Fermentationsprozess<br />
Konzentration [mg/l]<br />
100000<br />
10000<br />
1000<br />
100<br />
10<br />
1<br />
0.1<br />
Fermentation<br />
Akzeptor<br />
L-Phe Ace Amm Na Mg K Ca Mn Fe Cu<br />
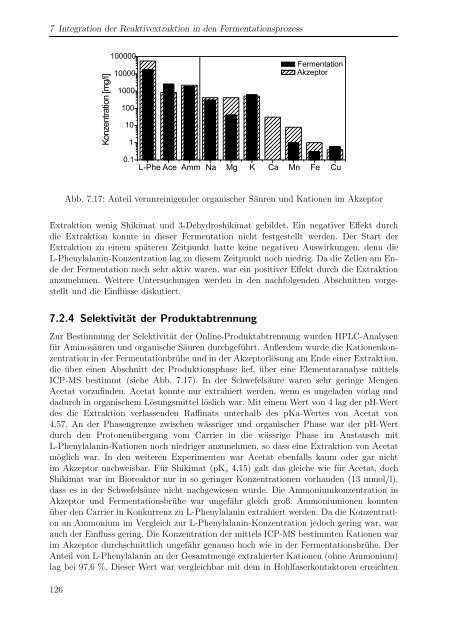
Abb. 7.17: Anteil verunreinigender organischer Säuren und Kationen im Akzeptor<br />
Extraktion wenig Shikimat und 3-Dehydroshikimat gebildet. Ein negativer Effekt durch<br />
die Extraktion konnte in dieser Fermentation nicht festgestellt werden. Der Start der<br />
Extraktion zu einem späteren Zeitpunkt hatte keine negativen Auswirkungen, denn die<br />
L-Phenylalanin-Konzentration lag zu diesem Zeitpunkt noch niedrig. Da die Zellen am Ende<br />
der Fermentation noch sehr aktiv waren, war ein positiver Effekt durch die Extraktion<br />
anzunehmen. Weitere Untersuchungen werden in den nachfolgenden Abschnitten vorgestellt<br />
und die Einflüsse diskutiert.<br />
7.2.4 Selektivität der Produktabtrennung<br />
Zur Bestimmung der Selektivität der Online-Produktabtrennung wurden HPLC-Analysen<br />
für Aminosäuren und organische Säuren durchgeführt. Außerdem wurde die Kationenkonzentration<br />
in der Fermentationbrühe und in der Akzeptorlösung am Ende einer Extraktion,<br />
die über einen Abschnitt der Produktionsphase lief, über eine Elementaranalyse mittels<br />
ICP-MS bestimmt (siehe Abb. 7.17). In der Schwefelsäure waren sehr geringe Mengen<br />
Acetat vorzufinden. Acetat konnte nur extrahiert werden, wenn es ungeladen vorlag und<br />
dadurch in organischem Lösungsmittel löslich war. Mit einem Wert von 4 lag der pH-Wert<br />
des die Extraktion verlassenden Raffinats unterhalb des pKa-Wertes von Acetat von<br />
4,57. An der Phasengrenze zwischen wässriger und organischer Phase war der pH-Wert<br />
durch den Protonenübergang vom Carrier in die wässrige Phase im Austausch mit<br />
L-Phenylalanin-Kationen noch niedriger anzunehmen, so dass eine Extraktion von Acetat<br />
möglich war. In den weiteren Experimenten war Acetat ebenfalls kaum oder gar nicht<br />
im Akzeptor nachweisbar. Für Shikimat (pKs 4,15) galt das gleiche wie für Acetat, doch<br />
Shikimat war im Bioreaktor nur in so geringer Konzentrationen vorhanden (13 mmol/l),<br />
dass es in der Schwefelsäure nicht nachgewiesen wurde. Die Ammoniumkonzentration in<br />
Akzeptor und Fermentationsbrühe war ungefähr gleich groß. Ammoniumionen konnten<br />
über den Carrier in Konkurrenz zu L-Phenylalanin extrahiert werden. Da die Konzentration<br />
an Ammonium im Vergleich zur L-Phenylalanin-Konzentration jedoch gering war, war<br />
auch der Einfluss gering. Die Konzentration der mittels ICP-MS bestimmten Kationen war<br />
im Akzeptor durchschnittlich ungefähr genauso hoch wie in der Fermentationsbrühe. Der<br />
Anteil von L-Phenylalanin an der Gesamtmenge extrahierter Kationen (ohne Ammonium)<br />
lag bei 97,6 %. Dieser Wert war vergleichbar mit dem in Hohlfaserkontaktoren erreichten<br />
126