Participación del Factor Silenciador Neuronal Restrictivo - Tesis ...
Participación del Factor Silenciador Neuronal Restrictivo - Tesis ...
Participación del Factor Silenciador Neuronal Restrictivo - Tesis ...
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Moléculas<br />
Inyectadas<br />
dnXREST + Bmp-4<br />
Genes<br />
Analizados<br />
Efecto observado<br />
Dex (-) Dex (+) st. 9<br />
Sox2 inhibición de la<br />
expresión<br />
92% (n=50) 27% (n=37)<br />
Keratin desplazamiento dorsal 100% (n=41) 13% (n=37)<br />
Slug desplazamiento dorsal 93% (n=14) 30% (n=10)<br />
msx-1 desplazamiento dorsal<br />
y aumento de<br />
expresión<br />
Krox20 inhibición de la<br />
expresión sobre el<br />
pliegue neural<br />
69% (n=13) 11% (n=18)<br />
86% (n=22) 41% (n=22)<br />
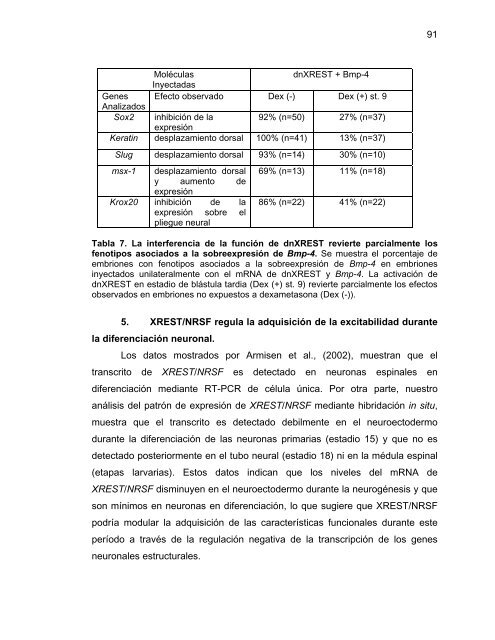
Tabla 7. La interferencia de la función de dnXREST revierte parcialmente los<br />
fenotipos asociados a la sobreexpresión de Bmp-4. Se muestra el porcentaje de<br />
embriones con fenotipos asociados a la sobreexpresión de Bmp-4 en embriones<br />
inyectados unilateralmente con el mRNA de dnXREST y Bmp-4. La activación de<br />
dnXREST en estadio de blástula tardia (Dex (+) st. 9) revierte parcialmente los efectos<br />
observados en embriones no expuestos a dexametasona (Dex (-)).<br />
5. XREST/NRSF regula la adquisición de la excitabilidad durante<br />
la diferenciación neuronal.<br />
Los datos mostrados por Armisen et al., (2002), muestran que el<br />
transcrito de XREST/NRSF es detectado en neuronas espinales en<br />
diferenciación mediante RT-PCR de célula única. Por otra parte, nuestro<br />
análisis <strong>del</strong> patrón de expresión de XREST/NRSF mediante hibridación in situ,<br />
muestra que el transcrito es detectado debilmente en el neuroectodermo<br />
durante la diferenciación de las neuronas primarias (estadio 15) y que no es<br />
detectado posteriormente en el tubo neural (estadio 18) ni en la médula espinal<br />
(etapas larvarias). Estos datos indican que los niveles <strong>del</strong> mRNA de<br />
XREST/NRSF disminuyen en el neuroectodermo durante la neurogénesis y que<br />
son mínimos en neuronas en diferenciación, lo que sugiere que XREST/NRSF<br />
podría modular la adquisición de las características funcionales durante este<br />
período a través de la regulación negativa de la transcripción de los genes<br />
neuronales estructurales.<br />
91