Thermodynamique (2004-2010). - Université de Genève
Thermodynamique (2004-2010). - Université de Genève
Thermodynamique (2004-2010). - Université de Genève
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
∂ 2 p/∂v 2 = 0 ⇒ kBT 3a<br />
=<br />
(v − b) 3 v4 En divisant ces <strong>de</strong>ux égalités, on obtient vc = 3b, ce qui donne alors Tc = 8a/(27bkB), et<br />
<strong>de</strong> l’équation d’état on déduit pc = a/(27b 2 ).<br />
Un critère additionnel pour la stabilité d’un flui<strong>de</strong> 7 est que la compressibilité soit<br />
positive. La compressibilité isotherme κT = −v −1 ∂v/∂p|T (chapitre 4.3) est facilement<br />
obtenue <strong>de</strong> l’équation 8.2 :<br />
κT =<br />
v 2 (v − b) 2<br />
kBT v 3 − 2a(v − b) 2<br />
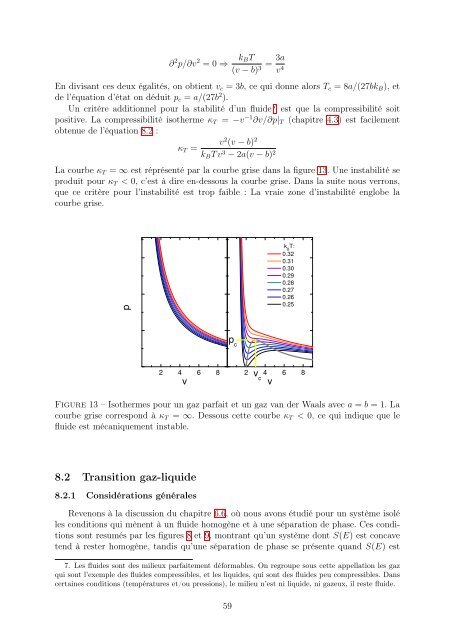
La courbe κT = ∞ est réprésenté par la courbe grise dans la figure 13. Une instabilité se<br />
produit pour κT < 0, c’est à dire en-<strong>de</strong>ssous la courbe grise. Dans la suite nous verrons,<br />
que ce critère pour l’instabilité est trop faible : La vraie zone d’instabilité englobe la<br />
courbe grise.<br />
p<br />
2 4 6 8 2 v 4 6 8<br />
c<br />
v<br />
Figure 13 – Isothermes pour un gaz parfait et un gaz van <strong>de</strong>r Waals avec a = b = 1. La<br />
courbe grise correspond à κT = ∞. Dessous cette courbe κT < 0, ce qui indique que le<br />
flui<strong>de</strong> est mécaniquement instable.<br />
8.2 Transition gaz-liqui<strong>de</strong><br />
8.2.1 Considérations générales<br />
Revenons à la discussion du chapitre 6.6, où nous avons étudié pour un système isolé<br />
les conditions qui mènent à un flui<strong>de</strong> homogène et à une séparation <strong>de</strong> phase. Ces conditions<br />
sont resumés par les figures 8 et 9, montrant qu’un système dont S(E) est concave<br />
tend à rester homogène, tandis qu’une séparation <strong>de</strong> phase se présente quand S(E) est<br />
7. Les flui<strong>de</strong>s sont <strong>de</strong>s milieux parfaitement déformables. On regroupe sous cette appellation les gaz<br />
qui sont l’exemple <strong>de</strong>s flui<strong>de</strong>s compressibles, et les liqui<strong>de</strong>s, qui sont <strong>de</strong>s flui<strong>de</strong>s peu compressibles. Dans<br />
certaines conditions (températures et/ou pressions), le milieu n’est ni liqui<strong>de</strong>, ni gazeux, il reste flui<strong>de</strong>.<br />
p c<br />
59<br />
v<br />
k B T:<br />
0.32<br />
0.31<br />
0.30<br />
0.29<br />
0.28<br />
0.27<br />
0.26<br />
0.25