Thermodynamique (2004-2010). - Université de Genève
Thermodynamique (2004-2010). - Université de Genève
Thermodynamique (2004-2010). - Université de Genève
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
inhomogène. L’entropie suit, comme toujours, <strong>de</strong> la définition S = − ∂F/∂T | N,V<br />
<br />
1/(γ−1)<br />
V − Nb kBT<br />
S = NkB ln ·<br />
+<br />
N e (γ − 1) ρ<br />
NkB<br />
γ − 1<br />
⇒ S = NkB<br />
γ − 1 ln<br />
<br />
kBT (v − b) γ−1 <br />
(γ − 1)ρ<br />
(8.3)<br />
L’énergie interne suit directement <strong>de</strong> l’expression F = E − ST , ce qui avec l’équation<br />
8.1 pour l’énergie libre resulte en<br />
E = NkBT<br />
γ − 1<br />
− aN2<br />
V<br />
Afin d’obtenir la relations S(E) nous substituons kBT/(γ − 1) = E/N + aN/V dans la<br />
relation 8.3, avec le resultat<br />
S = NkB<br />
γ − 1 ln<br />
<br />
ρ −1 (v − b) γ−1<br />
<br />
E a<br />
+ (8.4)<br />
N v<br />
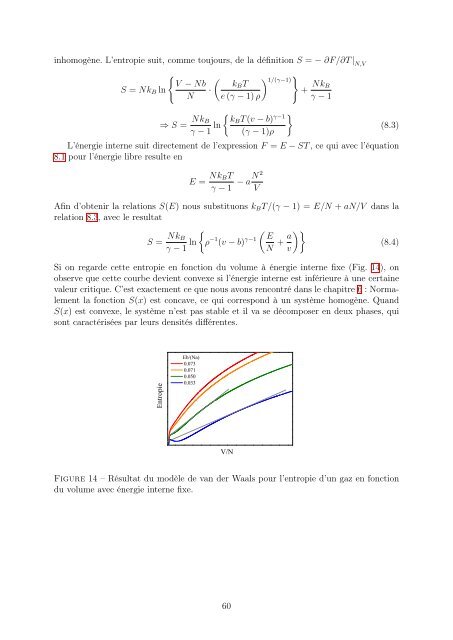
Si on regar<strong>de</strong> cette entropie en fonction du volume à énergie interne fixe (Fig. 14), on<br />
observe que cette courbe <strong>de</strong>vient convexe si l’énergie interne est inférieure à une certaine<br />
valeur critique. C’est exactement ce que nous avons rencontré dans le chapitre 6 : Normalement<br />
la fonction S(x) est concave, ce qui correspond à un système homogène. Quand<br />
S(x) est convexe, le système n’est pas stable et il va se décomposer en <strong>de</strong>ux phases, qui<br />
sont caractérisées par leurs <strong>de</strong>nsités différentes.<br />
Entropie<br />
Eb/(Na)<br />
0.073<br />
0.071<br />
0.050<br />
0.033<br />
V/N<br />
Figure 14 – Résultat du modèle <strong>de</strong> van <strong>de</strong>r Waals pour l’entropie d’un gaz en fonction<br />
du volume avec énergie interne fixe.<br />
60