Bilaga 9 Konsumentprodukter som hjälpmedel i hälso- och sjukvården
Bilaga 9 Konsumentprodukter som hjälpmedel i hälso- och sjukvården
Bilaga 9 Konsumentprodukter som hjälpmedel i hälso- och sjukvården
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
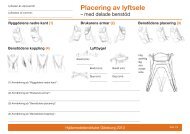
Hjälpmedelsinstitutet 2013-02-14<br />
Rapex-systemet är ett rapporteringssystem inom EU för snabba ingripanden när det<br />
gäller produkter <strong>som</strong> utgör allvarliga risker. Den svenska regleringen finns i<br />
förordningen (1993:1322) om informationsutbyte inom Europeiska ekonomiska<br />
samarbet<strong>som</strong>rådet i fråga om farliga konsumentvaror.<br />
Medlemsstaterna ska identifiera produkter <strong>som</strong> utgör allvarliga risker för hälsa<br />
<strong>och</strong> säkerhet. De ska vidta snabba ingripandeåtgärder för att skydda konsumenterna.<br />
I sådant fall ska medlemslandet omedelbart underrätta kommissionen via Rapexsystemet<br />
för snabbt informationsutbyte mellan medlemsländerna <strong>och</strong> kommissionen.<br />
Det ger möjlighet att begränsa eller förhindra spridning av farliga produkter. Rapexsystemets<br />
funktion beskrivs närmare i bilaga II till produktsäkerhetsdirektivet.<br />
Livsmedel, läkemedel <strong>och</strong> medicintekniska produkter hanteras genom andra<br />
insatssystem.<br />
Följaktligen följer det av 3 § i nämnda förordning att en svensk myndighet <strong>som</strong><br />
beslutar om åtgärder för att hindra, begränsa eller föreskriva särskilda villkor för<br />
tillhandahållande eller användning av en vara på den grunden att varan kan föra med<br />
sig en allvarlig risk för konsumenters hälsa eller säkerhet vid normal eller rimligen<br />
förutsebar användning, ska genast underrätta Konsumentverket om sitt beslut.<br />
Detsamma gäller när myndigheten har rekommenderat eller kommit överens med<br />
näringsidkaren om att vidta sådana åtgärder eller åtgärderna har vidtagits av<br />
näringsidkaren på eget initiativ.<br />
Enligt 5 § förordningen om informationsutbyte inom Europeiska ekonomiska<br />
samarbet<strong>som</strong>rådet i fråga om farliga konsumentvaror ska Konsumentverket genast<br />
underrätta Europeiska kommissionen om berörda myndigheters beslut <strong>och</strong> åtgärder.<br />
Detsamma gäller motsvarande beslut <strong>som</strong> fattas av verket. Vid användningen av<br />
Rapex ska medlemsländerna ge kommissionen information om uppgifter <strong>som</strong> gör det<br />
möjligt att identifiera produkten, en beskrivning av den risk <strong>som</strong> är förknippad med<br />
produkten <strong>och</strong> dokumentation <strong>som</strong> ger möjlighet att bedöma den, åtgärder <strong>som</strong> redan<br />
har vidtagits samt information om produktens distribution.<br />
4.5 Lagen om medicintekniska produkter<br />
Inledning<br />
Som redovisats framgår det av 2 e § HSL att där det bedrivs <strong>hälso</strong>- <strong>och</strong> sjukvård ska<br />
det bl.a. finnas den utrustning <strong>som</strong> behövs för att god vård ska kunna ges. Den<br />
medicinska miljön ställer särskilda säkerhetskrav på utrustning, apparater,<br />
engångsartiklar, instrument, informationssystem m.m. Det beror på att <strong>hälso</strong>- <strong>och</strong><br />
sjukvård är en högriskverksamhet <strong>som</strong> kan få fatala konsekvenser om t.ex. utrustning<br />
m.m. fallerar. Högkvalitativa komponenter, säkra handhavandegrepp, reservsystem<br />
<strong>och</strong> hygienisk design är några signifikativa egenskaper för produkter <strong>som</strong> ska<br />
användas för medicinska syften. De flesta produkter <strong>som</strong> används inom <strong>hälso</strong>- <strong>och</strong><br />
<strong>sjukvården</strong> är därför medicintekniska produkter. Bestämmelser om säkerhet för<br />
produkter <strong>som</strong> är avsedda för medicinska tillämpningar finns i lagen (1993:584) om<br />
24