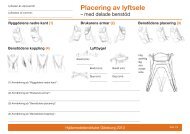
Bilaga 9 Konsumentprodukter som hjälpmedel i hälso- och sjukvården
Bilaga 9 Konsumentprodukter som hjälpmedel i hälso- och sjukvården
Bilaga 9 Konsumentprodukter som hjälpmedel i hälso- och sjukvården
You also want an ePaper? Increase the reach of your titles
YUMPU automatically turns print PDFs into web optimized ePapers that Google loves.
Hjälpmedelsinstitutet 2013-02-14<br />
Tillverkarens ansvar efter att en medicinteknisk produkt har släppts på marknaden<br />
Tillverkare av medicintekniska produkter har ett flertal skyldigheter efter att en<br />
medicinteknisk produkt har släppts på marknaden, s.k. Post Market- uppföljning.<br />
Skyldigheten innefattar bl.a. rapportering av olyckor <strong>och</strong> tillbud med<br />
medicintekniska produkter.<br />
Enligt 6 kap. 2 § Socialstyrelsens föreskrifter ( SOSFS 2008:1) om användning<br />
av medicintekniska produkter i <strong>hälso</strong>- <strong>och</strong> <strong>sjukvården</strong> ska en vårdgivare så snart <strong>som</strong><br />
möjligt efter ett tillbud eller en negativ händelse med en medicinteknisk produkt göra<br />
en anmälan till tillverkaren samt till Läkemedelsverket. Anmälan till tillverkare<br />
underlättas av att det finns ett krav på att medicintekniska produkter ska vara<br />
utmärkta med tillverkaruppgifter. Idag finns inget krav på en unik<br />
produktidentifiering (UDI). Ett sådant krav föreslås i Kommissionens förslag till ny<br />
förordning om medicintekniska produkter. Framställningen återkommer till<br />
Kommissionens förslag.<br />
Enligt 9 a § Läkemedelsverkets föreskrifter (LVFS 2003:11) har tillverkaren en<br />
rapporteringsskyldighet till Läkemedelsverket <strong>som</strong> kan aktualiseras på grund av en<br />
anmälan från en användare, t.ex. en vårdgivare, om en negativ händelse med en<br />
medicinteknisk produkt. Varje felfunktion eller försämring av en produkts<br />
egenskaper eller prestanda, <strong>och</strong> alla felaktigheter i en produkts märkning eller<br />
bruksanvisning, <strong>som</strong> kan leda till eller har lett till en patients eller användares död<br />
eller till en allvarlig försämring av <strong>hälso</strong>tillståndet för någon av dessa personer ska<br />
anmälas av tillverkaren till Läkemedelsverket. Även problem av tekniskt eller<br />
medicinskt slag <strong>som</strong> har samband med en produkts egenskaper eller prestanda, <strong>och</strong><br />
<strong>som</strong> föranlett tillverkaren att systematiskt återkalla produkter från marknaden ska<br />
rapporteras.<br />
Tillverkaren eller dennes representant ska enligt Läkemedelsverkets föreskrifter<br />
bevara relevant dokumentation kring den medicintekniska produkten under minst<br />
fem år, för implantat minst 15 år, efter det att den sista produkten har tillverkats<br />
Tillverkare av medicintekniska produkter ska enligt det medicintekniska regelverket<br />
vidta nödvändiga korrigerande säkerhetsåtgärder för att risker med produkterna ska<br />
hållas på en godtagbart låg nivå. Om åtgärderna berör produkter <strong>som</strong> redan<br />
distribuerats eller används ska tillverkaren informera alla berörda kunder/användare<br />
via ett säkerhetsmeddelande till marknaden (eng. Field Safety Notice, FSN).<br />
Korrigerande säkerhetsåtgärder på marknaden kan vara följande:<br />
Produktåtertagande från distributörer <strong>och</strong> kund/ användare. Kan innefatta ett<br />
utbyte mot en annan säker produkt.<br />
Produktmodifiering av produkten hos kund/ användare. Modifiering kan även<br />
gälla produktens bruksanvisning eller märkning. Utförs normalt av<br />
tillverkarens serviceorganisation eller i enlighet med tillverkarens anvisningar<br />
av personal med lämplig kompetens hos vårdgivare.<br />
Viktig information angående implanterade produkter.<br />
28