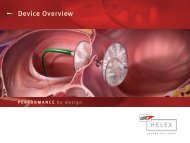
MODE D’EMPLOI :Implant d’occlusion septale GORE®Lire attentivement l’intégralité du mode d’emploi avant utilisation.Observer tous les avertissements et toutes les précautions indiquées dansle présent mode d’emploi.Le non-respect de ces directives peut entraîner des complications.DESCRIPTIONL’implant (système) d’occlusion septale GORE® se compose d’un implantd’occlusion et d’un système de pose. L’implant d’occlusion se compose d’unearmature métallique en nickel-titane (nitinol) avec feuillet en platine, recouvertede polytétrafluoroéthylène expansé (ePTFE). L’ePTFE incorpore un traitementhydrophile de la surface pour faciliter l’imagerie échocardiographique del’implant d’occlusion et du tissu environnant durant l’implantation. Une foisl’implant d’occlusion totalement déployé, il adopte une configuration de disquedouble afin d’empêcher le sang de passer entre l’oreillette droite et l’oreillettegauche. Le système de pose comprend un cathéter porteur de 75 cm de longueurutile et de 10 Fr de diamètre externe, un cathéter de contrôle et un mandrinassocié à une poignée. La poignée facilite le chargement, le déploiement et leverrouillage de l’implant d’occlusion. Elle permet également le repositionnementet le retrait de l’implant d’occlusion à l’aide du cordon de récupération, sinécessaire.L’implant d’occlusion est disponible avec les diamètres suivants : 15, 20,25 et 30 mm. L’implant d’occlusion est mis en place selon les techniquesconventionnelles de pose par cathéter. Il est possible de le mettre en place àl’aide d’un guide de 0,035" (0,89 mm), ou plus petit, si vous le souhaitez.FIGURE 1 : Implant d’occlusion septale GORE®FIGURE 1a : Vue de l’oreillette gaucheŒillet de l’oreillette gaucheCathéter de contrôle (gris)FIGURE 1b : Vue de l’oreillette droiteCathéter porteur (bleu)Valvule de l’implant d’occlusionŒillet de l’oreillette droiteVerrouillage de l’implant d’occlusionArmature métallique ennitinol avec feuillet en platineFIGURE 2 : Système de pose de l’implant d’occlusion septale GORE®Œillet de l’oreillette gaucheCathéter de contrôle (gris)Cathéter porteur (bleu)Orifice de rinçageMécanisme deverrouillage del’implant d’occlusion(rouge) Protection detransport(transparente)Cordon de récupérationGlissière de chargementet de déploiement (grise)Verrouillage du cordonde récupération (rouge)Cathéter porteur (bleu)- longueur utile de 75 cm -Raccord Luer du cathéter porteurPoignéeINDICATIONS / UTILISATIONL’implant d’occlusion septale GORE® est une prothèse d’implantation permanenteindiquée pour la fermeture transcathéter percutanée des communicationsinterauriculaires (CIA) de type ostium secundum ou <strong>for</strong>amen ovale perméable,par exemple.CONTRE-INDICATIONSL’implant d’occlusion septale GORE® est contre-indiqué pour une utilisation chezles patients :• qui ne peuvent pas prendre des antiagrégants plaquettaires ni desanticoagulants tels que l’aspirine, l’héparine ou la warfarine,• présentant une anatomie dans laquelle la taille ou la position de l’implantd’occlusion septale GORE® perturberait d’autres structures intracardiaquesou intravasculaires comme les valvules cardiaques ou les veinespulmonaires,• atteints d’une endocardite évolutive ou d’autres infections entraînantune bactériémie, ou présentant une septicémie connue dans le mois quiprécède l’implantation prévue ou toute autre infection qui ne peut pas êtretraitée avec succès avant la mise en place du dispositif,• présentant des thrombus intracardiaques connus.51
AVERTISSEMENTS• Relatifs à la taille du dispositif :- La taille de la communication interauriculaire et des cavitésauriculaires doit être évaluée sous échocardiographietransœsophagienne (ETO) ou échocardiographie intracardiaque (EIC)avec des mesures de débit par Doppler couleur afin de confirmerque l’espace est suffisant pour accueillir l’implant d’occlusion de lataille sélectionnée sans empiètement sur les structures cardiaquesadjacentes (par ex., les valvules A-V, les orifices des veinespulmonaires, le sinus coronaire ou d’autres structures essentielles).- Les cavités auriculaires doivent être suffisamment volumineuses pourpermettre le positionnement à plat des disques auriculaires droitet gauche contre le septum interauriculaire, avec l’espace entre lesdisques correspondant à l’épaisseur septale, et sans interférence avecles structures cardiaques essentielles ou la paroi libre des oreillettes.- Si l’implant d’occlusion passe à travers la communicationinterauriculaire lors de la con<strong>for</strong>mation des disques, il risque d’êtretrop petit et doit être retiré et remplacé par un implant d’occlusionplus grand.• Les dispositifs embolisés doivent être retirés. Un dispositif embolisé nedoit pas être retiré à travers les structures intracardiaques sauf si l’implantd’occlusion a été suffisamment rétracté dans une gaine.• L’implant d’occlusion septale GORE® doit être utilisé exclusivement pardes médecins <strong>for</strong>més à son utilisation et aux techniques transcathéter defermeture des communications interauriculaires.• Il se peut que les patients allergiques au nickel subissent une réactionallergique à ce dispositif. Certaines réactions allergiques peuvent êtregraves ; il faut demander aux patients de contacter immédiatement leurmédecin s’ils pensent qu’ils font une réaction allergique car ils ont desdifficultés pour respirer ou ils présentent une inflammation du visage oude la gorge. Certains patients peuvent également présenter une allergie aunickel si ce dispositif est implanté.PRÉCAUTIONSManipulation• L’implant d’occlusion septale GORE® est destiné à un usage uniqueseulement. Ne pas réutiliser un implant d’occlusion déverrouillé et retiré.• L’implant d’occlusion septale GORE® est à usage unique seulement. Nepas réutiliser le dispositif. <strong>Gore</strong> ne dispose d’aucune donnée relativeà la réutilisation de ce dispositif. Toute réutilisation risque de produireune défaillance du dispositif ou des complications lors de l’intervention,notamment l’endommagement du dispositif, l’altération de labiocompatibilité du dispositif et la contamination du dispositif. Touteréutilisation risque d’entraîner une infection, une lésion grave ou le décèsdu patient.• Examiner l’emballage avant de l’ouvrir. En cas de rupture de l’étanchéité, lecontenu risque de ne pas être stérile.• Examiner le produit avant de l’utiliser chez un patient. Ne pas utiliser leproduit s’il a été endommagé.• Ne pas l’utiliser au-delà de la date de péremption (« Utiliser avant le »)indiquée.• Ne pas restériliser.Procédure• L’implant d’occlusion septale GORE® ne doit être utilisé que chez lespatients dont le système vasculaire peut accueillir une gaine de posede 10 Fr.• L’implant d’occlusion septale GORE® ne doit être utilisé que chez lespatients dont le système vasculaire peut accueillir une gaine de pose de12 Fr quand un guide est utilisé.• Le temps de coagulation activée (TCA) doit être maintenu à plus de200 secondes durant toute l’intervention.• L’implant d’occlusion septale GORE® doit être utilisé uniquement enassociation avec les techniques d’imagerie appropriées pour évaluerl’anatomie septale et visualiser l’armature métallique.• Il faut disposer de matériel de récupération tel que des gaines de granddiamètre, des anses et des pinces de récupération pour le retrait d’urgenceou volontaire de l’implant d’occlusion.• Envisager le retrait de l’implant d’occlusion si :- La boucle de verrouillage ne réussit pas à capturer les trois œillets ;- L’implant d’occlusion ne reste pas en position plane, en appositioncontre les tissus septaux ;- L’implant d’occlusion sélectionné laisse un shunt excessif ;- L’implant d’occlusion empiète sur les structures cardiaquesadjacentes.• Si le déploiement n’est pas réussi après trois tentatives, il est recommandéd’utiliser un autre dispositif ou traitement pour la fermeture de lacommunication interauriculaire. Il faut tenir compte de l’exposition totaledu patient au rayonnement et à l’anesthésie si des tentatives prolongéesou multiples sont requises pour mettre en place l’implant d’occlusionseptale GORE®.Post-implantation• Après l’implantation du dispositif, administrer aux patients uneantibiothérapie prophylactique appropriée compatible avec les pratiqueshabituelles du médecin.• Après l’implantation, administrer aux patients un traitementantiplaquettaire pendant six mois. La décision de poursuivre le traitementantiplaquettaire au-delà de six mois est à la discrétion du médecin.• Chez les patients sensibles aux traitements antiplaquettaires, d’autrestraitements, comme des anticoagulants, doivent être considérés.• Les patients doivent être in<strong>for</strong>més de la nécessité d’éviter les ef<strong>for</strong>tsphysiques intenses pendant une période d’au moins deux semaines aprèsla mise en place de l’implant d’occlusion.• Les patients devront subir des examens échocardiographiquestransthoraciques (ETT) avant la sortie de l’hôpital et à 1, 6 et 12 moisaprès la mise en place de l’implant d’occlusion pour évaluer la fermeturede la communication interauriculaire. En outre, il convient d’évaluer avecattention la stabilité du dispositif lors de ces examens, car une instabilitépeut indiquer des fractures de l’armature métallique. Dans les cas oùla stabilité du dispositif est douteuse, il est recommandé d’effectuer unexamen radioscopique sans produit de contraste afin de détecter etd’évaluer toute éventuelle fracture de l’armature métallique.52