Zeitschrift für Rheumatologie – Supplement 1 - Deutsche ...
Zeitschrift für Rheumatologie – Supplement 1 - Deutsche ...
Zeitschrift für Rheumatologie – Supplement 1 - Deutsche ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Results: In the cjun promoter, a known insertion (at the position -617/<br />
-618, 2 RA samples) and a new mutation were identifi ed (-823/-824,<br />
1 OA sample). In addition, a new mutation was identifi ed in the junB<br />
promoter (-484, 2 RA/2 OA samples). In the cfos promoter, 2 known<br />
SNPs (-60, -135) were detected (both SNPs in 9 RA/8 OA/4 NC samples).<br />
Th e simultaneous presence of all detected nucleotide exchanges in<br />
SM tissue and blood indicates that they are germline mutations/SNPs.<br />
All detected mutations/SNPs caused a signifi cant decrease of constitutive<br />
reporter gene expression compared to the wt. Following stimulation<br />
with PMA, mutations/SNPs in the promoters of cjun and cfos caused<br />
a remarkable decrease of reporter gene expression (90% compared to<br />
the wt), whereas the mutation <strong>–</strong>484 in the junB promoter only caused<br />
a limited reduction in reporter gene expression.<br />
Conclusion: Diff erent germline mutations/SNPs are located in protooncogene<br />
promoters of RA and OA patients. All detected mutations/<br />
SNPs result in a signifi cant functional inhibition of the promoter, hinting<br />
to a possible role for the expression of disease-relevant genes in RA<br />
and/or OA. Frequency analysis of the mutations/SNPs in larger patient<br />
cohorts is ongoing.<br />
FVFER2 8. Forum Experimentelle <strong>Rheumatologie</strong><br />
Teil 2: Autoimmunity in- and outside the joints-<br />
paralells and differences<br />
FVFER2-1<br />
Ausbreitung von RA synovialen Fibroblasten im SCID Mausmodell<br />
der RA: Nachweis der Migration<br />
Kampmann A. 1 , Knedla A. 1 , Tarner IH. 1 , Stürz H. 2 , Steinmeyer J. 3 , Gay S. 4 ,<br />
Müller-Ladner U. 1 , Neumann E. 1<br />
1 Abt. <strong>Rheumatologie</strong>, JLU Gießen, Kerckhoff -Klinik, 2 Orthopädie, JLU<br />
Gießen, 3 Exp. Orthopädie, JLU Gießen, 4 Zentrum <strong>für</strong> Exp. <strong>Rheumatologie</strong>,<br />
USZ, Zürich, Schweiz<br />
Zielsetzung: Die Rheumatoide Arthritis (RA) beginnt meist in wenigen<br />
Gelenken und greift im Verlauf oft auf weitere Gelenke über.<br />
Der Mechanismus des Krankheitstransfers ist bislang nicht defi niert<br />
untersucht worden. Daher wurde ein Tiermodell entwickelt, bei dem<br />
RA synoviale Fibroblasten (SF) mit normalem humanen Knorpel in<br />
SCID-Mäuse koimplantiert werden, die Tiere aber zusätzlich an einer<br />
entfernten, kontralateralen Stelle Knorpel ohne RASF implantiert bekommen.<br />
Somit kann die RASF-Migration in diesen Tieren detailliert<br />
beobachtet werden.<br />
Methoden: Gruppe 1: 5x105 RASF wurden mit humanem Knorpel<br />
in SCID-Mäuse koimplantiert. An der kontralateralen Flanke wurde<br />
gesunder Knorpel implantiert. Gruppe 2: RASF wurden mit Knorpel<br />
koimplantiert: nach 11 Tagen Einheilungszeit wurde in dasselbe Tier<br />
Knorpel ohne RASF <strong>für</strong> 56 Tage kontralateral implantiert. Gruppe<br />
3: Knorpel ohne RASF wurde an der kontralateralen Seite, nach 14 Tagen<br />
Knorpel und RASF <strong>für</strong> 56 Tage implantiert. Nach Ablauf der Versuchszeit<br />
wurden Implantate, Organgewebe und Blut entnommen.<br />
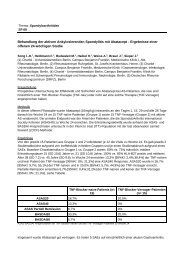
Ergebnisse: RASF können den primären und auch den kontralateral<br />
implantierten Knorpel invadieren. Der Invasionsgrad des kontralateralen<br />
Implantates hängt hierbei vom Implantationszeitpunkt ab.<br />
Werden beide Implantate gleichzeitig (Gruppe 1: primär Inv 2.5±0.5,<br />
Deg 2.0±0.5; kontralateral Inv 1.8±0.5, Deg 1.3±0.5.), oder zunächst<br />
das primäre Implantat mit RASF/Knorpel implantiert (Gruppe 2: primär<br />
Inv 2.4±0.4, Deg 1.9±0.7; kontralateral Inv 1.8±0.5, Deg 2.1±0.9),<br />
zeigten sich vergleichbare Invasions-/Degradationsgrade bei beiden<br />
Implantaten. Wurde das kontralaterale Implantat ohne Zellen zuerst<br />
implantiert (Gruppe 3: primär Inv 1.9±0.9, Deg 2.1±0.7; kontralateral<br />
Inv 2.7±0.6, Deg 2.2±0.8), war die kontralaterale Invasion deutlich stärker.<br />
In keinem der Organe (ausser Milz) wurden RASF nachgewiesen.<br />
Diskussion: Off ensichtlich können RASF von einem Invasions-/<br />
Degrada tionsort zu einem entfernten Knorpel wandern, da RASF eine<br />
massive Invasion und Degradation eines kontralateralen Implantates<br />
verursachen. Dieses Ergebnis unterstützt die Hypothese, dass RASF bei<br />
der Ausbreitung der RA zwischen Gelenken beteiligt sind.<br />
FVFER2-2<br />
Pathogenic and protective role of T cells in glucose-6-phosphate-isomerase-induced<br />
arthritis<br />
Bruns L. 1 , Frey O. 1 , Schubert D. 2 , Reichel A. 1 , Morawietz L. 3 , Krenn V. 3 ,<br />
Kamradt T. 1<br />
1 Institut <strong>für</strong> Immunologie, Friedrich-Schiller-Universität Jena, 2 <strong>Deutsche</strong>s<br />
Rheumaforschungszentrum Berlin, 3 Institut <strong>für</strong> Pathologie, Charite Universitätsmedizin<br />
Berlin<br />
Autoimmunity against the systemic autoantigen glucose-6-phosphate<br />
isomerase (G6PI) can induce arthritis in mice. In the TCR transgenic<br />
K/BxN model G6PI-specifi c T cells drive the production of autoantibodies.<br />
Once generated, the autoantibodies alone are suffi cient to transfer<br />
disease into naïve recipients. In contrast to these fi ndings, T cells play<br />
a major role both in the induction and the eff ector phase of G6PI-induced<br />
arthritis in genetically susceptible nontransgenic strains of mice.<br />
We show that the T cell response against G6PI is biased towards a highly<br />
infl ammatory phenotype with a predominant production of IL-6,<br />
TNF-α and IL-17. Neutralization of either IL-6 or TNF-α can inhibit<br />
disease progression. Depletion of CD4+ T cells before clinical signs of<br />
arthritis blocks the disease and more importantly, depletion on the clinical<br />
peak of arthritis can cure the disease, demonstrating a critical role<br />
for T cells not only in disease induction but also during eff ector stage.<br />
Th e highly infl ammatory T cell subset is controlled by CD4+CD25+<br />
regulatory T (Treg) cells: depletion of Treg prior to immunization increases<br />
the number of IL-17 producing cells and can switch the selflimited<br />
disease into a more chronic disease. Moreover, mice recovered<br />
from arthritis are protected against a reinduction of the disease. We are<br />
currently examining the role of Treg in this protection. Taken together,<br />
this data demonstrates for the fi rst time that CD4+ T cells can have a<br />
critical role as a direct eff ector cell in the pathogenesis of arthritis and<br />
might therefore have some implications for the development of new<br />
T cell directed therapies of human rheumatoid arthritis.<br />
FVFER2-3<br />
Anti-Infl ammatory Eff ects of Atorvastatin in Rheumatoid Arthritis<br />
Blaschke S. 1 , Viereck V. 2 , Schwarz G. 3 , Klinger HM. 3 , Guerluek S. 1 , Bernhard<br />
A. 1 , Wolf G. 1 , Müller GA. 1<br />
1 Abt. Nephrologie und <strong>Rheumatologie</strong>, Universitätsklinik Göttingen,<br />
2 3 Abt. Gynäkologie, Klinik Frauenfeld, Abt. Orthopädie, Universitätsklinik<br />
Göttingen<br />
Introduction: Statins such as atorvastatin (ATV) are 3-Hydroxy-3-methylglutaryl<br />
coenzyme A (HMG-CoA) reductase inhibitors widely used<br />
as lipid-lowering agents in medical practice. Several in vitro and in vivo<br />
studies suggest that statins may also exert immunomodulatory eff ects<br />
by inhibition of proinfl ammatory cytokine production in monocytes/<br />
macrophages as well as by direct inhibition of interferon-γ -(IFN-γ)<br />
induced MHC-II expression. Rheumatoid arthritis (RA) represents a<br />
chronic infl ammatory disease of still unknown etiology characterized<br />
by predominant T helper cell type 1 (Th 1) cytokine expression profi le.<br />
In this study, we analyzed the in vitro eff ects of ATV on Th 1 (IFN-γ)<br />
and Th 2 (IL-4, IL-10) cytokine production in diff erent peripheral T cell<br />
subsets as well as on chemokine production of synovial fi broblasts isolated<br />
from RA patients to characterize potential immunomodulatory<br />
eff ects of ATV in RA.<br />
Materials and Methods: Peripheral blood mononuclear cells (PBMC)<br />
were isolated from 25 RA patients and 20 healthy blood volunteers<br />
(both groups not treated with statins) as controls and were stimulated<br />
in vitro with 0.1 μM ATV. PBMC were analyzed before and aft er 24h of<br />
ATV stimulation by fl ow cytometry for CD4, CD8, CD 69 and HLA-<br />
<strong>Zeitschrift</strong> <strong>für</strong> <strong>Rheumatologie</strong> · <strong>Supplement</strong> 1 · 2006 | S19