Zeitschrift für Rheumatologie – Supplement 1 - Deutsche ...
Zeitschrift für Rheumatologie – Supplement 1 - Deutsche ...
Zeitschrift für Rheumatologie – Supplement 1 - Deutsche ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
S68<br />
Abstracts<br />
sprochen hatten. Die Randomisierung erfolgte unter Berücksichtigung<br />
von Methotrexat-Begleittherapie und Schweregrad der Psoriasis. Die<br />
Patienten erhielten über 24 Wochen 40 mg Adalimumab (ADA) oder<br />
Placebo (PBO) alle 14 Tage. Im Anschluss an die kontrollierte Studienphase<br />
erhielten alle Patienten in einer off enen Fortsetzungsperiode 40<br />
mg Adalimumab alle 14 Tage über weitere 24 Wochen.<br />
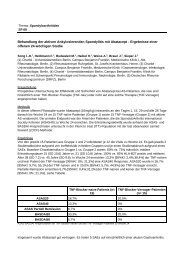
Ergebnisse: Bei den 138 Patienten (PBO, n=69; ADA, n=69), bei denen<br />
bei Studienbeginn ≥3% der KOF betroff en waren, wurden nach<br />
48 Wochen folgende Ansprechraten ermittelt: Ein PASI75- und/oder<br />
ACR20-Ansprechen erreichten 68 % der ADA-Patienten. Ein gleichzeitiges<br />
PASI75- und ACR20-Ansprechen erreichten 45% und ein<br />
gleichzeitiges PASI75- und ACR70-Ansprechen erreichten 26% der<br />
ADA-Patienten. Von denjenigen ADA-Patienten mit ACR50-Ansprechen<br />
erreichten 83% ein PASI75-Ansprechen und von den ADA-Patienten<br />
mit ACR70-Ansprechen erreichten dies 95% der Patienten. Von<br />
den ACR-Non-Respondern erreichten 29% ein PASI75- und 29% ein<br />
PASI90-Ansprechen.<br />
Schlussfolgerung: Die Th erapie mit ADA ist wirksam bei Patienten<br />
mit PsA sowohl gegen Hautsymptome als auch gegen Gelenkentzündungen.<br />
Bei ADA-Patienten, die ACR-Non-Responder waren, konnte<br />
häufi g ein PASI75-Ansprechen erzielt werden, und der Anteil des<br />
PASI75-Ansprechens nahm mit dem Anteil des ACR-Ansprechens zu<br />
und stieg bis auf 95 % bei Patienten mit ACR70-Ansprechen.<br />
POFR3-4<br />
Innovative lokale Schmerztherapie mit IDEA-033 (Ketoprofen in<br />
Transfersom®) zur Behandlung der Kniegelenksarthrose<br />
Rother, Matthias MR. 1 , Mazgareanu, Stefan MS. 1 , Cevc, Gregor GC. 1<br />
1 IDEA-AG, 2 Frankfurter Ring 193a, 380807 München<br />
Die technologische Grundlage von IDEA-033 sind ultradeformierbare<br />
Carrier (Transfersom®), welche die Hautbarriere, angetrieben durch<br />
den transkutanen Feuchtigkeitsgradienten, überwinden und eine gezielte<br />
Freisetzung des transportierten Wirkstoff s, in diesem Fall Ketoprofen,<br />
im tiefen peripheren Gewebe, wie z. B. Muskel oder Gelenk,<br />
bewirken. Transfersome® samt transportierten Ketoprofens werden,<br />
im Gegensatz zu NSAIDs in konventionellen topischen Darreichungsformen,<br />
nach Verabreichung auf die Haut nicht von der dermalen<br />
Mikrozirkulation resorbiert, was zu deutlich höheren Gewebekonzentrationen<br />
und sehr geringen Plasmakonzentrationen führt. Ketoprofen<br />
ist ein potentes Analgetikum mit ausgeprägter anti-infl ammatorischer<br />
Aktivität. IDEA-033 wurde in mehreren klinischen Studien zur Kniegelenksarthrose<br />
untersucht.<br />
In präklinischen pharmakokinetischen Untersuchungen konnte gezeigt<br />
werden, daß IDEA-033 deutlich höhere Ketoprofenkonzentrationen im<br />
Muskel erzeugt als orale und konventionelle topische Darreichungsformen.<br />
Ferner war die Ketoprofenkonzentration in der Synovia der<br />
nach oraler Gabe vergleichbar. Im Gegensatz zu konventionellen topischen<br />
Darreichungsformen wird die synoviale Wirkstoff anreicherung<br />
nur im Zielgelenk erreicht.<br />
Kurzzeitstudien (2 Wochen) zur Kniegelenksarthrose zeigten die<br />
Überlegenheit verschiedener Dosierungen von IDEA-033 (Ketoprofen<br />
Tagesdosis 75 bzw. 100 mg) gegenüber Plazebo bei vergleichbarer Wirkung<br />
zur gleichen Dosis oralen Ketoprofens bzw. von 200 mg Celecoxib.<br />
Die bislang größte Studie an 397 Patienten verglich eine Tagesdosis<br />
von etwa 200 mg Ketoprofen in IDEA-033 mit 200 mg Celecoxib und<br />
Plazebo in einem randomisiserten, parallelen, double-dummy Design.<br />
Die Patienten wurden über 6 Wochen behandelt, und als primäre Erfolgskriterien<br />
wurde die WOMAC Schmerzskala, die WOMAC Funktionsskala<br />
und die Gesamtzufriedenheit des Patienten mit der Behandlung<br />
erfaßt. IDEA-033 zeigte eine statistische Überlegenheit gegenüber<br />
Plazebo <strong>für</strong> alle drei Erfolgskriterien (WOMAC Funktion p=0.012<br />
gem. Per-Protocol Analyse, p=0.077 gem. Intention-To-Treat Analyse).<br />
Der Eff ekt war dem von Celecoxib vergleichbar . Eine post-hoc<br />
Analyse der Responderrate gemäß modifi zierter OMERACT-OARSI<br />
Kriterien zeigte <strong>für</strong> IDEA-033 eine Responderrate von 68.8% (p=0.025<br />
| <strong>Zeitschrift</strong> <strong>für</strong> <strong>Rheumatologie</strong> · <strong>Supplement</strong> 1 · 2006<br />
vs. Plazebo) gegenüber 63.6% <strong>für</strong> Celecoxib (p=n.s.). Die Ketoprofen<br />
Plasmaspiegel lagen im Bereich von 1-5 % gegenüber der Konzentration,<br />
die <strong>für</strong> einmalige systemischer Gabe publiziert wurden. Mit Ausnahme<br />
dermaler Irritationen, bevorzugt in der Kniekehle, gab es keine<br />
relevanten arzneimittelbezogenen Nebenwirkungen.<br />
Nach den bisherigen Ergebnissen erscheint IDEA-033 geeignet <strong>für</strong> die<br />
Kurz- und Langzeitbehandlung der Kniegelenksarthrose mit einer<br />
Wirksamkeit ähnlich der oraler NSAIDs bei gleichzeitig geringer systemischer<br />
Wirkstoff exposition.<br />
POFR3-5<br />
Immunogenität, Wirksamkeit und Sicherheit von Adalimumab in der<br />
klinischen Praxis<br />
Bender N. 1 , Dröll B. 2 , Wohlgemuth J. 2 , Armbruster F. 2 , Heilig B. 1<br />
1 Praxis <strong>für</strong> <strong>Rheumatologie</strong> Heidelberg, 2 Immundiagnostik AG Bensheim<br />
Wir untersuchten die Immunogenität, Wirksamkeit und Sicherheit<br />
von Adalimumab (Humira®), einem humanen IgG1-mAK gegen TNFalpha,<br />
in der klinischen Praxis ohne besondere Studienbedingungen an<br />
15 Patienten (14 RA, 1 PsA), die mit 40 mg Humira® s.c. alle 2 Wochen<br />
(längste Behandlungsdauer 50 Wochen) behandelt wurden, davon 10<br />
Patienten in Kombination von MTX, eine Patientin in Kombination<br />
von Lefl unomid und 4 Patienten mit Humira® als Monotherapie. Die<br />
Detektion von Antikörpern (AK)gegen Adalimumab wurde mittels<br />
eines speziell da<strong>für</strong> entwickelten Sandwich-ELISA der Firma Immundiagnostik<br />
(Bensheim) durchgeführt. Dieser Assay verwendet F(ab’)-<br />
Fragmente von Adalimumab als Bindungsantikörper <strong>für</strong> die im Serum<br />
des Patienten vorhandenen Anti-Adalimumab-AK und Peroxydasemarkierte<br />
Adalimumab-Moleküle als Detektionsantikörper. Die Absorption<br />
wurde im ELISA-Reader gemessen und mittels Cut-off ausgewertet.<br />
Die Krankheitsaktivität wurde unmittelbar vor Th erapie, nach<br />
3, 6, 12 und 18 Monaten anhand des DAS28 gemessen. Die Behandlung<br />
wurde abgebrochen beim Auft reten von Nebenwirkungen oder bei anhaltend<br />
hoher Krankheitsaktivität.<br />
13 (87%) Patienten zeigten im Verlauf der Th erapie einen Anstieg des<br />
AK-Titers in unserem Assay. Insgesamt brachen 14 (93%) Patienten die<br />
Th erapie ab, darunter 7 wegen Ineff ektivität, 6 in Folge von UAW und<br />
eine Patientin auf Grund einer geplanten OP. Bei 10 (67%) Patienten,<br />
allesamt Antikörper-positiv, wurde fehlendes Th erapieansprechen mit<br />
anhaltend hohem DAS28 beobachtet. Insgesamt wurden bei 7 (47%)<br />
Patienten UAW beobachtet, davon 3 (20%) mit Arzneimittelexanthem.<br />
Von diesen 7 Patienten waren wiederum 5 AK-positiv (2 mit Exanthem).<br />
Alle 4 Patienten, die mit Humira® als Monotherapie behandelt<br />
wurden, entwickelten Anti-Adalimumab-AK, darunter brachen die<br />
Th erapie 3 Patienten (2 mit Arzneimittelexanthem) in Folge von UAW<br />
und eine Patientin auf Grund anhaltend hoher Krankheitsaktivität ab.<br />
Ebenso war die Th erapiedauer in dieser Gruppe wesentlich kürzer als<br />
unter den Patienten mit Kombinationsbehandlung (6,0 ± 2,5 vs. 25,8 ±<br />
18,9 Wochen).<br />
Laut unseren Ergebnissen besitzt Adalimumab immunogene Strukturen,<br />
die vom menschlichen Körper, trotz komplett humanen AS-<br />
Sequenzen, als fremd erkannt werden. Möglicherweise handelt es<br />
sich dabei um die hypervariablen Regionen von Adalimumab oder<br />
um nicht humane Glykosilierungsreste, die durch die Phagen- Display-Technik<br />
entstehen. Eine Korrelation mit klinischen Parametern,<br />
wie Krankheitsaktivität oder Nebenwirkungen, kann auf Grund der<br />
insgesamt sehr hohen Inzidenz von Antikörpern gegen Adalimumab<br />
und der sehr niedrigen Anzahl an untersuchten Patienten nur eingeschränkt<br />
hergestellt werden. Möglicherweise liegt ein Zusammenhang<br />
von therapeutischem Versagen und der Anwesenheit von Anti-Adalimumab-AK<br />
vor.