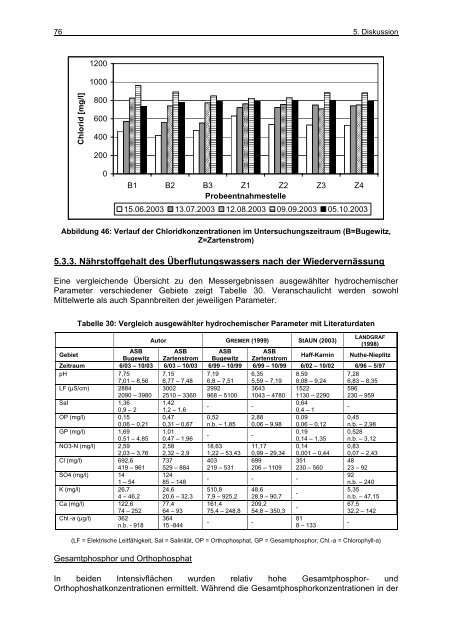
76 5. Diskussion Chlorid [mg/l] 1200 1000 800 600 400 200 0 B1 B2 B3 Z1 Z2 Z3 Z4 Probeentnahmestelle 15.06.2003 13.07.2003 12.08.2003 09.09.2003 05.10.2003 Abbildung 46: Verlauf der Chloridkonzentrationen <strong>im</strong> Untersuchungszeitraum (B=Bugewitz, Z=Zartenstrom) 5.3.3. Nährstoffgehalt <strong>des</strong> Überflutungswassers nach der Wiedervernässung Eine vergleichende Übersicht zu den Messergebnissen ausgewählter hydrochemischer Parameter verschiedener Gebiete zeigt Tabelle 30. Veranschaulicht werden sowohl Mittelwerte als auch Spannbreiten der jeweiligen Parameter. Tabelle 30: Vergleich ausgewählter hydrochemischer Parameter mit Literaturdaten Autor GREMER (1999) StAUN (2003) LANDGRAF (1998) Gebiet ASB Bugewitz ASB Zartenstrom ASB Bugewitz ASB Zartenstrom Haff-Karnin Nuthe-Nieplitz Zeitraum 6/03 – 10/03 6/03 – 10/03 6/99 – 10/99 6/99 – 10/99 6/02 – 10/02 6/96 – 5/97 pH 7,75 7,15 7,19 6,35 8,59 7,28 7,01 – 8,56 6,77 – 7,48 6,8 – 7,51 5,59 – 7,19 8,08 – 9,24 6,83 – 8,35 LF (µS/cm) 2884 3002 2992 3643 1522 596 2090 – 3980 2510 – 3360 968 – 5100 1043 – 4780 1130 – 2290 230 – 959 Sal 1,36 0,9 – 2 1,42 1,2 – 1,6 - - 0,64 0,4 – 1 - OP (mg/l) 0,15 0,47 0,52 2,88 0,09 0,45 0,06 – 0,21 0,31 – 0,67 n.b. – 1,85 0,06 – 9,98 0,06 – 0,12 n.b. – 2,98 GP (mg/l) 1,69 0,51 – 4,85 1,01 0,47 – 1,96 - - 0,19 0,14 – 1,35 0,528 n.b. – 3,12 NO3-N (mg/l) 2,59 2,58 18,63 11,17 0,14 0,83 2,03 – 3,76 2,32 – 2,9 1,22 – 53,43 0,99 – 29,34 0,001 – 0,44 0,07 – 2,43 Cl (mg/l) 692,6 737 403 699 351 48 419 – 961 529 – 884 219 – 531 206 – 1109 230 – 560 23 – 92 SO4 (mg/l) 14 1 – 54 124 85 – 148 - - - 92 n.b. – 240 K (mg/l) 26,7 4 – 46,2 24,6 20,6 – 32,3 510,8 7,9 – 925,2 48,6 28,9 – 90,7 - 5,35 n.b. – 47,15 Ca (mg/l) 122,6 74 – 252 77,4 64 – 93 161,4 75,4 – 248,8 209,2 54,8 – 350,3 - 67,5 32,2 – 142 Chl.-a (µg/l) 362 n.b. - 918 364 15 -844 - - 81 8 – 133 - (LF = Elektrische Leitfähigkeit, Sal = Salinität, OP = Orthophosphat, GP = Gesamtphosphor, Chl.-a = Chlorophyll-a) Gesamtphosphor <strong>und</strong> Orthophosphat In beiden Intensivflächen wurden relativ hohe Gesamtphosphor- <strong>und</strong> Orthophoshatkonzentrationen ermittelt. Während die Gesamtphosphorkonzentrationen in der
5. Diskussion 77 IF Bugewitz z. T. extrem hohe Werte erreichten, waren sie am Zartenstrom wesentlich niedriger. Die unterschiedlichen Gesamtphosphorgehalte wiederspiegeln damit nicht die gegenwärtige Vegetation beider Flächen, da die IF Bugewitz <strong>im</strong> Vergleich zum Zartenstrom durch eine anspruchslosere Vegetation charakterisiert ist. Die Ursache für dieses widersprüchliche Ergebnis ist in den sehr komplexen Bindungsformen <strong>des</strong> Phosphors zu suchen, was durch die Untersuchung <strong>des</strong> Orthophosphatgehaltes bestätigt wird. Ein Teil <strong>des</strong> Gesamtphosphors liegt als anorganisches Phosphat vorwiegend in gelöster Form vor, wobei eine unterschiedlich starke sorptive Bindung an Huminstoffen, z. T. unter Mitwirkung von Kationen vorstellbar ist (STEINBERG & BALTES 1984). Ein anderer Teil ist dagegen organisch geb<strong>und</strong>en, <strong>und</strong> wird erst durch Abbau abgestorbener Biomasse freigesetzt (DICKINSON 1983). Die direkte Aufnahme von Phosphor durch Pflanzenwurzeln erfolgt dagegen überwiegend als Orthophosphat (KLAPPER 1992). Die eigenen Untersuchungen zeigen, dass die Orthophoshatgehalte der Fläche Zartenstrom die Konzentrationen der Fläche Bugewitz um das 3fache übersteigen, so dass hier trotz niedrigerer Gesamtphosphorgehalte bessere Ernährungsbedingungen für die Vegetation vorliegen. Die Höhe <strong>des</strong> Orthophosphatgehaltes <strong>des</strong> Wassers korrespondiert daher besser mit dem Trophie-Zeigerwert der Vegetation. REDDY & D`ANGELO (1994) geben an, dass der organische Phosphor in Mooren oft mit Humus- <strong>und</strong> Fulvosäuren assoziert ist <strong>und</strong> mehr als 40 % <strong>des</strong> Gesamtphosphors betragen kann, der anaerob nur schwer mineralisiert wird. Gerade in der Intensivfläche Bugewitz kann ein hoher Anteil an Huminstoffen <strong>im</strong> Wasser vermutet werden, weil das Wasser eine intensive Braunfärbung aufweist. Da das Überflutungswasser das gesamte Stadtbruch durchfließen muss, bevor es <strong>im</strong> Polder Bugewitz ankommt, ist theoretisch eine Anreicherung mit Huminstoffen denkbar. In entwässerten Mooren wird organisch geb<strong>und</strong>ener Phosphor dagegen in leichter verfügbare P-Bindungsformen überführt, wobei Phosphat wahrscheinlich an Festphasen wie Eisen-(III)-Hydroxide sorbiert wird. Da diese Bindung redoxempfindlich ist, führen anoxische Bedingungen zu einer P-Rücklösung (GELBRECHT & KOPPISCH 2001), was zu einem hohen Anstieg der P-Konzentrationen in <strong>wiedervernässten</strong> Niedermooren führen kann (GELBRECHT & LENGSFELD 1998). Dies dürfte eine Ursache für die relativ hohen P-Konzentrationen <strong>im</strong> UG sein. Berücksichtigt werden sollte jedoch auch, dass in den Poldern viele Jahre mit Phosphaten gedüngt wurde (PRAGER 2000). Weiterhin kam es infolge der Überflutung zu einem großflächigen Absterben der Ausgangsvegetation, was zu einer hohen P-Freisetzung geführt haben könnte. In Überflutungsmooren spielt außerdem der allochthone P-Eintrag aus Oberflächengewässern eine erhebliche Rolle (GELBRECHT & KOPPISCH 2001). Im ASB erfolgt dieser überwiegend mit dem Überflutungswasser <strong>des</strong> Haffs. Da das Haffwasser jedoch deutlich geringere P-Konzentrationen aufweist als das Überstauwasser der <strong>wiedervernässten</strong> Flächen (Tabelle 30), sind die hohen P-Gehalte warscheinlich auf gewässerinterne Umsetzungsprozesse rückführbar. SCHRAUTZER (2001) führt an, dass die Gefahr einer P-Freisetzung nach einer Überflutung in basenreichen, zuvor intensiv genutzten Niedermooren besonders hoch ist. Er geht jedoch davon aus, dass das ins Bodenwasser abgegebene Phosphat gleichzeitig von Mikroorganismen <strong>und</strong> höheren Pflanzen aufgenommen werden kann. SCHEFFER (1998) weist darauf hin, das sommerlich rasch erwärmende Flachwasserseen durch eine hohe mikrobielle Aktivität <strong>und</strong> einen schnell ablaufenden Stoffaustausch zwischen Sed<strong>im</strong>ent <strong>und</strong> dem gesamten Wasserkörper gekennzeichnet sind, woraus sich die hohen <strong>und</strong> teilweise schwankenden Nährstoffkonzentrationen ableiten ließen. Der Vergleich mit früheren Phosphatmessungen <strong>im</strong> ASB zeigt seit 1999 eine deutliche Abnahme auf 1/6 bis 1/7 in der IF Zartenstrom <strong>und</strong> auf 1/3 am Dauerpegel Bugewitz (Abbildung 47). Auch wenn die vom Autor ermittelten Orthophosphatkonzentrationen aufgr<strong>und</strong> der nur zwe<strong>im</strong>aligen Messung wenig repräsentativ sind, muss von einer deutlichen Abnahme ausgegangen werden, da die Gesamtphosphorgehalte von 2003 am Zartenstrom bereits nur noch 1/3 der Orthophosphatkonzentrationen von 1999 betragen. Einerseits konnte ein beträchtlicher Teil <strong>des</strong> Phosphates in der neu etablierten Vegetation gespeichert