Download (3638Kb) - tuprints
Download (3638Kb) - tuprints
Download (3638Kb) - tuprints
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Intensität [a.u.]<br />
Intensität [a.u.]<br />
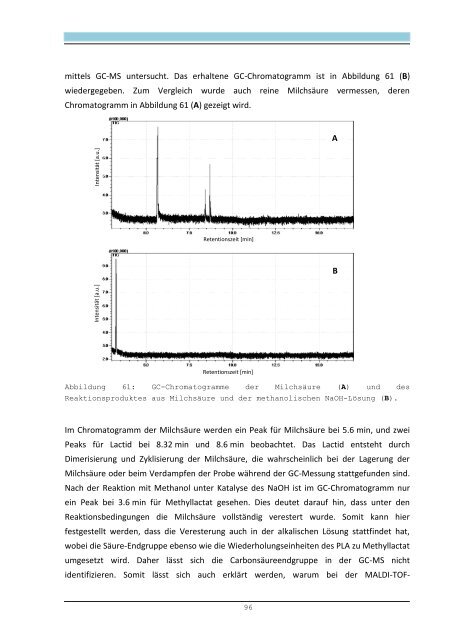
mittels GC-MS untersucht. Das erhaltene GC-Chromatogramm ist in Abbildung 61 (B)<br />
wiedergegeben. Zum Vergleich wurde auch reine Milchsäure vermessen, deren<br />
Chromatogramm in Abbildung 61 (A) gezeigt wird.<br />
A<br />
Retentionszeit [min]<br />
B<br />
Retentionszeit [min]<br />
Abbildung 61: GC-Chromatogramme der Milchsäure (A) und des<br />
Reaktionsproduktes aus Milchsäure und der methanolischen NaOH-Lösung (B).<br />
Im Chromatogramm der Milchsäure werden ein Peak für Milchsäure bei 5.6 min, und zwei<br />
Peaks für Lactid bei 8.32 min und 8.6 min beobachtet. Das Lactid entsteht durch<br />
Dimerisierung und Zyklisierung der Milchsäure, die wahrscheinlich bei der Lagerung der<br />
Milchsäure oder beim Verdampfen der Probe während der GC-Messung stattgefunden sind.<br />
Nach der Reaktion mit Methanol unter Katalyse des NaOH ist im GC-Chromatogramm nur<br />
ein Peak bei 3.6 min für Methyllactat gesehen. Dies deutet darauf hin, dass unter den<br />
Reaktionsbedingungen die Milchsäure vollständig verestert wurde. Somit kann hier<br />
festgestellt werden, dass die Veresterung auch in der alkalischen Lösung stattfindet hat,<br />
wobei die Säure-Endgruppe ebenso wie die Wiederholungseinheiten des PLA zu Methyllactat<br />
umgesetzt wird. Daher lässt sich die Carbonsäureendgruppe in der GC-MS nicht<br />
identifizieren. Somit lässt sich auch erklärt werden, warum bei der MALDI-TOF-<br />
96