HEARTLINE HSM Genoa Cardiology Meeting - Aristea
HEARTLINE HSM Genoa Cardiology Meeting - Aristea
HEARTLINE HSM Genoa Cardiology Meeting - Aristea
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
Sia in modelli di piccola che di grossa taglia è stata dimostrata la capacità di G-CSF di indurre<br />
neovascolarizzazione nelle zone perinfartuali e ridurre l’apoptosi di cellule endoteliali.<br />
In un modello di ischemia miocardica nel ratto la terapia con G-CSF protratta per giorni<br />
ha portato ad un migliorato signicativo della funzione cardiaca globale, attenuando il rimodellamento<br />
miocardico post-ischemico e incrementando il numero di capillari nelle zone<br />
perinfartuali, in assenza tuttavia di rigenerazione in senso cardiomiocitario. Benché il meccanismo<br />
di azione sia ancora oggetto di studio, è stato riportato da Ohki e Capoccia una<br />
stimolazione di neutroli e monociti mediata da G-CSF in grado di promuovere la neovascolarizzazione<br />
in tessuti ischemici attraverso meccanismi di tipo paracrino. Inoltre G-CSF<br />
mobilizza progenitori endoteliali (EPCs) i quali possono favorire l’angiogenesi e ridurre la<br />
progressione dell’aterosclerosi. Date le capacità di G-CSF di incrementare l’espressione<br />
di molecole di adesione e chemochine (SDF-1), è possibile che un forte aumento di cellule<br />
CXCR + , EPCs e leucociti circolanti sia responsabile dell’incremento della vascolarizzazione<br />
evidenziata in numerosi studi a livello perinfartuale. Oltre all’angiogenesi, è possibile<br />
che G-CSF, attraverso il coinvolgimento di molecole di adesione (ICAM-1), citochine e leucociti,<br />
stimoli anche l’arteriogenesi. A dimostrazione è stato riportato un aumento di ICAM-1,<br />
un accumulo di leucociti e una proliferazione di cellule endoteliali e muscolari lisce in seguito<br />
a somministrazione di G-CSF in un modello di IMA.<br />
L’infarto miocardico acuto è caratterizzato da stress ossidativo e stato inammatorio che<br />
inuenzano il successivo rimodellamento avverso del ventricolo sinistro. In seguito ad insulto<br />
ischemico, cellule inammatorie e miociti rilasciano citochine che agiscono nei processi<br />
di sopravvivenza, apoptosi, angiogenesi e alterazione della matrice cellulare. G-CSF<br />
endogeno ha dimostrato di esercitare un ruolo antinammatorio modulando il rilascio di citochine<br />
coinvolte nell’inammazione e nei processi di rimodellamento post-infartuale. In<br />
particolare, è dimostrato il coinvolgimento di un recettore specico per G-CSF a livello monocitario.<br />
Un effetto protettivo del G-CSF nei confronti dello stress ossidativo è stato ripor-<br />
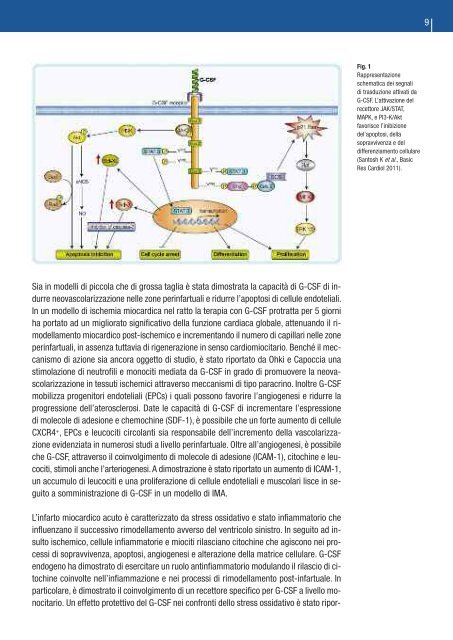
Fig. 1<br />
Rappresentazione<br />
schematica dei segnali<br />
di trasduzione attivati da<br />
G-CSF. L’attivazione del<br />
recettore JAK/STAT,<br />
MAPK, e PI -K/Akt<br />
favorisce l’inibizione<br />
del’apoptosi, della<br />
sopravvivenza e del<br />
differenziamento cellulare<br />
(Santosh K et al., Basic<br />
Res Cardiol 2011).<br />
9