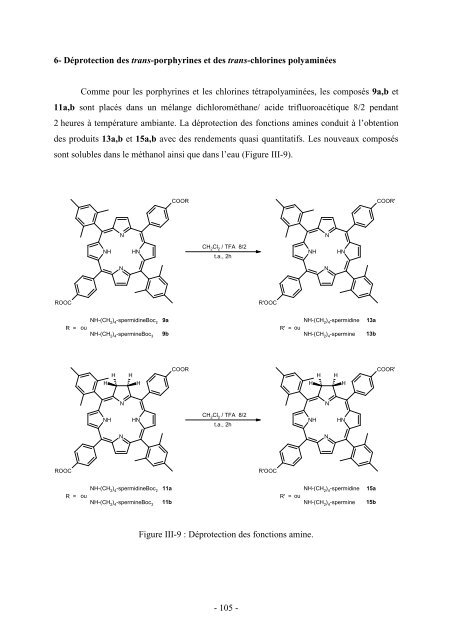
6- Déprotection des trans-<strong>porphyrines</strong> <strong>et</strong> des trans-<strong>chlorines</strong> <strong>polyaminées</strong> Comme pour les <strong>porphyrines</strong> <strong>et</strong> les <strong>chlorines</strong> tétra<strong>polyaminées</strong>, les composés 9a,b <strong>et</strong> 11a,b sont placés dans un mélange dichlorométhane/ acide trifluoroacétique 8/2 pendant 2 heures à température ambiante. La déprotection des fonctions amines conduit à l’obtention des produits 13a,b <strong>et</strong> 15a,b avec des rendements quasi quantitatifs. Les nouveaux composés sont solubles dans le méthanol ainsi que dans l’eau (Figure III-9). ROOC R = ROOC R = NH NH N N N N HN NH-(CH2 ) 4-spermidineBoc2 ou NH-(CH2 ) 4-spermineBoc3 H H H H HN NH-(CH2 ) 4-spermidineBoc2 ou NH-(CH2 ) 4-spermineBoc3 9a 9b 11a 11b COOR COOR CH 2 Cl 2 / TFA 8/2 t.a., 2h CH 2 Cl 2 / TFA 8/2 t.a., 2h - 105 - R'OOC R'OOC Figure III-9 : Déprotection des fonctions amine. NH H NH N N H H N N HN NH-(CH2 ) 4-spermidine R' = ou NH-(CH2 ) 4-spermine H HN NH-(CH2 ) 4-spermidine R' = ou NH-(CH2 ) 4-spermine 13a 13b 15a 15b COOR' COOR'
7- Caractérisations 7-1- Spectroscopie UV-visible Les spectres des composés protégés 9a,b <strong>et</strong> 11a,b, ainsi que celui de la trans-porphyrine 6, ont été réalisés dans le dichlorométhane. Pour les produits déprotégés 13a,b, <strong>et</strong> 15a,b, les mesures ont été effectuées dans le méthanol <strong>et</strong> dans l’eau. Le spectre de la trans-porphyrine dicarboxylique 7 a été réalisé uniquement dans le méthanol. Les résultats sont reportés dans le tableau III-1. Tableau III-1 : Bandes caractéristiques des spectres UV-visible des composés 6 - 7 - 9a,b - 11a,b - 13a,b <strong>et</strong> 15a,b. λmax (nm) [coefficient d’absorption (ε x10 -3 mol -1 .L.cm -1 )], à 20°C, (a : dans le dichlorométhane, b : dans le méthanol, c : dans l’eau). Composés Bande de Sor<strong>et</strong> Q IV Q III Q II Q I 6 a 419 (392,4) 515 (18,3) 549 (7,5) 591 (5,4) 648 (4,7) 7 b 414 (144,8) 512 (6,0) 546 (2,7) 589 (1,7) 645 (1,3) 9a a 419 (306,3) 515 (13,5) 549 (5,4) 591 (4,1) 646 (2,7) 9b a 419 (338,2) 515 (14,8) 549 (6,1) 590 (4,4) 646 (3,0) 11a a 420 (92,4) 520 (11,6) 546 (9,7) 598 (5,4) 654 (18,8) 11b a 420 (116,0) 519 (7,7) 546 (5,3) 598 (2,8) 652 (15,4) 13a b 415 (330,5) 513 (15,1) 546 (6,1) 589 (4,3) 645 (2,7) 13a c 414 (285,0) 517 (11,9) 533 (5,2) 581 (4,2) 635 (2,6) 13b b 415 (318,8) 513 (12,7) 545 (5,6) 589 (3,7) 646 (2,3) 13b c 414 (390,9) 517 (14,5) 552 (6,5) 581 (5,4) 634 (3,2) 15a b 416 (110,7) 518 (9,3) 543 (6,6) 597 (3,7) 651 (19,9) 15a c 415 (88,0) 521 (6,9) 548 (4,9) 596 (2,7) 650 (11,1) 15b b 416 (134,7) 516 (10,0) 544 (6,8) 596 (3,9) 651 (19,3) 15b c 415 (111,9) 520 (7,8) 548 (5,4) 595 (3,1) 649 (10,7) - 106 -
- Page 1:
JURY : Rapporteurs : UNIVERSITE DE
- Page 5:
REMERCIEMENTS
- Page 8 and 9:
J’adresse tous mes remerciements
- Page 11 and 12:
SOMMAIRE Remerciements.............
- Page 13 and 14:
8- Caractérisations...............
- Page 15 and 16:
LISTE DES ABREVIATIONS - 2 -
- Page 17 and 18:
ADN : acide désoxyribonucléique A
- Page 19 and 20:
INTRODUCTION GENERALE - 6 -
- Page 21 and 22:
INTRODUCTION GENERALE Les porphyrin
- Page 23 and 24:
CHAPITRE I : LES PORPHYRINES ET LES
- Page 25 and 26:
Chapitre I Les porphyrines et les c
- Page 27 and 28:
encore par la métallation. 3 Ainsi
- Page 29 and 30:
éduction. 6 On peut également cit
- Page 31 and 32:
Figure I-6 : Profil des bandes Q po
- Page 33 and 34:
Figure I-9 : Principe de la techniq
- Page 35 and 36:
Figure I-10 : Cône d’anisotropie
- Page 37 and 38:
zones : - Les carbones meso qui ré
- Page 39 and 40:
Calvin et coll. 15 ont montré qu'i
- Page 41 and 42:
Une autre approche permettant de fo
- Page 43 and 44:
types de substituants différents (
- Page 45 and 46:
dihydroxytétraphénylchlorine (Fig
- Page 47 and 48:
H 3 C 6 C 6 H 5 FeTTPCl PhIO FeTTPC
- Page 49 and 50:
Figure I-25 : Transformation photoc
- Page 51 and 52:
modèles animaux puis sur des humai
- Page 53 and 54:
photosensibilisateurs utilisés en
- Page 55 and 56:
Le dérivé d’hématoporphyrine (
- Page 57 and 58:
HO OH NH N N - 44 - HN HO Figure I-
- Page 59 and 60:
N Cl N Sn N - 46 - Cl N CO 2 Et Fig
- Page 61 and 62:
O H N OH 2 Porphobilinogène Uropor
- Page 63 and 64:
photosensibilisateurs semblent inad
- Page 65 and 66:
6- Les polyamines 72, 73 Figure I-3
- Page 67 and 68: NH 2 benzylamine N H 2 H N CN sperm
- Page 69 and 70: O Ar H Ar = phényl- 2-naphtyl- 9-a
- Page 71 and 72: polyamines est également en équil
- Page 73 and 74: Cette combinaison permet de réduir
- Page 75 and 76: 7- But du travail Compte tenu du r
- Page 77 and 78: NH NH N N HN N N HN O O O O NH N NH
- Page 79 and 80: CHAPITRE II : SYNTHESE DE PORPHYRIN
- Page 81 and 82: 1- Introduction Chapitre II Synthè
- Page 83 and 84: 2- Stratégie de synthèse Les éta
- Page 85 and 86: 3- Synthèse des précurseurs polya
- Page 87 and 88: obtenus avec des rendements respect
- Page 89 and 90: BocNH N O BocNH N N NH 2 O NHBoc 1)
- Page 91 and 92: O P O H O N N N + O H P _ O N + + N
- Page 93 and 94: H3C S N H O O NH 2 Δ - 80 - C H 3
- Page 95 and 96: 7- Caractérisations L’ensemble d
- Page 97 and 98: spectres comparatifs des porphyrine
- Page 99 and 100: 7-3- RMN du proton Les spectres de
- Page 101 and 102: - 88 - N NH N H NH O O O O O NH N N
- Page 103 and 104: Pyrrole Phényle Tableau II-4 : RMN
- Page 105 and 106: Nous observons la résonance des pr
- Page 107 and 108: CHAPITRE III : SYNTHESE DE PORPHYRI
- Page 109 and 110: 1- Introduction Chapitre III Synth
- Page 111 and 112: N NHR N NBoc R' NH NH 2 N H NHBoc H
- Page 113 and 114: Lindsey a réalisé une étude trè
- Page 115 and 116: distillé avec le meso-mésitaldéh
- Page 117: HOOC NH N N 7 HN COOH + N H 2 R N N
- Page 121 and 122: 7-2- Spectrométrie de masse MALDI
- Page 123 and 124: Figure III-12 : Groupe des principa
- Page 125 and 126: N H 2 O N NH NH 2 N N H 2 N H H N N
- Page 127 and 128: Tableau III-4 : RMN 1 H des chlorin
- Page 129 and 130: Nous observons cinq signaux (4 doub
- Page 131 and 132: CHAPITRE IV : SYNTHESE DE TRIMERES
- Page 133 and 134: 1- Introduction Chapitre IV Synthè
- Page 135 and 136: NH N N HN O O HO H H H H NH H H H H
- Page 137 and 138: C H 3 C H 3 NH N N HN + CH 3 50 éq
- Page 139 and 140: 6- Synthèse de la bis(hydroxyphén
- Page 141 and 142: C H 3 C H 3 C H 3 N N H H N CH 3 CH
- Page 143 and 144: superposition des spectres de chaqu
- Page 145 and 146: 8-3- RMN du proton L’attribution
- Page 147 and 148: Nous retrouvons, pour les porphyrin
- Page 149 and 150: H 3,5 7,53 m 7,51-7,56 m CH3 2,70 s
- Page 151 and 152: L’étude des spectres des momomè
- Page 153 and 154: CHAPITRE V : QUELQUES DONNEES PHARM
- Page 155 and 156: 1- Introduction Chapitre V Quelques
- Page 157 and 158: 4- Interaction avec l’ADN Figure
- Page 159 and 160: Nous constatons, pour ce composé,
- Page 161 and 162: formes d’ADN. En absence de photo
- Page 163 and 164: composés pour l’ADN (paragraphe
- Page 165 and 166: - 152 -
- Page 167 and 168: - 154 -
- Page 169 and 170:
- 156 -
- Page 171 and 172:
Hydrazine monohydrate 98% Aldrich H
- Page 173 and 174:
3- Chromatographie - Chromatographi
- Page 175 and 176:
7- Photoclivage de l’ADN Le photo
- Page 177 and 178:
49,4 (CH2α), 47,7 (CH2α'), 40,4 (
- Page 179 and 180:
SM Haute Résolution: Calculée pou
- Page 181 and 182:
Trouvée : m/z 417,3440 [M+H] + . N
- Page 183 and 184:
5,15-bis(4-méthylesterphényl) 10,
- Page 185 and 186:
5,10,15,20-tétrakis (N 1 ,N 8 -bis
- Page 187 and 188:
5,15-bis (N 1 ,N 8 -bis-tert-butoxy
- Page 189 and 190:
Procédure générale de réduction
- Page 191 and 192:
5,10,15,20-tétrakis (N 1 ,N 8 ,N 1
- Page 193 and 194:
5,15-bis (N 1 ,N 8 ,N 12 -tris-tert
- Page 195 and 196:
5,10,15,20-tétrakis (spermidine (N
- Page 197 and 198:
5,15-bis (spermidine (N 4 -(4-amino
- Page 199 and 200:
5,10,15,20-tétrakis (spermidine (N
- Page 201 and 202:
5,15-bis (spermidine (N 4 -(4-amino
- Page 203 and 204:
5-(4-hydroxyphényl)-10,15,20-trito
- Page 205 and 206:
5,15-bis (4-hydroxyphényl) 10,20-b
- Page 207 and 208:
5,15 bis (phényl(5-(4-propyloxyph
- Page 209 and 210:
- 196 -
- Page 211 and 212:
- 198 -
- Page 213 and 214:
HOOC HOOC H 3 COOC NH NH N N 4 N HN
- Page 215 and 216:
- 202 - N H O O N O O N H O O N H O
- Page 217 and 218:
N H 2 HN N H 2 HN NH2 N H 2 NH 2 N
- Page 219 and 220:
HO NH NH N N 16 N N 18 HN HN OH OH
- Page 221 and 222:
Figure I-1 ; Les différentes class
- Page 223:
Figure IV-8 : Spectre UV-visible du
- Page 227:
thicker or more profound tumors. We