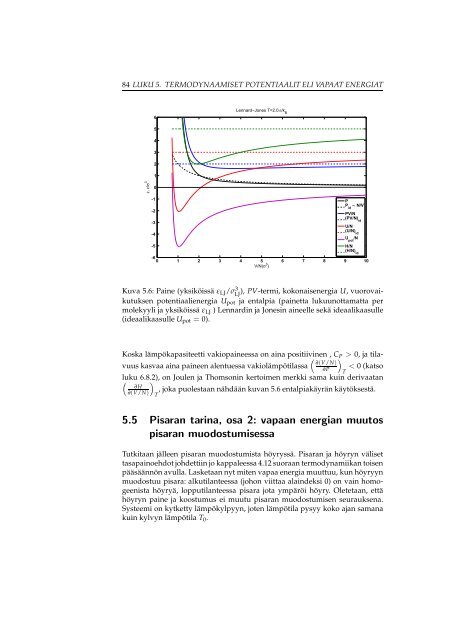
84 LUKU 5. TERMODYNAAMISET POTENTIAALIT ELI VAPAAT ENERGIAT6Lennard−Jones T=2.0 ε/k B54321ε, ε/σ 30-1PPid ∝ N/V-2-3-4PV/N(PV/N) idU/N(U/N) idU pot/N-5H/N(H/N) id-60 1 2 3 4 5 6 7 8 9 10V/N(σ 3 )Kuva 5.6: Paine (yksiköissä ε LJ /σLJ 3 ), PV-termi, kokonaisenergia U, vuorovaikutuksenpotentiaalienergia U pot <strong>ja</strong> entalpia (painetta lukuunottamatta permolekyyli <strong>ja</strong> yksiköissä ε LJ ) Lennardin <strong>ja</strong> Jonesin aineelle sekä ideaalikaasulle(ideaalikaasulle U pot = 0).Koska lämpökapasiteetti vakiopaineessa on aina positiivinen(, C) P > 0, <strong>ja</strong> tilavuuskasvaa aina paineen alentuessa vakiolämpötilassa ∂(V/N)∂P< 0 (katsoTluku 6.8.2),)on Joulen <strong>ja</strong> Thomsonin kertoimen merkki sama kuin derivaatan, joka puolestaan nähdään kuvan 5.6 entalpiakäyrän käytöksestä.(∂H∂(V/N)T5.5 Pisaran tarina, osa 2: vapaan energian muutospisaran muodostumisessaTutkitaan jälleen pisaran muodostumista höyryssä. Pisaran <strong>ja</strong> höyryn välisettasapainoehdot johdettiin jo kappaleessa 4.12 suoraan termodynamiikan toisenpääsäännön avulla. Lasketaan nyt miten vapaa energia muuttuu, kun höyryynmuodostuu pisara: alkutilanteessa (johon viittaa alaindeksi 0) on vain homogeenistahöyryä, lopputilanteessa pisara jota ympäröi höyry. Oletetaan, ettähöyryn paine <strong>ja</strong> koostumus ei muutu pisaran muodostumisen seurauksena.Systeemi on kytketty lämpökylpyyn, joten lämpötila pysyy koko a<strong>ja</strong>n samanakuin kylvyn lämpötila T 0 .
5.5. PISARAN TARINA, OSA 2: VAPAAN ENERGIAN MUUTOS PISARANMUODOSTUMISESSA 85Homogeenisen höyryn tai nesteen energia voidaan lausua muodossaU = T 0 S− PV + ∑ µ i N i ,<strong>ja</strong> faasien välisen ra<strong>ja</strong>pinnan (pinta-ala A) energia muodossaU = T 0 S+ Aσ+∑ µ i N i .Alkutilanteessa on vain höyryn (k) energiaaU 0 = T 0 S 0 − P 0 V 0 + ∑ µ 0 i,k N0 i,k .Lopputilanteessa systeemin kokonaisenergia on summa höyryn, nesteen (n) <strong>ja</strong>ra<strong>ja</strong>pinnan(p) energioistaU = T 0 (S k + S n + S p )−P k V k − P n V n + σA+ ∑ µ i,k N i,k + ∑ µ i,n N i,n + ∑ µ i,p N i,p= T 0 S tot − P k V k − P n V n + σA+ ∑ µ i,k N i,k + ∑ µ i,n N i,n + ∑ µ i,p N i,p ,missä S tot = S k + S n + S p . Tässä tapauksessa sopiva vapaa energia voidaanvalita ainakin kolmella eri tavalla. Oikea valinta riippuu siitä, mikä todellisessakoetilanteessa tai a<strong>ja</strong>tuskokeessa pysyy vakiona.1. Pidetään ensin kaasufaasin (höyryn) kemiallinen potentiaali µ i,k = µ 0 i,k<strong>ja</strong> systeemin kokonaistilavuus V 0 = V k + V n vakioina. Tämä edellyttää,että systeemiin lisätään hiukkasia, jos kemiallinen potentiaali pyrkii laskemaan,<strong>ja</strong> poistetaan, jos kemiallinen potentiaali pyrkii nousemaanSuuri potentiaali on tällöin sopiva termodynaaminen potentiaali, <strong>ja</strong> alkutilassase onΩ 0 = U 0 − T 0 S 0 − ∑ µ 0 i,k N0 i,k = −P 0V 0 = −P 0 (V n + V k ).Lopputilan suuri potentiaali onΩ = U−T 0 S tot − ∑ µ 0 i,k N i,tot = U−T 0 S tot − ∑ µ 0 i,k (N i,k+N i,n + N i,p )= −P k V k − P n V n + σA+∑(µ i,n − µ 0 i,k )N i,n+∑(µ i,p − µ 0 i,k )N i,p.Suuren potentiaalin muutos pisaran muodostumisessa on siten∆Ω =(P 0 − P n )V n +(P 0 − P k )V k + σA+ ∑(µ i,n − µ 0 i,k )N i,n+∑(µ i,p − µ 0 i,k )N i,p.Jos oletamme, että paitsi kaasun kemialliset potentiaalit µ i,k , myös kaasunkoostumus x i,k pysyy muuttumattomana myös kaasun paineen onpysyttävä vakiona Maxwellin relaation (5.13)( ∂V∂N i)T,P,N j̸=i=( ) ∂µ∂PT,N i
- Page 1 and 2:
TermofysiikanperusteetIsmo Napari j
- Page 3 and 4:
SISÄLTÖiii4.6 Entropia (5.3) . .
- Page 5 and 6:
Luku 1Johdanto1.1 Termofysiikan osa
- Page 7 and 8:
1.3. IDEAALIKAASUN TILANYHTÄLÖ (1
- Page 9 and 10:
1.3. IDEAALIKAASUN TILANYHTÄLÖ (1
- Page 11 and 12:
1.4. ESIMERKKEJÄ TILANYHTÄLÖIST
- Page 13 and 14:
2.2. LÄMPÖMITTARIT JA LÄMPÖTILA
- Page 15 and 16:
2.2. LÄMPÖMITTARIT JA LÄMPÖTILA
- Page 17 and 18:
3.1. TYÖ (2.2, 2.7) 13ten, että j
- Page 19 and 20:
3.2. EKSAKTIT JA EPÄEKSAKTIT DIFFE
- Page 21 and 22:
3.2. EKSAKTIT JA EPÄEKSAKTIT DIFFE
- Page 23 and 24:
3.3. TERMODYNAMIIKAN ENSIMMÄINEN P
- Page 25 and 26:
3.4. LÄMPÖKAPASITEETIT (2.5) 21Er
- Page 27 and 28:
3.5. KVASISTAATTISIA IDEAALIKAASUPR
- Page 29 and 30:
3.5. KVASISTAATTISIA IDEAALIKAASUPR
- Page 31 and 32:
3.5. KVASISTAATTISIA IDEAALIKAASUPR
- Page 33 and 34:
Luku 4Termodynamiikan toinenpääs
- Page 35 and 36:
4.1. TOINEN PÄÄSÄÄNTÖ JA CARNO
- Page 37 and 38: 4.1. TOINEN PÄÄSÄÄNTÖ JA CARNO
- Page 39 and 40: 4.3. CARNOT’N JÄÄKAAPPI JA LÄM
- Page 41 and 42: 4.4. IDEAALIKAASUKONEITA (5.2) 3754
- Page 43 and 44: 4.4. IDEAALIKAASUKONEITA (5.2) 39el
- Page 45 and 46: 4.5. CLAUSIUKSEN EPÄYHTÄLÖ (5.6)
- Page 47 and 48: 4.6. ENTROPIA (5.3) 43Systeemid¯W
- Page 49 and 50: 4.6. ENTROPIA (5.3) 45Adiabaattises
- Page 51 and 52: 4.7. SISÄINEN ENERGIA JA MAXWELLIN
- Page 53 and 54: 4.7. SISÄINEN ENERGIA JA MAXWELLIN
- Page 55 and 56: 4.8. ESIMERKKEJÄ ENTROPIAN MUUTOKS
- Page 57 and 58: 4.8. ESIMERKKEJÄ ENTROPIAN MUUTOKS
- Page 59 and 60: 4.9. ENTROPIAN DIFFERENTIAALI JA ER
- Page 61 and 62: 4.9. ENTROPIAN DIFFERENTIAALI JA ER
- Page 63 and 64: 4.11. TERMODYNAMIIKAN PÄÄSÄÄNN
- Page 65 and 66: 4.12. PISARAN TARINA, OSA 1: TAUSTA
- Page 67 and 68: 4.12. PISARAN TARINA, OSA 1: TAUSTA
- Page 69 and 70: 4.12. PISARAN TARINA, OSA 1: TAUSTA
- Page 71 and 72: 5.2. YMPÄRISTÖN KANSSA VUOROVAIKU
- Page 73 and 74: 5.2. YMPÄRISTÖN KANSSA VUOROVAIKU
- Page 75 and 76: 5.2. YMPÄRISTÖN KANSSA VUOROVAIKU
- Page 77 and 78: 5.3. VAPAAT ENERGIAT JA NIIDEN TASA
- Page 79 and 80: 5.3. VAPAAT ENERGIAT JA NIIDEN TASA
- Page 81 and 82: 5.4. MIKSI TERMODYNAAMISIA POTENTIA
- Page 83 and 84: 5.4. MIKSI TERMODYNAAMISIA POTENTIA
- Page 85 and 86: 5.4. MIKSI TERMODYNAAMISIA POTENTIA
- Page 87: 5.4. MIKSI TERMODYNAAMISIA POTENTIA
- Page 91 and 92: 5.5. PISARAN TARINA, OSA 2: VAPAAN
- Page 93 and 94: Luku 6Faasien ja faasimuutostenterm
- Page 95 and 96: 6.3. STABIILISUUS 91Kuva 6.1: Vakaa
- Page 97 and 98: 6.4. FAASIDIAGRAMMI JA GIBBSIN FAAS
- Page 99 and 100: 6.4. FAASIDIAGRAMMI JA GIBBSIN FAAS
- Page 101 and 102: 6.5. FAASIMUUTOKSEN KERTALUKU 97esi
- Page 103 and 104: 6.6. VAPAA ENERGIA-DIAGRAMMIT (8.1)
- Page 105 and 106: 6.7. CLAUSIUKSEN JA CLAPEYRONIN YHT
- Page 107 and 108: 6.7. CLAUSIUKSEN JA CLAPEYRONIN YHT
- Page 109 and 110: 6.8. FAASIMUUTOKSET JA VAN DER WAAL
- Page 111 and 112: 6.8. FAASIMUUTOKSET JA VAN DER WAAL
- Page 113 and 114: 6.8. FAASIMUUTOKSET JA VAN DER WAAL
- Page 115 and 116: 6.8. FAASIMUUTOKSET JA VAN DER WAAL
- Page 117 and 118: 6.9. PISARAN TARINA, OSA 3: TASAPAI
- Page 119 and 120: 6.9. PISARAN TARINA, OSA 3: TASAPAI
- Page 121 and 122: 6.9. PISARAN TARINA, OSA 3: TASAPAI
- Page 123 and 124: 6.9. PISARAN TARINA, OSA 3: TASAPAI
- Page 125 and 126: Luku 7Liuosten termodynamiikkaa7.1
- Page 127 and 128: 7.1. PARTIAALISET MOLEKYYLISUUREET
- Page 129 and 130: 7.2. LAIMEIDEN LIUOSTEN HÖYRYNPAIN
- Page 131 and 132: 7.3. OSMOOSI 127lisessä kappaleess
- Page 133: 129eliValitaan ensin dx ̸= 0 ja dz