urn:nbn:de:hbz:468-20130312-112320-7 - Bergische Universität ...
urn:nbn:de:hbz:468-20130312-112320-7 - Bergische Universität ...
urn:nbn:de:hbz:468-20130312-112320-7 - Bergische Universität ...
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
4. Indoloindol-basierte Polymere 75<br />
4.3.3 Poly[3,8-(5,10-dido<strong>de</strong>cyl-5,10-dihydroindolo[3,2-b]indol)-alt-4,7-<br />
[2,1,3]benzothiadiazol] (PInInBT) und Poly[3,8-(5,10-dido<strong>de</strong>cyl-5,10-dihydroindolo[3,2-<br />
b]indol)-alt-4,7-(bis(thiophen-2-yl)-[2,1,3]benzothiadiazol)] (PInInTBTT)<br />
PInInBT wur<strong>de</strong> wie zuvor PInInSiF und PInInF konventionell über eine Suzuki-<br />
Kreuzkupplungsreaktion hergestellt. Da das verwen<strong>de</strong>te TBBT-Monomer distannyliert vorlag,<br />
wur<strong>de</strong> das Polymer mit <strong>de</strong>n zusätzlichen „Thiophenspacern“, PInInTBTT,<br />
mikrowellenunterstützt über eine Stille-Kupplung synthetisiert (s. Schema 15). Das<br />
verwen<strong>de</strong>te Monomer, 4,7-(Di(5-(tributylstannyl)thiophen-2-yl)benzo[c][1,2,5]thiadiazol<br />
(62), wur<strong>de</strong> von Dr. Ramkumar Santhanagopal zur Verfügung gestellt.<br />
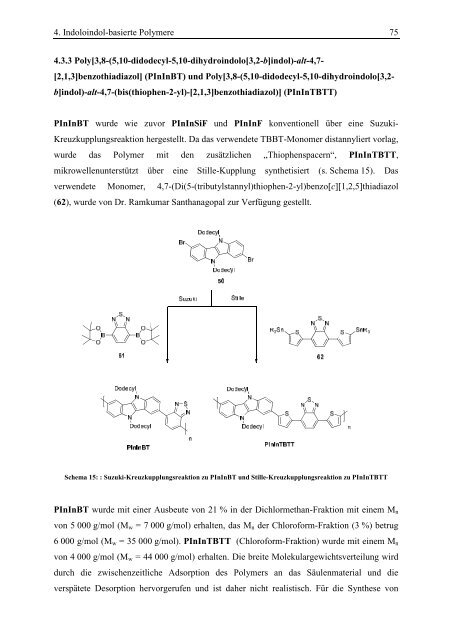
Schema 15: : Suzuki-Kreuzkupplungsreaktion zu PInInBT und Stille-Kreuzkupplungsreaktion zu PInInTBTT<br />
PInInBT wur<strong>de</strong> mit einer Ausbeute von 21 % in <strong>de</strong>r Dichlormethan-Fraktion mit einem M n<br />
von 5 000 g/mol (M w = 7 000 g/mol) erhalten, das M n <strong>de</strong>r Chloroform-Fraktion (3 %) betrug<br />
6 000 g/mol (M w = 35 000 g/mol). PInInTBTT (Chloroform-Fraktion) wur<strong>de</strong> mit einem M n<br />
von 4 000 g/mol (M w = 44 000 g/mol) erhalten. Die breite Molekulargewichtsverteilung wird<br />
durch die zwischenzeitliche Adsorption <strong>de</strong>s Polymers an das Säulenmaterial und die<br />
verspätete Desorption hervorgerufen und ist daher nicht realistisch. Für die Synthese von