133 Experimenteller Teil 1 H NMR (600 MHz, CD2Cl2) δ/ppm = 8.22 (d, 4 JHH = 2.0 Hz, 2 H, 4-H), 8.18 (2 H, 7-H), 7.73 (d, 4 JHH = 2.0 Hz, 2 H, 6-H), 7.14 (4 H, 10-H), 4.04 (2 H, 14-H), 2.98 (sept, 3 JHH = 6.8 Hz, 4 H, 12-H), 1.21 (d, 3 JHH = 6.8 Hz, 24 H, 13-H). 13 C NMR (151 MHz, CD2Cl2) δ/ppm = 165.09 (C 7 ), 160.59 (C 2 ), 149.31 (C 4 ), 143.01 (C 8 ), 140.80 (C 6 ), 139.10 (C 9 ), 138.99 (C 11 ), 123.82 (C 10 ), 120.31 (C 1 ), 87.05 (C 5 ), 79.64 (C 3 ), 41.75 (C 14 ), 28.26 (C 12 ), 23.44 (C 13 ). EA für C39H42I4N2O2 (M = 1078.38 g mol -1 ). berechnet: C 43.44 % H 3.93 % N 2.60 % gef<strong>und</strong>en: C 43.47 % H 4.20 % N 2.53 % ES-MS m/z = 1077.9 (M + ). [{(2,6-(3,5-(CF3)2C6H3)2-4-yl-C6H2)-N=C(H)-(3,5-I2-2-(OH)-C6H2)}2] CF3Benz/I Blass-gelber Feststoff; Ausbeute: 79 % 1 H NMR (400 MHz, CD2Cl2) δ/ppm = 12.94 (2 H, OH), 8.14 (d, 4 JHH = 1.5 Hz, 2 H, 4-H), 8.01 (8 H, 13-H), 7.95 (4 H, 15-H), 7.90 (6 H, 7-H, 10-H), 7.29 (d, 4 JHH = 1.5 Hz, 2 H, 6-H). I I F 3C OH F 3C CF 3 13 C NMR (101 MHz, CD2Cl2) δ ppm 168.04 (C 7 ), 159.76 (C 2 ), 150.53 (C 4 ), 144.51 (C 8 ), 140.73 (C 6 ), 140.39 (C 12 ), 138.15 (C 11 ), 133.17 (C 9 ), 131.95 (q, 2 JCF = 33.7 Hz, C 14 ), 130.16 (C 13 ), 129.94 (C 10 ), 123.24 (q, 1 JCF = 272.5 Hz, C 16 ), 121.78 (C 15 ), 119.33 (C 1 ), 86.55 (C 5 ), 80.15 (C 3 ). F3C 15 16 CF3 14 13 6 10 9 12 7 1 N 11 8 N 2 HO CF 3 F 3C CF 3 5 3 I I 4
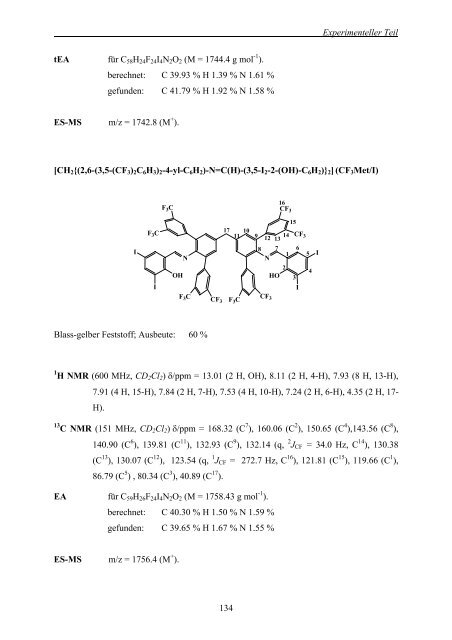
tEA für C58H24F24I4N2O2 (M = 1744.4 g mol -1 ). berechnet: C 39.93 % H 1.39 % N 1.61 % gef<strong>und</strong>en: C 41.79 % H 1.92 % N 1.58 % ES-MS m/z = 1742.8 (M + ). 134 Experimenteller Teil [CH2{(2,6-(3,5-(CF3)2C6H3)2-4-yl-C6H2)-N=C(H)-(3,5-I2-2-(OH)-C6H2)}2] (CF3Met/I) Blass-gelber Feststoff; Ausbeute: 60 % 1 H NMR (600 MHz, CD2Cl2) δ/ppm = 13.01 (2 H, OH), 8.11 (2 H, 4-H), 7.93 (8 H, 13-H), 7.91 (4 H, 15-H), 7.84 (2 H, 7-H), 7.53 (4 H, 10-H), 7.24 (2 H, 6-H), 4.35 (2 H, 17- H). 13 C NMR (151 MHz, CD2Cl2) δ/ppm = 168.32 (C 7 ), 160.06 (C 2 ), 150.65 (C 4 ),143.56 (C 8 ), 140.90 (C 6 ), 139.81 (C 11 ), 132.93 (C 9 ), 132.14 (q, 2 JCF = 34.0 Hz, C 14 ), 130.38 (C 13 ), 130.07 (C 12 ), 123.54 (q, 1 JCF = 272.7 Hz, C 16 ), 121.81 (C 15 ), 119.66 (C 1 ), 86.79 (C 5 ) , 80.34 (C 3 ), 40.89 (C 17 ). EA für C59H26F24I4N2O2 (M = 1758.43 g mol -1 ). berechnet: C 40.30 % H 1.50 % N 1.59 % gef<strong>und</strong>en: C 39.65 % H 1.67 % N 1.55 % ES-MS m/z = 1756.4 (M + ). I F 3C I F 3C 16 CF3 17 11 10 9 12 13 N 8 N 7 1 6 2 OH HO 3 I F3C F3C CF3 14 15 CF 3 CF 3 5 4 I
- Seite 1 und 2:
Polymerisation von Ethylen und 1-Ol
- Seite 3 und 4:
Danksagung Mein Dank gilt all denen
- Seite 5 und 6:
Inhaltsverzeichnis Inhaltsverzeichn
- Seite 7 und 8:
Inhaltsverzeichnis 8.5.4. Ethylenpo
- Seite 9 und 10:
Inhaltsverzeichnis Abb. 3-12 Schema
- Seite 11 und 12:
Inhaltsverzeichnis Abb. 6-18 DSC-Sp
- Seite 13 und 14:
py Pyridinato SDS Natriumdodecylsul
- Seite 15 und 16:
TON UV Ultraviolett Stoffmenge umge
- Seite 17 und 18:
CF3Met/I Komplexe i Pr/I*py : L = p
- Seite 19 und 20:
1. Einleitung 1 Einleitung Wasser a
- Seite 21 und 22:
1.1. Methodisches und Terminologie
- Seite 23 und 24:
5 Einleitung bildendes Polymer den
- Seite 25 und 26:
7 Einleitung verschiedene Katalysat
- Seite 27 und 28:
Phosphinoenolato-Komplexe 9 Einleit
- Seite 29 und 30:
1.2.2. Darstellung von Polyethylenl
- Seite 31 und 32:
13 Einleitung Für die von Brookhar
- Seite 33 und 34:
15 Einleitung 20-mal mehr Polymerpa
- Seite 35 und 36:
17 Einleitung Spektroskopische Unte
- Seite 37 und 38:
19 Einleitung in Wasser zu einer Mi
- Seite 39 und 40:
21 Einleitung Miniemulsion dispergi
- Seite 41 und 42:
23 Einleitung Lösungsmitteln gelö
- Seite 43 und 44:
25 Aufgabenstellung Die bislang beo
- Seite 45 und 46:
27 Polymerisation von 1-Olefinen an
- Seite 47 und 48:
29 Polymerisation von 1-Olefinen Si
- Seite 49 und 50:
31 Polymerisation von 1-Olefinen vo
- Seite 51 und 52:
3.2.2. Polymermikrostruktur 33 Poly
- Seite 53 und 54:
35 Polymerisation von 1-Olefinen Di
- Seite 55 und 56:
37 Polymerisation von 1-Olefinen Mo
- Seite 57 und 58:
39 Polymerisation von 1-Olefinen St
- Seite 59 und 60:
41 Polymerisation von 1-Olefinen 3.
- Seite 61 und 62:
Volume (%) 15 10 5 0 10 100 Abb. 3-
- Seite 63 und 64:
45 Polymerisation von 1-Olefinen Wi
- Seite 65 und 66:
Aktivierung von Salicylaldiminato-N
- Seite 67 und 68:
Aktivierung von Salicylaldiminato-N
- Seite 69 und 70:
Aktivierung von Salicylaldiminato-N
- Seite 71 und 72:
Aktivierung von Salicylaldiminato-N
- Seite 73 und 74:
Aktivierung von Salicylaldiminato-N
- Seite 75 und 76:
57 Versuch Katalysator Bedingungen
- Seite 77 und 78:
Aktivierung von Salicylaldiminato-N
- Seite 79 und 80:
Aktivierung von Salicylaldiminato-N
- Seite 81 und 82:
Aktivierung von Salicylaldiminato-N
- Seite 83 und 84:
Aktivierung von Salicylaldiminato-N
- Seite 85 und 86:
Aktivierung von Salicylaldiminato-N
- Seite 87 und 88:
Aktivierung von Salicylaldiminato-N
- Seite 89 und 90:
Aktivierung von Salicylaldiminato-N
- Seite 91 und 92:
Aktivierung von Salicylaldiminato-N
- Seite 93 und 94:
Polymerisation in Gegenwart polarer
- Seite 95 und 96:
Polymerisation in Gegenwart polarer
- Seite 97 und 98:
Polymerisation in Gegenwart polarer
- Seite 99 und 100:
Polymerisation in Gegenwart polarer
- Seite 101 und 102: 82 Versuch Katalysator Bedingungen
- Seite 103 und 104: Polymerisation in Gegenwart polarer
- Seite 105 und 106: Zweikernige Salicylaldiminato-Ni(II
- Seite 107 und 108: Zweikernige Salicylaldiminato-Ni(II
- Seite 109 und 110: 6.2. Liganden- und Komplex-Synthese
- Seite 111 und 112: Zweikernige Salicylaldiminato-Ni(II
- Seite 113 und 114: Zweikernige Salicylaldiminato-Ni(II
- Seite 115 und 116: Zweikernige Salicylaldiminato-Ni(II
- Seite 117 und 118: Zweikernige Salicylaldiminato-Ni(II
- Seite 119 und 120: Zweikernige Salicylaldiminato-Ni(II
- Seite 121 und 122: 102 Versuch Bedingungen Katalysator
- Seite 123 und 124: Zweikernige Salicylaldiminato-Ni(II
- Seite 125 und 126: Zweikernige Salicylaldiminato-Ni(II
- Seite 127 und 128: Zweikernige Salicylaldiminato-Ni(II
- Seite 129 und 130: Zweikernige Salicylaldiminato-Ni(II
- Seite 131 und 132: 7.1. Polymerisation von 1-Olefinen
- Seite 133 und 134: 114 Zusammenfassende Diskussion 7.2
- Seite 135 und 136: 116 Zusammenfassende Diskussion Rea
- Seite 137 und 138: 118 Zusammenfassende Diskussion pol
- Seite 139 und 140: 120 Zusammenfassende Diskussion ode
- Seite 141 und 142: 122 Experimenteller Teil Benzol-d 6
- Seite 143 und 144: 2,2‘,6,6‘-Tetraisopropylbenzidi
- Seite 145 und 146: 3,3‘,5,5‘-Tetrabrom-4,4‘-diam
- Seite 147 und 148: EA für C45H22F24N2 (M = 1046.63 g
- Seite 149 und 150: 130 Experimenteller Teil 13 C NMR (
- Seite 151: [{(2,6- i Pr2-4-yl-C6H2)-N=C(H)-(3,
- Seite 155 und 156: 136 Experimenteller Teil Zu einer S
- Seite 157 und 158: Orange-roter Feststoff; Ausbeute: 8
- Seite 159 und 160: Orangener Feststoff; Ausbeute: 82 %
- Seite 161 und 162: 8.4.2. Einkernige Salicylaldiminato
- Seite 163 und 164: 8.4.3. Triphenylphosphin-Komplexe 1
- Seite 165 und 166: 31 P NMR (162 MHz, C6D6) δ/ppm = 2
- Seite 167 und 168: 148 Experimenteller Teil etwas Tolu
- Seite 169 und 170: 150 Experimenteller Teil organische
- Seite 171 und 172: 8.6. Messmethoden und Geräte 8.6.1
- Seite 173 und 174: Verzweigungen 1000 C-Atome 154 Expe
- Seite 175 und 176: 156 Experimenteller Teil betrieben.
- Seite 177 und 178: 158 Experimenteller Teil 4. Mit den
- Seite 179 und 180: 160 Experimenteller Teil Kernresona
- Seite 181 und 182: 20 G. W. Coates, P. D. Hustad, S. R
- Seite 183 und 184: 66 K. A. Ostoja-Starzewski, J. Witt
- Seite 185 und 186: 113 N. R. Grove, P. A. Kohl, S. A.
- Seite 187 und 188: 155 C. Pellecchia, A. Zambelli, Mac
- Seite 189: 200 J. C. Randall, JMS-Rev. Macromo