Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
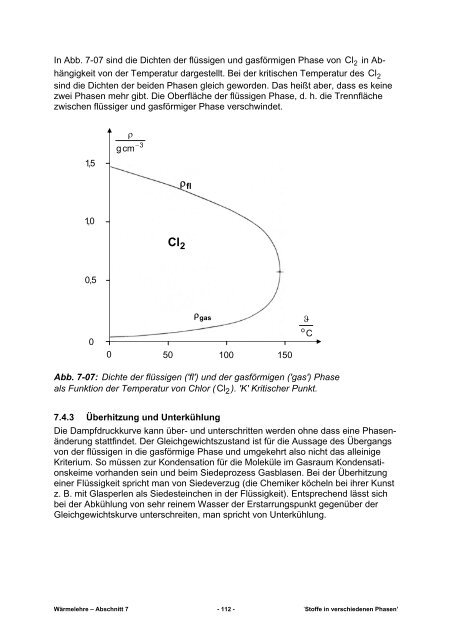
In Abb. 7-07 sind die Dichten der flüssigen und gasförmigen Phase von Cl 2 in Abhängigkeit<br />
von der Temperatur dargestellt. Bei der kritischen Temperatur des Cl 2<br />
sind die Dichten der beiden Phasen gleich geworden. Das heißt aber, dass es keine<br />
zwei Phasen mehr gibt. Die Oberfläche der flüssigen Phase, d. h. die Trennfläche<br />
zwischen flüssiger und gasförmiger Phase verschwindet.<br />
1 ,5<br />
ρ<br />
g cm<br />
−3<br />
ρ fl<br />
1 ,0<br />
Cl 2<br />
0 ,5<br />
0<br />
ρ gas<br />
0 50 100<br />
150<br />
ϑ<br />
o<br />
C<br />
Abb. 7-07: Dichte der flüssigen ('fl') und der gasförmigen ('gas') Phase<br />
als Funktion der Temperatur von Chlor ( Cl 2 ). 'K' Kritischer Punkt.<br />
7.4.3 Überhitzung und Unterkühlung<br />
Die Dampfdruckkurve kann über- und unterschritten werden ohne dass eine Phasenänderung<br />
stattfindet. Der Gleichgewichtszustand ist für die Aussage des Übergangs<br />
von der flüssigen in die gasförmige Phase und umgekehrt also nicht das alleinige<br />
Kriterium. So müssen zur Kondensation für die Moleküle im Gasraum Kondensationskeime<br />
vorhanden sein und beim Siedeprozess Gasblasen. Bei der Überhitzung<br />
einer Flüssigkeit spricht man von Siedeverzug (die Chemiker köcheln bei ihrer Kunst<br />
z. B. mit Glasperlen als Siedesteinchen in der Flüssigkeit). Entsprechend lässt sich<br />
bei der Abkühlung von sehr reinem Wasser der Erstarrungspunkt gegenüber der<br />
Gleichgewichtskurve unterschreiten, man spricht von Unterkühlung.<br />
<strong>Wärmelehre</strong> – Abschnitt 7<br />
- 112 -<br />
’Stoffe in verschiedenen Phasen’















![[1.5pt] Wellenlehre[8.5pt] Zusammenfassung - gilligan-online](https://img.yumpu.com/21507627/1/184x260/15pt-wellenlehre85pt-zusammenfassung-gilligan-online.jpg?quality=85)