Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
3.2.5.3 Gase<br />
Gase zeigen eine besonders interessante Temperaturabhängigkeit der (spezifischen<br />
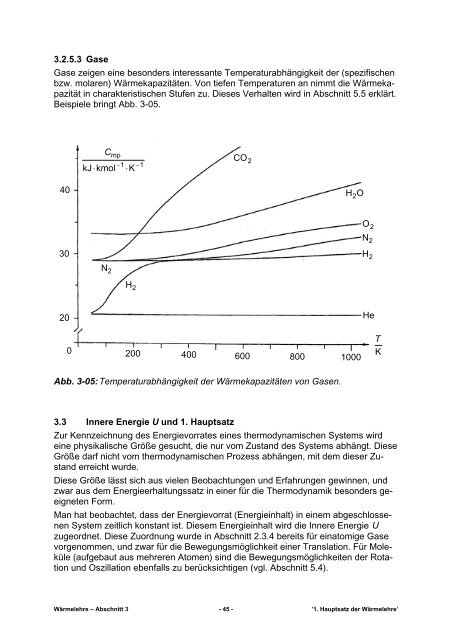
bzw. molaren) Wärmekapazitäten. Von tiefen Temperaturen an nimmt die Wärmekapazität<br />
in charakteristischen Stufen zu. Dieses Verhalten wird in Abschnitt 5.5 erklärt.<br />
Beispiele bringt Abb. 3-05.<br />
C<br />
kJ⋅kmol<br />
mp<br />
− 1<br />
⋅K<br />
−1<br />
CO 2<br />
40<br />
O H 2<br />
30<br />
N 2<br />
H 2<br />
O 2<br />
N<br />
2<br />
H 2<br />
20<br />
He<br />
0<br />
200 400 600 800 1000<br />
T<br />
K<br />
Abb. 3-05: Temperaturabhängigkeit der Wärmekapazitäten von Gasen.<br />
3.3 Innere Energie U und 1. Hauptsatz<br />
Zur Kennzeichnung des Energievorrates eines thermodynamischen Systems wird<br />
eine physikalische Größe gesucht, die nur vom Zustand des Systems abhängt. Diese<br />
Größe darf nicht vom thermodynamischen Prozess abhängen, mit dem dieser Zustand<br />
erreicht wurde.<br />
Diese Größe lässt sich aus vielen Beobachtungen und Erfahrungen gewinnen, und<br />
zwar aus dem Energieerhaltungssatz in einer für die Thermodynamik besonders geeigneten<br />
Form.<br />
Man hat beobachtet, dass der Energievorrat (Energieinhalt) in einem abgeschlossenen<br />
System zeitlich konstant ist. Diesem Energieinhalt wird die Innere Energie U<br />
zugeordnet. Diese Zuordnung wurde in Abschnitt 2.3.4 bereits für einatomige Gase<br />
vorgenommen, und zwar für die Bewegungsmöglichkeit einer Translation. Für Moleküle<br />
(aufgebaut aus mehreren Atomen) sind die Bewegungsmöglichkeiten der Rotation<br />
und Oszillation ebenfalls zu berücksichtigen (vgl. Abschnitt 5.4).<br />
<strong>Wärmelehre</strong> – Abschnitt 3<br />
- 45 -<br />
’1. Hauptsatz der <strong>Wärmelehre</strong>’















![[1.5pt] Wellenlehre[8.5pt] Zusammenfassung - gilligan-online](https://img.yumpu.com/21507627/1/184x260/15pt-wellenlehre85pt-zusammenfassung-gilligan-online.jpg?quality=85)