Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
3.2 Wärmekapazitäten<br />
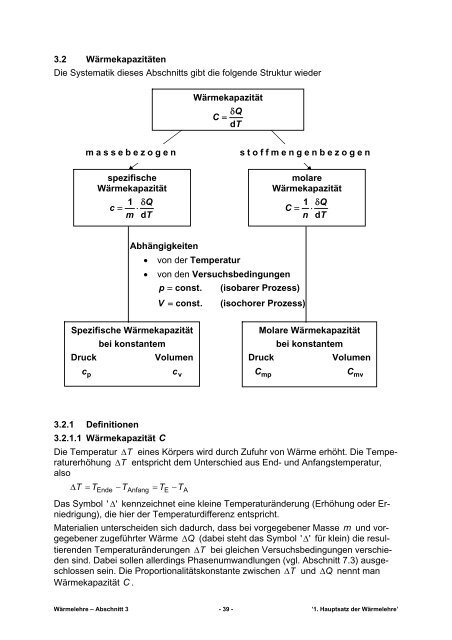
Die Systematik dieses Abschnitts gibt die folgende Struktur wieder<br />
Wärmekapazität<br />
δQ<br />
C = d T<br />
massebezogen<br />
spezifische<br />
Wärmekapazität<br />
1 δQ<br />
c = ⋅<br />
m dT<br />
stoffmengenbezogen<br />
molare<br />
Wärmekapazität<br />
1 δQ<br />
C = ⋅<br />
n dT<br />
Abhängigkeiten<br />
• von der Temperatur<br />
• von den Versuchsbedingungen<br />
p = const. (isobarer Prozess)<br />
V = const. (isochorer Prozess)<br />
Spezifische Wärmekapazität<br />
Druck<br />
c p<br />
bei konstantem<br />
Volumen<br />
c v<br />
Molare Wärmekapazität<br />
Druck<br />
bei konstantem<br />
Volumen<br />
C mp<br />
C mv<br />
3.2.1 Definitionen<br />
3.2.1.1 Wärmekapazität C<br />
Die Temperatur ΔT eines Körpers wird durch Zufuhr von Wärme erhöht. Die Temperaturerhöhung<br />
ΔT entspricht dem Unterschied aus End- und Anfangstemperatur,<br />
also<br />
Δ T = T<br />
Ende<br />
−T<br />
Anfang<br />
= T<br />
E<br />
−T<br />
A<br />
Das Symbol ' Δ' kennzeichnet eine kleine Temperaturänderung (Erhöhung oder Erniedrigung),<br />
die hier der Temperaturdifferenz entspricht.<br />
Materialien unterscheiden sich dadurch, dass bei vorgegebener Masse m und vorgegebener<br />
zugeführter Wärme Δ Q (dabei steht das Symbol 'Δ'<br />
für klein) die resultierenden<br />
Temperaturänderungen Δ T bei gleichen Versuchsbedingungen verschieden<br />
sind. Dabei sollen allerdings Phasenumwandlungen (vgl. Abschnitt 7.3) ausgeschlossen<br />
sein. Die Proportionalitätskonstante zwischen Δ T und ΔQ nennt man<br />
Wärmekapazität C .<br />
<strong>Wärmelehre</strong> – Abschnitt 3<br />
- 39 -<br />
’1. Hauptsatz der <strong>Wärmelehre</strong>’















![[1.5pt] Wellenlehre[8.5pt] Zusammenfassung - gilligan-online](https://img.yumpu.com/21507627/1/184x260/15pt-wellenlehre85pt-zusammenfassung-gilligan-online.jpg?quality=85)