Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
5 Molare Wärmekapazitäten eines idealen Gases<br />
Dieser Abschnitt zeigt eine Anwendung der kinetischen Gastheorie. Ausgehend von<br />
den in Kapitel 2 entwickelten Modellvorstellungen für ein ideales Gas sollen berechnet<br />
werden<br />
• die molare Wärmekapazität bei konstantem Volumen C mv ,<br />
• die molare Wärmekapazität bei konstantem Druck C mp .<br />
Daraus ergibt sich als weiteres Ergebnis der Isentropenexponent κ , der in Abschnitt<br />
4.4 als Quotient aus C und C definiert wurde.<br />
mp<br />
mv<br />
An dieser Anwendung der kinetischen Gastheorie soll beispielhaft die Vorgehensweise<br />
eines Physikers/einer Physikerin gezeigt werden<br />
• durchführen von Einzelexperimenten,<br />
• sammeln, sortieren und katalogisieren experimenteller Ergebnisse,<br />
• auffinden von Regeln und Gesetzmäßigkeiten,<br />
• ableiten von Gesetzmäßigkeiten aus einem Modell (Theorie),<br />
• vergleichen von theoretischen Vorhersagen und experimentellen Ergebnissen,<br />
• erweitern und Verfeine des Modells.<br />
5.1 Experimentelle Ergebnisse<br />
In Tabelle 5-01 sind, geordnet nach ein-, zwei- und mehratomigen Molekülen, die<br />
experimentell ermittelte Wärmekapazitäten C und C zusammengestellt.<br />
Einatomig<br />
Zweiatomig<br />
Cmp<br />
Gas −1<br />
−1<br />
Jmol K<br />
He<br />
Ar<br />
H 2<br />
O 2<br />
N 2<br />
Cl 2<br />
20,80<br />
20,80<br />
28,76<br />
29,43<br />
29,09<br />
34,70<br />
mv<br />
C<br />
Jmol<br />
mv<br />
−1<br />
K<br />
12,47<br />
12,47<br />
20,43<br />
21,06<br />
20,76<br />
25,74<br />
−1<br />
mp<br />
C<br />
mp mv<br />
−1<br />
−1<br />
Jmol<br />
−C<br />
K<br />
8,33<br />
8,33<br />
8,33<br />
8,37<br />
8,33<br />
8,96<br />
C<br />
κ =<br />
C<br />
mp<br />
mv<br />
1,67<br />
1,67<br />
1,41<br />
1,40<br />
1,40<br />
1,35<br />
Mehratomig<br />
CO 2<br />
SO 2<br />
C 2 O 2<br />
NH3<br />
36,96<br />
40,39<br />
51,70<br />
36,84<br />
28,46<br />
31,40<br />
43,12<br />
27,84<br />
8,50<br />
8,99<br />
8,58<br />
9,00<br />
1,30<br />
1,29<br />
1,20<br />
1,31<br />
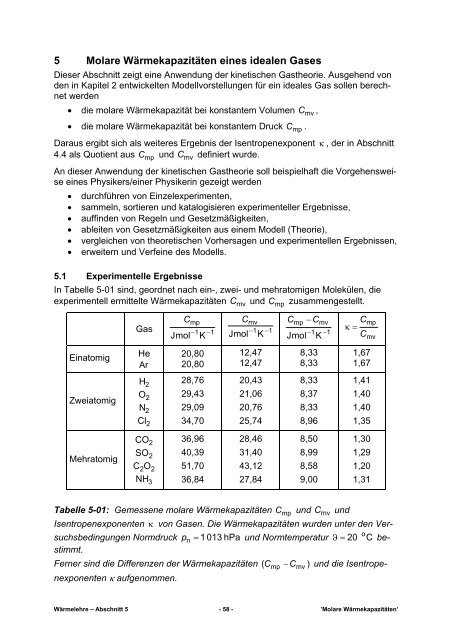
Tabelle 5-01: Gemessene molare Wärmekapazitäten C und C und<br />
Isentropenexponenten κ von Gasen. Die Wärmekapazitäten wurden unter den Versuchsbedingungen<br />
Normdruck<br />
stimmt.<br />
mp<br />
p n = 1 013 hPa und Normtemperatur ϑ = 20 o C be-<br />
Ferner sind die Differenzen der Wärmekapazitäten C − C ) und die Isentropenexponenten<br />
κ aufgenommen.<br />
( mp mv<br />
mv<br />
<strong>Wärmelehre</strong> – Abschnitt 5<br />
- 58 -<br />
’Molare Wärmekapazitäten’















![[1.5pt] Wellenlehre[8.5pt] Zusammenfassung - gilligan-online](https://img.yumpu.com/21507627/1/184x260/15pt-wellenlehre85pt-zusammenfassung-gilligan-online.jpg?quality=85)