Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Der Schmelzvorgang, also der Übergang vom festen in den flüssigen Zustand, wird<br />
anschaulich durch das Reißen der Federn bei zu großer thermischer Bewegung der<br />
Teilchen im Kristallgitter beschrieben.<br />
In Flüssigkeiten sind die Teilchen nicht mehr an eine bestimmte definierte Gleichgewichtslage<br />
gebunden; sie sind gegeneinander verschiebbar. Die Anziehungskräfte<br />
sind ungerichtet. Die daraus resultierende Wimmelbewegung der Teilchen in der<br />
Flüssigkeit kann indirekt sichtbar gemacht werden (BROWNsche Molekularbewegung).<br />
Flüssigkeiten sind nicht formbeständig. Die Dichten von Flüssigkeiten liegen<br />
3 −3<br />
bei etwa ρ ≈ 10 kg m .<br />
Der Übergang vom flüssigen in den gasförmigen Zustand heißt Verdampfung.<br />
Bei Gasen ist der Abstand zwischen den Teilchen so groß, dass die ungerichtete<br />
Wechselwirkung zwischen den Teilchen im Vergleich zu Flüssigkeiten sehr klein<br />
wird. Zusammenstöße zwischen den einzelnen Gasteilchen führen zur Ablenkung<br />
aus der ursprünglichen Flugrichtung. Für ein einzelnes Teilchen ergibt sich so eine<br />
völlig regellose Zickzackbahn.<br />
Gase haben keine Form; sie füllen nach einiger Zeit jeden ihnen zur Verfügung gestellten<br />
Raum aus. Die Dichte von Gasen ist stark abhängig von der Temperatur und<br />
dem Druck. Bei Normbedingungen, also bei ϑn = 0 o C und p n = 1 013 hPa , liegen<br />
−3<br />
die Dichten von Gasen bei etwa ρ ≈ 1kgm .<br />
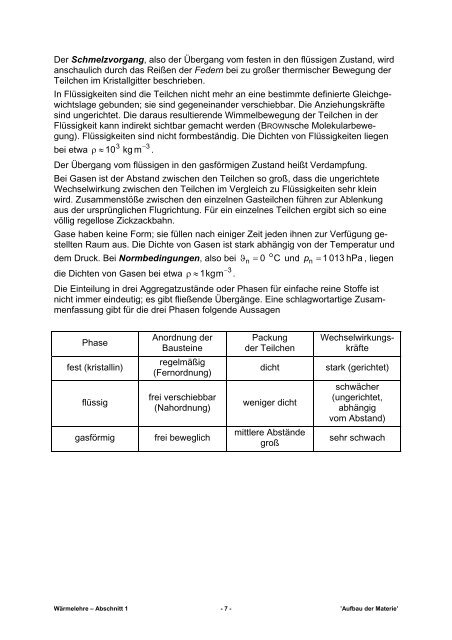
Die Einteilung in drei Aggregatzustände oder Phasen für einfache reine Stoffe ist<br />
nicht immer eindeutig; es gibt fließende Übergänge. Eine schlagwortartige Zusammenfassung<br />
gibt für die drei Phasen folgende Aussagen<br />
Phase<br />
fest (kristallin)<br />
flüssig<br />
gasförmig<br />
Anordnung der<br />
Bausteine<br />
regelmäßig<br />
(Fernordnung)<br />
frei verschiebbar<br />
(Nahordnung)<br />
frei beweglich<br />
Packung<br />
der Teilchen<br />
dicht<br />
weniger dicht<br />
mittlere Abstände<br />
groß<br />
Wechselwirkungskräfte<br />
stark (gerichtet)<br />
schwächer<br />
(ungerichtet,<br />
abhängig<br />
vom Abstand)<br />
sehr schwach<br />
<strong>Wärmelehre</strong> – Abschnitt 1<br />
- 7 -<br />
’Aufbau der Materie’















![[1.5pt] Wellenlehre[8.5pt] Zusammenfassung - gilligan-online](https://img.yumpu.com/21507627/1/184x260/15pt-wellenlehre85pt-zusammenfassung-gilligan-online.jpg?quality=85)