Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Es gibt keine experimentelle Beobachtung, die dieser Aussage widerspricht. Auch<br />
sämtliche Folgerungen, die aus dieser Aussage gezogen werden, stehen wieder mit<br />
der experimentellen Beobachtung in Einklang.<br />
Die Innere Energie U , also der Energieinhalt eines geschlossenen Systems, kann<br />
durch Energieübertragung, also Austausch von Arbeit und Wärme über die Systemgrenzen,<br />
geändert werden, d. h. durch<br />
• Wärmezufuhr,<br />
• Wärmeabgabe,<br />
• von außen am System verrichtete Arbeit,<br />
• vom System nach außen abgegebene Arbeit.<br />
Vorzeichenvereinbarung<br />
Die Vorzeichen von umgesetzten Wärmen und Arbeiten wurden folgendermaßen<br />
festgelegt (vgl. Abschnitte 3.1.3 und 3.1.4)<br />
• einem System zugeführte Wärme und Arbeit zählen positiv,<br />
• vom System verrichtete Arbeit und abgegebene Wärme zählen negativ.<br />
Zustands<br />
variable y<br />
(Beispiel<br />
Druck p )<br />
'Weg 2'<br />
'E'<br />
'A'<br />
'Weg 1'<br />
Zustandsvariable x<br />
(Beispiel Volumen V )<br />
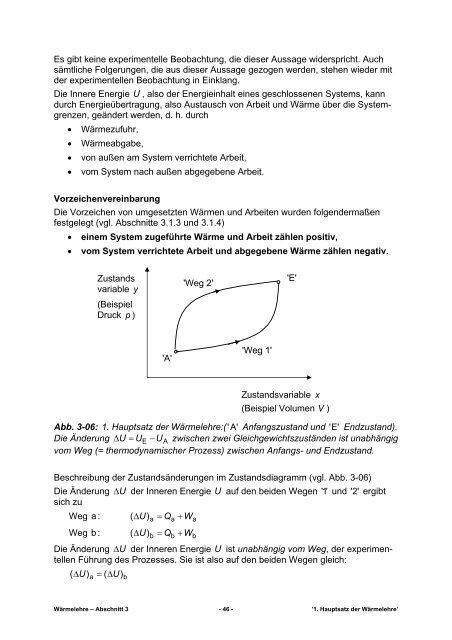
Abb. 3-06: 1. Hauptsatz der <strong>Wärmelehre</strong>:( ' A' Anfangszustand und ' E' Endzustand).<br />
Die Änderung ΔU<br />
= U E −U<br />
A zwischen zwei Gleichgewichtszuständen ist unabhängig<br />
vom Weg (= thermodynamischer Prozess) zwischen Anfangs- und Endzustand.<br />
Beschreibung der Zustandsänderungen im Zustandsdiagramm (vgl. Abb. 3-06)<br />
Die Änderung Δ U der Inneren Energie U auf den beiden Wegen ' 1'<br />
und '2'<br />
ergibt<br />
sich zu<br />
Weg a : ( Δ U = Q + W<br />
Weg b :<br />
) a<br />
) b<br />
a<br />
( Δ U = Q + W<br />
b<br />
a<br />
b<br />
Die Änderung ΔU der Inneren Energie U ist unabhängig vom Weg, der experimentellen<br />
Führung des Prozesses. Sie ist also auf den beiden Wegen gleich:<br />
( ΔU)<br />
= ( ΔU<br />
a ) b<br />
<strong>Wärmelehre</strong> – Abschnitt 3<br />
- 46 -<br />
’1. Hauptsatz der <strong>Wärmelehre</strong>’















![[1.5pt] Wellenlehre[8.5pt] Zusammenfassung - gilligan-online](https://img.yumpu.com/21507627/1/184x260/15pt-wellenlehre85pt-zusammenfassung-gilligan-online.jpg?quality=85)