Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Wärmelehre - gilligan-online
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
7.2 Isothermen realer Gase<br />
7.2.1 Experimentell ermittelte Isothermen<br />
Die Isothermen eines idealen Gases stellen im p,V -Diagramm Hyperbeln dar (vgl.<br />
Abschnitt 4.3), dies lässt sich aus der allgemeinen Zustandsgleichung ableiten. Reale<br />
Gase folgen der Gasgleichung nur bei geringen Drucken und hohen Temperaturen,<br />
oder anders ausgedrückt, für den Grenzfall ρ → 0 . Bei hohen Dichten treten beträchtliche<br />
Abweichungen vom idealen Verhalten auf. Dies ist für Kohlenstoffdioxid in<br />
Abb. 7-02 und Abb. 7-03 dargestellt.<br />
10 6 pPa<br />
10<br />
9<br />
8<br />
7<br />
6<br />
5<br />
Kohlenstoffdioxid ( CO 2 )<br />
n = 1 mol<br />
T = 273,15 K<br />
errechnete Isotherme<br />
ideales Gas: pV = nR<br />
m<br />
T<br />
4<br />
3<br />
gemessene Isotherme<br />
2<br />
1<br />
0<br />
0<br />
100<br />
200 300<br />
400<br />
500<br />
cm<br />
V<br />
mol<br />
3<br />
mol<br />
−1<br />
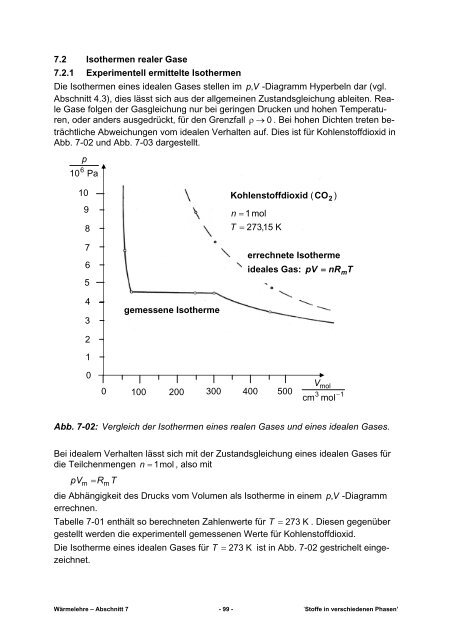
Abb. 7-02: Vergleich der Isothermen eines realen Gases und eines idealen Gases.<br />
Bei idealem Verhalten lässt sich mit der Zustandsgleichung eines idealen Gases für<br />
die Teilchenmengen n = 1mol , also mit<br />
pV<br />
m =<br />
R<br />
m<br />
T<br />
die Abhängigkeit des Drucks vom Volumen als Isotherme in einem p,V -Diagramm<br />
errechnen.<br />
Tabelle 7-01 enthält so berechneten Zahlenwerte für T = 273 K . Diesen gegenüber<br />
gestellt werden die experimentell gemessenen Werte für Kohlenstoffdioxid.<br />
Die Isotherme eines idealen Gases für T = 273 K ist in Abb. 7-02 gestrichelt eingezeichnet.<br />
<strong>Wärmelehre</strong> – Abschnitt 7<br />
- 99 -<br />
’Stoffe in verschiedenen Phasen’















![[1.5pt] Wellenlehre[8.5pt] Zusammenfassung - gilligan-online](https://img.yumpu.com/21507627/1/184x260/15pt-wellenlehre85pt-zusammenfassung-gilligan-online.jpg?quality=85)