- Page 1 and 2:
Sudaryatno Sudirham ing Utari Menge
- Page 3 and 4:
Hak cipta pada penulis, 2010 SUDIRH
- Page 5 and 6:
iv Distribusi Fermi-Dirac. Kondukti
- Page 7 and 8:
A. Schopenhauer, 1788 - 1860 Dari M
- Page 9 and 10:
Gerakan benda dapat pula dinyatakan
- Page 11 and 12:
1eV 4 = 1, 6019 × 10 = 1, 6019 ×
- Page 13 and 14:
melalui radiasi. Dua benda yang ber
- Page 15 and 16:
f, dan untuk setiap temperatur T, d
- Page 17 and 18:
sama dengan frekuensinya kali suatu
- Page 19 and 20:
Jika Eke adalah energi kinetik maks
- Page 21 and 22:
Mengenai energi potensialnya, kita
- Page 23 and 24:
karena itu kita menggunakan momentu
- Page 25 and 26:
atau 18 hf = E2 − E1 = Ek1 − Ek
- Page 27 and 28:
Heisenberg: Prinsip Ketidak-Pastian
- Page 29 and 30:
Jika θ merupakan fungsi x, θ = kx
- Page 31 and 32:
Dengan demikian maka persamaan gelo
- Page 33 and 34:
2.3. Panjang Gelombang de Broglie,
- Page 35 and 36:
28 penembak elektron berkas elektro
- Page 37 and 38:
30 • Bahwa elektron dapat dipanda
- Page 39 and 40:
dengan p dan x adalah peubah-peubah
- Page 41 and 42:
34 ∂ ∂ h u = j( hω0 ) u = jEu
- Page 43 and 44:
36 1 ∂ T( t) − jh = a = konstan
- Page 45 and 46:
sebagai fungsi waktu karena posisi
- Page 47 and 48:
40 2mE 2mE s = ± j = ± j α, deng
- Page 49 and 50:
pendekatan Bohr yang harus membuat
- Page 51 and 52:
Karena V = 0, persamaan Schrödinge
- Page 53 and 54:
46 E1 Kotak Potensial Kotak Potensi
- Page 55 and 56:
Fungsi gelombang dinyatakan dalam r
- Page 57 and 58:
2 sr adalah R 1 = A1e dengan = −
- Page 59 and 60:
nol. Dalam tinjauan tiga dimensi, p
- Page 61 and 62:
Dalam mekanika klasik, vektor momen
- Page 63 and 64:
56 1 jmlϕ Φ( ϕ) = e dengan m l =
- Page 65 and 66:
sampai l = (n - 1). Status momentum
- Page 67 and 68:
60 - dari status 2p ke 1s, dari 3s
- Page 69 and 70:
62 2 2 2 Ze Ze e V ( r) = − − +
- Page 71 and 72:
Orbital 1s memiliki simetri bola, y
- Page 73 and 74:
Atom F (fluor) memiliki 9 elektron.
- Page 75 and 76:
68 Y: 1s 2 2s 2 2p 6 3s 2 3p 6 3d 2
- Page 77 and 78:
70 Perhatikan bahwa ada dua unsur y
- Page 79 and 80:
5.5. Ionisasi dan Energi Ionisasi A
- Page 81 and 82:
Penambahan elektron 2s dari helium
- Page 83 and 84:
5.6. Afinitas Elektron Kalau energi
- Page 85 and 86:
Hal ini terjadi karena jumlah proto
- Page 87 and 88:
54 Xe [Kr] 4d 10 5s 2 5p 6 53 I [Kr
- Page 89 and 90:
82 elektron. Unsur nomer 21 (Sc) sa
- Page 91 and 92:
Perubahan energi potensial terhadap
- Page 93 and 94:
elektron dan menjadi ion Li + . Li
- Page 95 and 96:
tersebut memiliki spin yang berlawa
- Page 97 and 98:
Ikatan Hidrogen. Ikatan hidrogen te
- Page 99 and 100:
Kita telah melihat di bab sebelumny
- Page 101 and 102:
dengan XA dan XB masing-masing adal
- Page 103 and 104:
Bentuk hexagonal pada HCP maupun be
- Page 105 and 106:
dipandang dari atas) adalah seperti
- Page 107 and 108:
Di antara bola-bola yang tersusun r
- Page 109 and 110:
102 Tabel-6.4. Bilangan Koordinasi
- Page 111 and 112:
atom-atom dengan ikatan tak-berarah
- Page 113 and 114:
106 H H | | C = C | | H H ethylene
- Page 115 and 116:
kelompok atom yang menempati tiap-t
- Page 117 and 118:
delapan elektron di kulit terluarny
- Page 119 and 120:
7.1.4. Kristal Ionik Walau sangat j
- Page 121 and 122:
114 Selain ketidak-sempurnaan terse
- Page 123 and 124:
antaian ini cukup fleksible sehingg
- Page 125 and 126:
c) rantaian panjang yang merupakan
- Page 127 and 128:
(d) salah satu macam polimer menjad
- Page 129 and 130:
Dalam satu unit kristal jarak antar
- Page 131 and 132:
8.1. Teori Pita Energi Dalam pembah
- Page 133 and 134:
8.1.1. Pita Energi Pada Material Ko
- Page 135 and 136:
Pada 0 o K elektron terdistribusi d
- Page 137 and 138:
130 E E E g Semikonduktor intrinsik
- Page 139 and 140:
dengan i = x, y, z . Tanda ± pada
- Page 141 and 142:
Pengisian Status Pada 0 o K. Pada p
- Page 143 and 144:
Jadi elektron dalam padatan yang be
- Page 145 and 146:
menambahkan celah energi seperti di
- Page 147 and 148:
Pada kasus dua dimensi kita melihat
- Page 149 and 150:
energi terhadap bilangan gelombang,
- Page 151 and 152:
tidak menimbulkan arus listrik. Jik
- Page 153 and 154:
9.2. Pendekatan Statistik Pada temp
- Page 155 and 156:
148 yang sudah ada. Dengan asumsi i
- Page 157 and 158:
150 −βEi ni = gie Z (9.23) Inil
- Page 159 and 160:
Oleh karena itu persamaan (9.29) in
- Page 161 and 162:
9.4. Konduktivitas dan Resistivitas
- Page 163 and 164:
Tabel-9.2. Resistivitas (ρe) unsur
- Page 165 and 166:
total filamen adalah L sama dengan
- Page 167 and 168:
erjarak d, maka kapasitansi pelat p
- Page 169 and 170:
162 (a) (b) Gb.10.1. Diagram fasor
- Page 171 and 172:
164 Tabel-10.3. Kekuatan Dielektrik
- Page 173 and 174:
166 + + − + − − − − + −
- Page 175 and 176:
10.6. Arus Polarisasi Dan Arus Depo
- Page 177 and 178:
170 A σ − − − − − −
- Page 179 and 180:
Karena adalah jumlah molekul per s
- Page 181 and 182:
molekul dengan arah medan. Oleh kar
- Page 183 and 184: 176 dE C v = (11.1) dT Sudaryatno S
- Page 185 and 186: Angka inilah yang diperoleh oleh Du
- Page 187 and 188: 180 2 ⎛ ⎞ hfE / kBT dE hf = = 3
- Page 189 and 190: Phonon. Dalam analisisnya, Debye me
- Page 191 and 192: Faktor-Faktor Lain Yang Turut Berpe
- Page 193 and 194: Pada temperatur kamar, metal memili
- Page 195 and 196: 188 σT σe = LoT Sudaryatno S & Ni
- Page 197 and 198: 11.6. Ringkasan Dua bentuk utama en
- Page 199 and 200: 192 c). Jika bidang batas memberika
- Page 201 and 202: diberi tanda negatif jika ia keluar
- Page 203 and 204: mengatakan bahwa sistem memiliki en
- Page 205 and 206: 198 q reaksi = −qcampuran reagen
- Page 207 and 208: 200 dq < dqrev (12.10) Sementara it
- Page 209 and 210: eagen menyebar ke sejumlah (relatif
- Page 211 and 212: 12.6. Energi Bebas (free energies)
- Page 213 and 214: 206 dG = dq − dq P, T rev Sudarya
- Page 215 and 216: keseimbangan thermodinamik bisa mer
- Page 217 and 218: Jika keadaan ideal tidak kita perti
- Page 219 and 220: Dalam kasus yang tergambarkan pada
- Page 221 and 222: hanya memperhatikan temperatur dan
- Page 223 and 224: yaitu C. Sementara itu titik tripel
- Page 225 and 226: Entropi di suatu temperatur dihitun
- Page 227 and 228: Tinjau larutan padat dengan komposi
- Page 229 and 230: 222 L + α ↔ β (13.4) Perbedaan
- Page 231 and 232: Kerja yang diperlukan untuk memperb
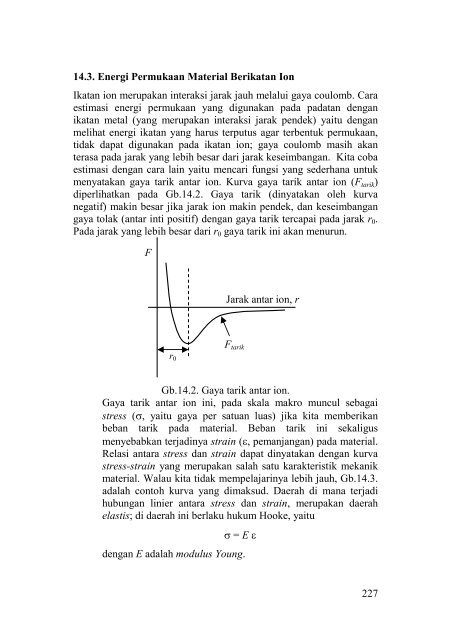
- Page 233: Demikian pula halnya dengan energi
- Page 237 and 238: Modulus Young dapat ditentukan, jar
- Page 239 and 240: ocor, memicu partial-discharge, yan
- Page 241 and 242: 234 xa ∆x x Gb.15.1. Difusi dalam
- Page 243 and 244: maka persamaan ini mirip dengan dis
- Page 245 and 246: Jadi jika Qvol adalah energi aktiva
- Page 247 and 248: sempurnaan Schottky berupa pasangan
- Page 249 and 250: 242 Tabel-16.1. Energi Bebas Pemben
- Page 251 and 252: 244 metal daerah terjadinya oksidas
- Page 253 and 254: konstan. Lapisan oksida ini nonprot
- Page 255 and 256: Perhatikan reaksi berikut (lihat Gb
- Page 257 and 258: yang tercelup dalam elektrolit deng
- Page 259 and 260: konsentrasi stress akan menjadi ano
- Page 261 and 262: 12. Jere H. Brophy, Robert M. Rose,
- Page 263 and 264: ionisasi 72 irreversible 198, 199 i
- Page 265: 258 Biodata Penulis Nama: Sudaryatn