- 60 - Die Essigsäureproduktion zeigte nur geringgradige Erhöhungen bis zu 8 % zwischen Tag 10 und 19 (s. Tab. 9.144). Die verlängerte Zulage von Clostridien beeinflusste den Verlauf der Graphen aller oben aufgeführten Parameter nicht. Bei einem Vergleich der Essigsäureproduktion durch die Silagen (LUMPP 2011) und einer Kombination der Silagen mit Clostridien zeigte sich bei allen Zulagen eine gleichgerichtete Verringerung bis zu -13,4 % (vergl. Tab. 4.7). Tab. 4.7: Prozentualer Unterschied der Essigsäureproduktion zwischen Silagezulage (LUMPP 2011) und der Kombination aus Silage- und Clostridienzulage ∆ Tag 10-14 (%) K-01 S-11 S-05 ∆ Tag 15-18 (%) ∆ Tag 10-14 (%) ∆ Tag 15-18 (%) ∆ Tag 10-14 (%) ∆ Tag 15-18 (%) C. botulinum, 1 mL -13,4 -4,93 -5,08 -6,96 -5,76 -7,23 C. botulinum, 2 mL -9,30 -8,94 -11,3 -6,56 -5,31 -9,53 C. perfringens, 1 mL -8,11 -7,53 -8,73 -7,74 -5,78 -9,30 C. perfringens, 2 mL -5,14 0,04 -5,55 -9,44 -0,20 -15,0 C. botulinum, 1 mL, 9 Tage -6,10 -7,52 -7,61 -3,82 C. botulinum, 2 mL, 9 Tage -7,18 -6,19 Die n-Buttersäureproduktion in Fermentern, in denen K-01 mit C. botulinum kombiniert wurde, lag um ca. 4 % niedriger als wenn lediglich K-01 zugelegt wurde (LUMPP 2011). Eine Verdopplung der Clostridienzulage zeigte keinen Einfluss. Ersetzte man die Kontrollsilage durch die beiden Schadgrassilagen, lag die n-Buttersäureproduktion zwischen Tag 10 und 14 bis zu 9,42 % höher, wenn Silage und Clostridien kombiniert wurden. Eine Zulage von C. perfringens verursachte eine höhere n-Buttersäureproduktion bei Kombinationszulage als bei reiner Silagezulage (s. Tab. 4.8). Hier verstärkte sich die Produktion auch, wenn die Clostridiengabe verdoppelt wurde (s. Tabb. 9.145-9.154).
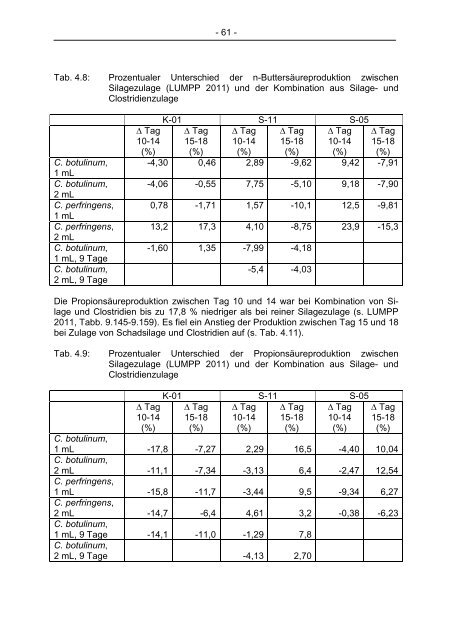
- 61 - Tab. 4.8: Prozentualer Unterschied der n-Buttersäureproduktion zwischen Silagezulage (LUMPP 2011) und der Kombination aus Silage- und Clostridienzulage C. botulinum, 1 mL C. botulinum, 2 mL C. perfringens, 1 mL C. perfringens, 2 mL C. botulinum, 1 mL, 9 Tage C. botulinum, 2 mL, 9 Tage ∆ Tag 10-14 (%) K-01 S-11 S-05 ∆ Tag 15-18 (%) ∆ Tag 10-14 (%) ∆ Tag 15-18 (%) ∆ Tag 10-14 (%) ∆ Tag 15-18 (%) -4,30 0,46 2,89 -9,62 9,42 -7,91 -4,06 -0,55 7,75 -5,10 9,18 -7,90 0,78 -1,71 1,57 -10,1 12,5 -9,81 13,2 17,3 4,10 -8,75 23,9 -15,3 -1,60 1,35 -7,99 -4,18 -5,4 -4,03 Die Propionsäureproduktion zwischen Tag 10 und 14 war bei Kombination von Silage und Clostridien bis zu 17,8 % niedriger als bei reiner Silagezulage (s. LUMPP 2011, Tabb. 9.145-9.159). Es fiel ein Anstieg der Produktion zwischen Tag 15 und 18 bei Zulage von Schadsilage und Clostridien auf (s. Tab. 4.11). Tab. 4.9: Prozentualer Unterschied der Propionsäureproduktion zwischen Silagezulage (LUMPP 2011) und der Kombination aus Silage- und Clostridienzulage ∆ Tag 10-14 (%) K-01 S-11 S-05 ∆ Tag 15-18 (%) ∆ Tag 10-14 (%) ∆ Tag 15-18 (%) ∆ Tag 10-14 (%) ∆ Tag 15-18 (%) C. botulinum, 1 mL -17,8 -7,27 2,29 16,5 -4,40 10,04 C. botulinum, 2 mL -11,1 -7,34 -3,13 6,4 -2,47 12,54 C. perfringens, 1 mL -15,8 -11,7 -3,44 9,5 -9,34 6,27 C. perfringens, 2 mL -14,7 -6,4 4,61 3,2 -0,38 -6,23 C. botulinum, 1 mL, 9 Tage -14,1 -11,0 -1,29 7,8 C. botulinum, 2 mL, 9 Tage -4,13 2,70
- Seite 1 und 2:
Tierärztliche Hochschule Hannover
- Seite 3:
„Was wir wissen, ist ein Tropfen,
- Seite 6 und 7:
II 3.5 Literaturangabe zur Analyse
- Seite 8 und 9:
Abkürzungsverzeichnis AS Aminosäu
- Seite 11 und 12:
1 Einleitung - 1 - In den letzten z
- Seite 13 und 14:
2.2 Protozoen des Pansens - 3 - Ein
- Seite 15 und 16:
Fortsetzung Tab. 2.2 Epidinium caud
- Seite 17 und 18:
- 7 - Überleben von K. aerogenes m
- Seite 19 und 20: - 9 - 6 % solche wie Enterococcus f
- Seite 21 und 22: - 11 - 2.4.1.1 Eintragsquellen von
- Seite 23 und 24: - 13 - gegen B-M nur minimal toxisc
- Seite 25 und 26: - 15 - Tab. 2.6: Unterschiede der r
- Seite 27 und 28: - 17 - REINSTEIN et al. 2007; CALLA
- Seite 29 und 30: - 19 - der Überlebensfähigkeit da
- Seite 31 und 32: - 21 - zoen überleben (KING et al.
- Seite 33 und 34: - 23 - Hemmung der Salmonellen. In
- Seite 35 und 36: 3 Material und Methoden - 25 - Reag
- Seite 37 und 38: 3.2.2 Herkunft der Silagen - 27 - Z
- Seite 39 und 40: - 29 - Tab. 3.2: Während der acht
- Seite 41 und 42: - 31 - 3.4.1.1 Die Clostridienzulag
- Seite 43 und 44: - 33 - Tab. 3.5: Kriterien zur Beur
- Seite 45 und 46: - 35 - Fortsetzung Tab. 3.6 Janusgr
- Seite 47 und 48: - 37 - Tab. 3.8: Ergebnisse der Vor
- Seite 49 und 50: - 39 - Fortsetzung Tab. 3.8 Methylg
- Seite 51 und 52: - 41 - Fortsetzung Tab. 3.9 Methylg
- Seite 53 und 54: Fortsetzung Tab. 3.12 Methylenblau
- Seite 55 und 56: 100% 80% 60% 40% 20% 0% ohne Zusatz
- Seite 57 und 58: - 47 - 3.8.2 Färbemethoden zur Dif
- Seite 59 und 60: 4 Ergebnisse - 49 - In der Ergebnis
- Seite 61 und 62: mmol/L 27 18 9 0 - 51 - 0 2 4 6 8 1
- Seite 63 und 64: - 53 - bzw. 45,4 % über denen von
- Seite 65 und 66: % 140 70 0 % 140 70 0 - 55 - Tag 10
- Seite 67 und 68: - 57 - Eine verlängerte neuntägig
- Seite 69: - 59 - Fortsetzung Tab. 4.6 C. botu
- Seite 73 und 74: Tab. 4.10: Prozentuale Veränderung
- Seite 75 und 76: Fortsetzung Tab. 4.11 Zulage n-Vale
- Seite 77 und 78: Hefefüllung - 67 - Abb. 4.7: Proze
- Seite 79 und 80: - 69 - Auch bei Zulage von 2 mL C.
- Seite 81 und 82: - 71 - 4.5 Ergebnisse der PCR-Unter
- Seite 83 und 84: 5 Diskussion 5.1 Intention der Arbe
- Seite 85 und 86: - 75 - Versuchen nur eine Protease,
- Seite 87 und 88: 5.5 Statistik - 77 - Die statistisc
- Seite 89 und 90: - 79 - Auch bei Zulage von C. botul
- Seite 91 und 92: % 70 30 -10 Schadsilagenzulage- mik
- Seite 93 und 94: % 70 30 -10 Schadsilagenzulage- mik
- Seite 95 und 96: - 85 - 5.6.2.3 Bakterieller Protein
- Seite 97 und 98: - 87 - Aminosäuren aufwies, gefolg
- Seite 99 und 100: - 89 - 5.6.4 Auswirkungen auf die P
- Seite 101 und 102: - 91 - Durch die enormen Kosten der
- Seite 103 und 104: - 93 - Irle, Annika (2011): Untersu
- Seite 105 und 106: - 95 - Irle, Annika (2011): In vitr
- Seite 107 und 108: 8 Literaturverzeichnis - 97 - ABBIT
- Seite 109 und 110: - 99 - BERGERE, J. L., M. ROUSSEAU
- Seite 111 und 112: - 101 - CALLAWAY, T. R., R. O. ELDE
- Seite 113 und 114: - 103 - DARGATZ, D. A., S. J. WELLS
- Seite 115 und 116: - 105 - FIELDS, B. S, E. B. SHOTTS,
- Seite 117 und 118: - 107 - GOEPFERT, J. M., u. R. HICK
- Seite 119 und 120: - 109 - HENTGES, D. J. (1967): Infl
- Seite 121 und 122:
- 111 - KALZENDORF, C. (2004): Stra
- Seite 123 und 124:
- 113 - LYTTLETON, J. W. (1973): Pr
- Seite 125 und 126:
- 115 - MITSCHERLICH, E., S. GÜRT
- Seite 127 und 128:
- 117 - POPOFF, M. R., u. J. LECOAN
- Seite 129 und 130:
- 119 - SCHIMMEL, D. (2002): Ergebn
- Seite 131 und 132:
- 121 - STOUTHAMER, A. H. (1979): T
- Seite 133 und 134:
- 123 - WALLIS, O. C., u. G. S. COL
- Seite 135 und 136:
9 Anhang - 125 - 9.1 Nährstoffanal
- Seite 137 und 138:
- 127 - Fortsetzung Tab. 9.6 Küvet
- Seite 139 und 140:
- 129 - 9.5 Methodenbeschreibung de
- Seite 141 und 142:
Zusammensetzung des Clostridien-Med
- Seite 143 und 144:
- 133 - Cl. botulinum-Diagnostik mi
- Seite 145 und 146:
Bot A-F/R FW: tgc agg aca aat gca a
- Seite 147 und 148:
Für 16S, DNAX 2. PCR, cpa, BoNT D
- Seite 149 und 150:
Tab. 9.9: pH-Werte in der Fermenter
- Seite 151 und 152:
Tab. 9.13: pH-Werte in der Fermente
- Seite 153 und 154:
Tab. 9.17: Ammoniakkonzentration (m
- Seite 155 und 156:
Tab. 9.21: Überstandsvolumen (mL)
- Seite 157 und 158:
Tab. 9.25: Gasproduktion (mL) währ
- Seite 159 und 160:
Tab. 9.29: Methankonzentration (Vol
- Seite 161 und 162:
Tab. 9.33: Methankonzentration (Vol
- Seite 163 und 164:
Tab. 9.37: Wasserstoffkonzentration
- Seite 165 und 166:
Tab. 9.41: Kohlendioxidkonzentratio
- Seite 167 und 168:
Tab. 9.45: Stickstoffkonzentration
- Seite 169 und 170:
Tab. 9.49: Sauerstoffkonzentration
- Seite 171 und 172:
Tab. 9.53: Sauerstoffkonzentration
- Seite 173 und 174:
Tab. 9.57: Proteingehalt (µg/mL RS
- Seite 175 und 176:
Tab. 9.61: Essigsäurekonzentration
- Seite 177 und 178:
Tab. 9.65: Essigsäureproduktion (m
- Seite 179 und 180:
Tab. 9.69: Propionsäurekonzentrati
- Seite 181 und 182:
Tab. 9.73: Propionsäurekonzentrati
- Seite 183 und 184:
Tab. 9.77: Propionsäureproduktion
- Seite 185 und 186:
Tab. 9.81: i-Buttersäurekonzentrat
- Seite 187 und 188:
Tab. 9.85: i-Buttersäureproduktion
- Seite 189 und 190:
Tab. 9.89: n-Buttersäurekonzentrat
- Seite 191 und 192:
Tab. 9.93: n-Buttersäurekonzentrat
- Seite 193 und 194:
Tab. 9.97: n-Buttersäureproduktion
- Seite 195 und 196:
Tab. 9.101: i-Valeriansäurekonzent
- Seite 197 und 198:
Tab. 9.105: i-Valeriansäureprodukt
- Seite 199 und 200:
Tab. 9.109: n-Valeriansäurekonzent
- Seite 201 und 202:
Tab. 9.113: n-Valeriansäurekonzent
- Seite 203 und 204:
Tab. 9.117: n-Valeriansäureprodukt
- Seite 205 und 206:
Tab. 9.121: Hexansäurekonzentratio
- Seite 207 und 208:
Tab. 9.125: Hexansäureproduktion (
- Seite 209 und 210:
Tab. 9.129: Summe aller flüchtigen
- Seite 211 und 212:
Tab. 9.133: Summe aller flüchtigen
- Seite 213 und 214:
Tab. 9.137: Produktion aller flüch
- Seite 215 und 216:
Tab. 9.140: Prozentualer Unterschie
- Seite 217 und 218:
Tab. 9.142: Prozentualer Unterschie
- Seite 219 und 220:
Tab. 9.144: Prozentualer Unterschie
- Seite 221 und 222:
Tab. 9.145: Vergleich der Silagezul
- Seite 223 und 224:
Tab. 9.147: Vergleich der Silagezul
- Seite 225 und 226:
Tab. 9.149: Vergleich der Silagezul
- Seite 227 und 228:
Tab. 9.151: Vergleich der Silagezul
- Seite 229 und 230:
Tab. 9.153: Vergleich der Silagezul
- Seite 231 und 232:
Tab. 9.155: Vergleich der Silagezul
- Seite 233 und 234:
Tab. 9.157: Vergleich der Silagezul
- Seite 235 und 236:
Tab. 9.159: Vergleich der Silagezul
- Seite 237 und 238:
Tab. 9.162: Prozentualer Unterschie
- Seite 239 und 240:
Tab. 9.165: Prozentuale Verteilung
- Seite 241 und 242:
Tab. 9.167: Prozentuale Verteilung









![Tmnsudation.] - TiHo Bibliothek elib](https://img.yumpu.com/23369022/1/174x260/tmnsudation-tiho-bibliothek-elib.jpg?quality=85)






