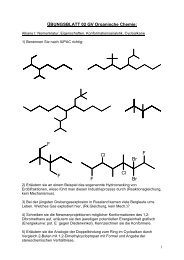
NIEMALS OHNE SCHUTZBRILLE IM LABOR !!!!! - oc1.uni-bayreuth.de
NIEMALS OHNE SCHUTZBRILLE IM LABOR !!!!! - oc1.uni-bayreuth.de
NIEMALS OHNE SCHUTZBRILLE IM LABOR !!!!! - oc1.uni-bayreuth.de
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
H 3 C<br />
O<br />
H3C S O<br />
O<br />
O<br />
O S O CH3+ Na �<br />
O<br />
CH CH 2 CH 3<br />
CH 3<br />
� ����<br />
�������� �����<br />
� ����� � ��� �<br />
����� �����<br />
� ������<br />
4.3 Herstellung sekundärer und tertiärer Alkylhalogeni<strong>de</strong>:<br />
Br<br />
CH 3<br />
�<br />
CH CH 2 CH 3<br />
Sekundäre und tertiäre Alkohole können nicht so einfach in entsprechen<strong>de</strong><br />
Alkylhalogeni<strong>de</strong> überführt wer<strong>de</strong>n wie primäre:<br />
Versucht man etwa mit 48 %iger Bromwasserstoffsäure (HBr) aus einem sekundären<br />
o<strong>de</strong>r tertiären Alkohol das Bromid herzustellen, so erhält man oft in überwiegen<strong>de</strong>r<br />
Menge Olefine. Grund für diese gegenüber primären Alkoholen an<strong>de</strong>rs verlaufen<strong>de</strong><br />
Reaktion ist <strong>de</strong>r Wechsel <strong>de</strong>s Reaktionmechanismus, wenn man von primären über<br />
sekundäre zu tertiären Alkoholen übergeht. Der gedrängte räumliche Bau verhin<strong>de</strong>rt<br />
<strong>de</strong>n Angriff <strong>de</strong>s Reagenz im Zuge einer SN2-Reaktion. An<strong>de</strong>rerseits wird durch<br />
Zunahme <strong>de</strong>s +I-Effektes vom primären zum tertiären C-Atom hin <strong>de</strong>r Bindungsbruch<br />
zur austreten<strong>de</strong>n Gruppe (-OH bzw. – �<br />
OH2) erleichtert:<br />
H 3C<br />
CH 2<br />
OH<br />
CH 3<br />
CH 3<br />
CH 3<br />
H3C CH OH H3C C OH<br />
CH 3<br />
Dies führt dazu, dass die Bindung zur austreten<strong>de</strong>n Gruppe schon vor <strong>de</strong>m Angriff von<br />
X �<br />
unter Bildung eines Carbenium-Ions gelöst wird (SN1-Mechanismus). Das gebil<strong>de</strong>te<br />
Carbenium-Ion wird mit steigen<strong>de</strong>m +I-Effekt stabilisiert.<br />
Während primäre Alkohole normalerweise bei Substitutionen nach <strong>de</strong>m SN2-<br />
Mechanismus reagieren, wer<strong>de</strong>n tertiäre Alkohole nach <strong>de</strong>m SN1-Mechanismus<br />
substituiert. Die Reaktion sekundärer Alkohole ist zumeist eine Mischung zwischen<br />
62