NIEMALS OHNE SCHUTZBRILLE IM LABOR !!!!! - oc1.uni-bayreuth.de
NIEMALS OHNE SCHUTZBRILLE IM LABOR !!!!! - oc1.uni-bayreuth.de
NIEMALS OHNE SCHUTZBRILLE IM LABOR !!!!! - oc1.uni-bayreuth.de
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
R<br />
R<br />
R<br />
C OH H3O �<br />
R<br />
R<br />
CH2 +<br />
- H2O �<br />
C CH 2<br />
R<br />
>+ �<br />
@<br />
; �<br />
R<br />
R<br />
C CH 2<br />
R<br />
R<br />
R<br />
R<br />
C<br />
X<br />
C CH 2<br />
R<br />
� - H2O OH2 CH R<br />
R<br />
R<br />
C CH 2<br />
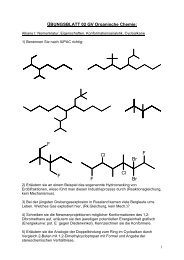
Da die SN1-Reaktion und damit die ungewünschte Olefinbildung (E1-Eliminierung)<br />
durch protische polare Lösungsmittel geför<strong>de</strong>rt wird (För<strong>de</strong>rung <strong>de</strong>r Solvatation von<br />
Kationen und Anionen, die Voraussetzung für die Bindungsspaltung ist), muß man zur<br />
Herbeiführung einer SN2-Reakzion ein aprotisches dipolares Lösungsmittel verwen<strong>de</strong>n.<br />
Diese för<strong>de</strong>rt zwar auch die Solvatation, da sie aber zum Anion keine<br />
Wasserstoffbrücke ausbil<strong>de</strong>n können, ist die primäre Abdissoziation von X �<br />
und damit auch die miteinan<strong>de</strong>r konkurrieren<strong>de</strong>n SN1- und E1-Reaktionen.<br />
R<br />
R<br />
�<br />
erschwert<br />
Da die sterisch weniger gespannten Olefine thermodynamisch stabiler, d.h. eine<br />
größere negative freie Bildungsenthalpie haben, wer<strong>de</strong>n sie bei höheren<br />
Temperaturen bevorzugt gebil<strong>de</strong>t. Der Grund dafür ist <strong>de</strong>r bei höheren<br />
Temperaturen größere Energieinhalt <strong>de</strong>r Ausgangsmoleküle.<br />
Will man sekundäre und tertiäre Alkohole in die Halogeni<strong>de</strong><br />
überführen, sollte man daher bei tiefen Temperaturen arbeiten.<br />
Damit allein kann die Ausbeutemin<strong>de</strong>rung zufolge Olefinbildung nur<br />
eingeschränkt, nicht aber vermie<strong>de</strong>n wer<strong>de</strong>n. Deshalb wählt man zur Herstellung<br />
sekundärer und tertiärer Alkylhalogeni<strong>de</strong> <strong>de</strong>n Umweg <strong>de</strong>r Umsetzung mit<br />
Phosphorhalogeni<strong>de</strong>n o<strong>de</strong>r Thionylchlorid.<br />
Br2 und I2 reagiert wie bereits früher ausgeführt, mit rotem Phosphor<br />
unter PX3 Bildung. Dieses Reagenz setzt sich mit Alkoholen zu einem<br />
64