Metallorganisch chemische ... - JUWEL - Forschungszentrum Jülich
Metallorganisch chemische ... - JUWEL - Forschungszentrum Jülich
Metallorganisch chemische ... - JUWEL - Forschungszentrum Jülich
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
12 2 Grundlagen<br />
Paradebeispiel für derartige hoch-ε Materialien ist die lückenlose Mischungsreihe SrTiO3-<br />
(Ba,Sr)TiO3-BaTiO3 die in der Perowskit Struktur (A 2+ B 4+ O3 2- ) kristallisiert. Die Bezeichnung<br />
Perowskit stammt von dem russischen Grafen Perovsky, der als erster auf die besonderen<br />
Eigenschaften von CaTiO3 aufmerksam wurde. Die kubische Einheitszelle ist in Abbildung<br />
2.1 dargestellt. Im Perowskitgitter ist das große A 2+ Kation zwölffach koordiniert. Das<br />
kleinere B 4+ Kation befindet sich in der Mitte eines Oktaeders aus O2-Anionen und liegt damit<br />
in sechsfacher Koordination vor.<br />
Obwohl die Strukturbezeichnung sich ursprünglich auf die kubische Struktur bezog werden<br />
heute auch verzerrte Strukturen mit zu den Perowskiten gerechnet. Die Verzerrung der Zellstruktur<br />
im Perowskit hängt stark mit dem Ionenradius der Kationen zusammen. Die obere<br />
Grenze für die A-Ionen ist gleich der Größe für die Sauerstoffatome mit einem Ionenradius<br />
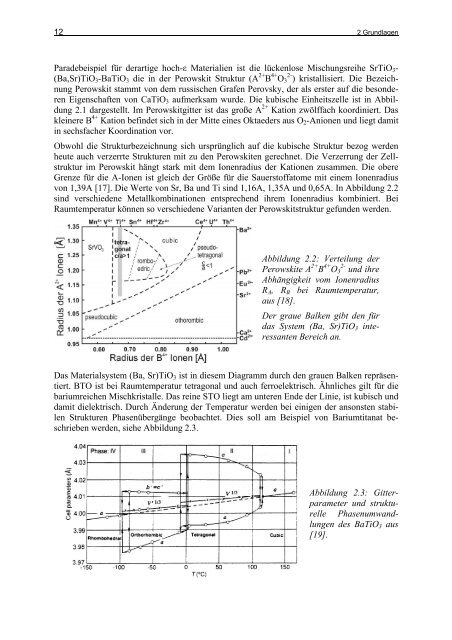
von 1,39A [17]. Die Werte von Sr, Ba und Ti sind 1,16A, 1,35A und 0,65A. In Abbildung 2.2<br />
sind verschiedene Metallkombinationen entsprechend ihrem Ionenradius kombiniert. Bei<br />
Raumtemperatur können so verschiedene Varianten der Perowskitstruktur gefunden werden.<br />
Abbildung 2.2: Verteilung der<br />
Perowskite A 2+ B 4+ O3 2- und ihre<br />
Abhängigkeit vom Ionenradius<br />
RA, RB bei Raumtemperatur,<br />
aus [18].<br />
Der graue Balken gibt den für<br />
das System (Ba, Sr)TiO3 interessanten<br />
Bereich an.<br />
Das Materialsystem (Ba, Sr)TiO3 ist in diesem Diagramm durch den grauen Balken repräsentiert.<br />
BTO ist bei Raumtemperatur tetragonal und auch ferroelektrisch. Ähnliches gilt für die<br />
bariumreichen Mischkristalle. Das reine STO liegt am unteren Ende der Linie, ist kubisch und<br />
damit dielektrisch. Durch Änderung der Temperatur werden bei einigen der ansonsten stabilen<br />
Strukturen Phasenübergänge beobachtet. Dies soll am Beispiel von Bariumtitanat beschrieben<br />
werden, siehe Abbildung 2.3.<br />
Abbildung 2.3: Gitterparameter<br />
und strukturellePhasenumwandlungen<br />
des BaTiO3 aus<br />
[19].