Untersuchung der Ursachen von Aromaveränderungen an einem ...
Untersuchung der Ursachen von Aromaveränderungen an einem ...
Untersuchung der Ursachen von Aromaveränderungen an einem ...
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Theoretischer Teil: Zum Phasenüberg<strong>an</strong>g flüssig - gasförmig<br />
Der Gesamtdampfdruck p <strong>der</strong> Mischung setzt sich nach dem DALTONschen<br />
Gesetz additiv aus den einzelnen Partialdrücken zusammen, so dass gilt:<br />
A<br />
B<br />
A<br />
*<br />
A<br />
B<br />
- 24 -<br />
*<br />
B<br />
*<br />
B<br />
p = p + p = x p + x p = p + ( p − p )x<br />
(Gl. 2)<br />
Aus <strong>der</strong> Gleichung ist ersichtlich, dass <strong>der</strong> Gesamtdampfdruck bei konst<strong>an</strong>ter<br />
Temperatur linear <strong>von</strong> <strong>der</strong> Zusammensetzung abhängt. Würde die Konzentration<br />
einer Subst<strong>an</strong>z in <strong>der</strong> flüssigen Phase steigen, würde sich ohne Berücksichtigung<br />
<strong>der</strong> verän<strong>der</strong>ten Matrixeinflüsse auch ihre Konzentration in <strong>der</strong><br />
Gasphase erhöhen. Analoges gilt für abnehmende Konzentrationen.<br />
Stehen flüssige und gasförmige Phase im Gleichgewicht, so muss ihre Zusammensetzung<br />
aber nicht notwendigerweise übereinstimmen. Es ist vielmehr<br />
zu erwarten, dass die Komponente mit <strong>der</strong> höheren Flüchtigkeit sich im<br />
Dampfraum relativ zur Komponente mit <strong>der</strong> geringeren Flüchtigkeit <strong>an</strong>reichert.<br />
Nach dem DALTONschen Gesetz lassen sich die Molenbrüche y für die Komponenten<br />
A und B in <strong>der</strong> Gasphase wie folgt definieren:<br />
pA yA = bzw.<br />
p<br />
*<br />
A<br />
p B<br />
*<br />
B<br />
A<br />
y B =<br />
(Gl. 3)<br />
p<br />
Setzt m<strong>an</strong> Gleichung 1 und 2 in Gleichung 3, lässt sich <strong>der</strong> Molenbruch <strong>der</strong><br />
Komponente A bzw. B unter Berücksichtigung ihrer Dampfdrücke in Abhängigkeit<br />
<strong>der</strong> Zusammensetzung <strong>der</strong> flüssigen Phase ableiten:<br />
y<br />
A<br />
=<br />
p<br />
*<br />
B<br />
x<br />
+ ( p<br />
A<br />
*<br />
A<br />
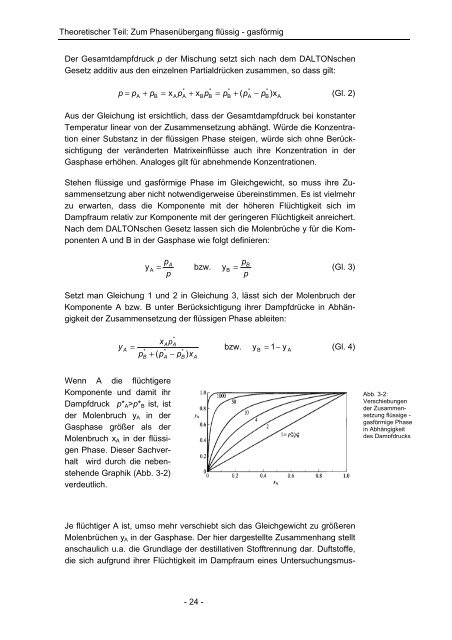
Wenn A die flüchtigere<br />
Komponente und damit ihr<br />
Dampfdruck p*A>p*B ist, ist<br />
<strong>der</strong> Molenbruch yA in <strong>der</strong><br />
Gasphase größer als <strong>der</strong><br />
Molenbruch xA in <strong>der</strong> flüssigen<br />
Phase. Dieser Sachverhalt<br />
wird durch die nebenstehende<br />
Graphik (Abb. 3-2)<br />
verdeutlich.<br />
p<br />
*<br />
A<br />
*<br />
B<br />
− p ) x<br />
A<br />
bzw. yB 1−<br />
y A<br />
= (Gl. 4)<br />
Je flüchtiger A ist, umso mehr verschiebt sich das Gleichgewicht zu größeren<br />
Molenbrüchen yA in <strong>der</strong> Gasphase. Der hier dargestellte Zusammenh<strong>an</strong>g stellt<br />
<strong>an</strong>schaulich u.a. die Grundlage <strong>der</strong> destillativen Stofftrennung dar. Duftstoffe,<br />
die sich aufgrund ihrer Flüchtigkeit im Dampfraum eines <strong>Untersuchung</strong>smus-<br />
Abb. 3-2:<br />
Verschiebungen<br />
<strong>der</strong> Zusammensetzung<br />
flüssige -<br />
gasförmige Phase<br />
in Abhängigkeit<br />
des Dampfdrucks