Immobilisierung
resolver
resolver
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
Ergebnisse und Diskussion<br />
400<br />
350<br />
300<br />
i [nA]<br />
250<br />
200<br />
150<br />
100<br />
∆<br />
50<br />
0<br />
0,0 0,2 0,4<br />
E [V vs Ag/AgCl]<br />
0,0 0,2 0,4<br />
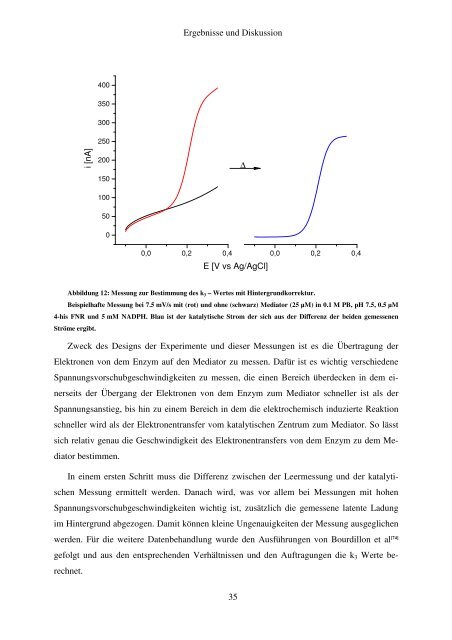
Abbildung 12: Messung zur Bestimmung des k 3 – Wertes mit Hintergrundkorrektur.<br />
Beispielhafte Messung bei 7.5 mV/s mit (rot) und ohne (schwarz) Mediator (25 µM) in 0.1 M PB, pH 7.5, 0.5 µM<br />
4-his FNR und 5 mM NADPH. Blau ist der katalytische Strom der sich aus der Differenz der beiden gemessenen<br />
Ströme ergibt.<br />
Zweck des Designs der Experimente und dieser Messungen ist es die Übertragung der<br />
Elektronen von dem Enzym auf den Mediator zu messen. Dafür ist es wichtig verschiedene<br />
Spannungsvorschubgeschwindigkeiten zu messen, die einen Bereich überdecken in dem einerseits<br />
der Übergang der Elektronen von dem Enzym zum Mediator schneller ist als der<br />
Spannungsanstieg, bis hin zu einem Bereich in dem die elektrochemisch induzierte Reaktion<br />
schneller wird als der Elektronentransfer vom katalytischen Zentrum zum Mediator. So lässt<br />
sich relativ genau die Geschwindigkeit des Elektronentransfers von dem Enzym zu dem Mediator<br />
bestimmen.<br />
In einem ersten Schritt muss die Differenz zwischen der Leermessung und der katalytischen<br />
Messung ermittelt werden. Danach wird, was vor allem bei Messungen mit hohen<br />
Spannungsvorschubgeschwindigkeiten wichtig ist, zusätzlich die gemessene latente Ladung<br />
im Hintergrund abgezogen. Damit können kleine Ungenauigkeiten der Messung ausgeglichen<br />
werden. Für die weitere Datenbehandlung wurde den Ausführungen von Bourdillon et al [74]<br />
gefolgt und aus den entsprechenden Verhältnissen und den Auftragungen die k 3 Werte berechnet.<br />
35