Immobilisierung
resolver
resolver
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Ergebnisse und Diskussion<br />
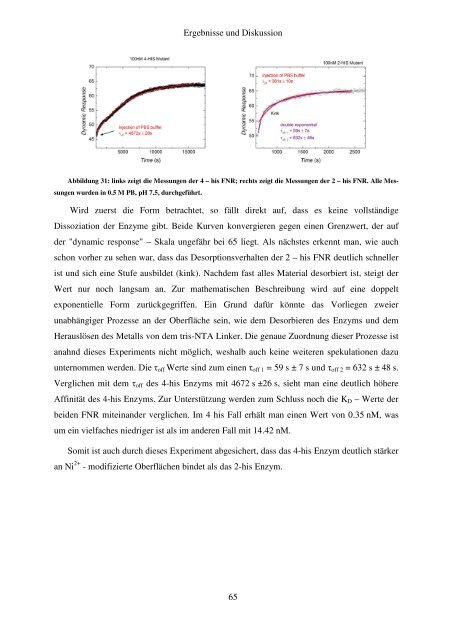
Abbildung 31: links zeigt die Messungen der 4 – his FNR; rechts zeigt die Messungen der 2 – his FNR. Alle Messungen<br />
wurden in 0.5 M PB, pH 7.5, durchgeführt.<br />
Wird zuerst die Form betrachtet, so fällt direkt auf, dass es keine vollständige<br />
Dissoziation der Enzyme gibt. Beide Kurven konvergieren gegen einen Grenzwert, der auf<br />
der "dynamic response" – Skala ungefähr bei 65 liegt. Als nächstes erkennt man, wie auch<br />
schon vorher zu sehen war, dass das Desorptionsverhalten der 2 – his FNR deutlich schneller<br />
ist und sich eine Stufe ausbildet (kink). Nachdem fast alles Material desorbiert ist, steigt der<br />
Wert nur noch langsam an. Zur mathematischen Beschreibung wird auf eine doppelt<br />
exponentielle Form zurückgegriffen. Ein Grund dafür könnte das Vorliegen zweier<br />
unabhängiger Prozesse an der Oberfläche sein, wie dem Desorbieren des Enzyms und dem<br />
Herauslösen des Metalls von dem tris-NTA Linker. Die genaue Zuordnung dieser Prozesse ist<br />
anahnd dieses Experiments nicht möglich, weshalb auch keine weiteren spekulationen dazu<br />
unternommen werden. Die τ off Werte sind zum einen τ off 1 = 59 s ± 7 s und τ off 2 = 632 s ± 48 s.<br />
Verglichen mit dem τ off des 4-his Enzyms mit 4672 s ±26 s, sieht man eine deutlich höhere<br />
Affinität des 4-his Enzyms. Zur Unterstützung werden zum Schluss noch die K D – Werte der<br />
beiden FNR miteinander verglichen. Im 4 his Fall erhält man einen Wert von 0.35 nM, was<br />
um ein vielfaches niedriger ist als im anderen Fall mit 14.42 nM.<br />
Somit ist auch durch dieses Experiment abgesichert, dass das 4-his Enzym deutlich stärker<br />
an Ni 2+ - modifizierte Oberflächen bindet als das 2-his Enzym.<br />
65