Immobilisierung
resolver
resolver
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
Ergebnisse und Diskussion<br />
DNS – Strangs, was sich in der Absenkung des Signals bemerkbar macht. In der Dissoziationsphase<br />
wird die Lösung vor der Sensoroberfläche gegen Puffer ausgetauscht und die Konzentration<br />
des Analyten auf null gesetzt. Dadurch stellt sich das Gleichgewicht zwischen adsorbierten<br />
und desorbierten Stoffen neu ein und ein Teil (in dem theoretischen Beispiel alles)<br />
des Analyten geht wieder in Lösung. Aus der Form der Kurven lässt sich mit mathematischen<br />
Methoden, analog zu den oben beschriebenen Teilen in der SPR Spektroskopie, die Adsorptions-<br />
und Desorptionskonstante (k on und k off ) bestimmen und aus dieser dann die Dissoziationskonstante<br />
(K D ).<br />
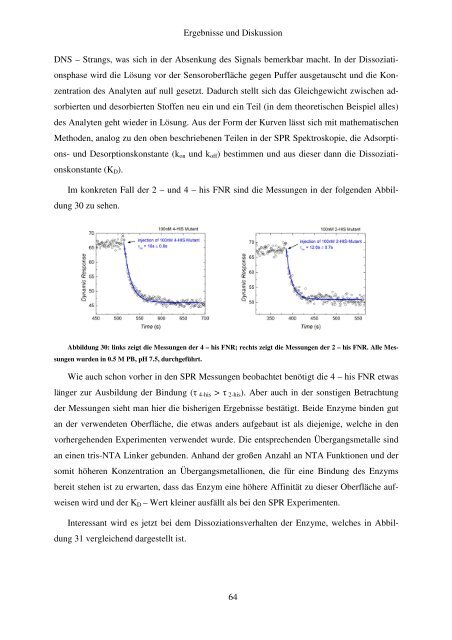
Im konkreten Fall der 2 – und 4 – his FNR sind die Messungen in der folgenden Abbildung<br />
30 zu sehen.<br />
Abbildung 30: links zeigt die Messungen der 4 – his FNR; rechts zeigt die Messungen der 2 – his FNR. Alle Messungen<br />
wurden in 0.5 M PB, pH 7.5, durchgeführt.<br />
Wie auch schon vorher in den SPR Messungen beobachtet benötigt die 4 – his FNR etwas<br />
länger zur Ausbildung der Bindung (τ 4-his > τ 2-his). Aber auch in der sonstigen Betrachtung<br />
der Messungen sieht man hier die bisherigen Ergebnisse bestätigt. Beide Enzyme binden gut<br />
an der verwendeten Oberfläche, die etwas anders aufgebaut ist als diejenige, welche in den<br />
vorhergehenden Experimenten verwendet wurde. Die entsprechenden Übergangsmetalle sind<br />
an einen tris-NTA Linker gebunden. Anhand der großen Anzahl an NTA Funktionen und der<br />
somit höheren Konzentration an Übergangsmetallionen, die für eine Bindung des Enzyms<br />
bereit stehen ist zu erwarten, dass das Enzym eine höhere Affinität zu dieser Oberfläche aufweisen<br />
wird und der K D – Wert kleiner ausfällt als bei den SPR Experimenten.<br />
Interessant wird es jetzt bei dem Dissoziationsverhalten der Enzyme, welches in Abbildung<br />
31 vergleichend dargestellt ist.<br />
64