Skript zur Vorlesung
Skript zur Vorlesung
Skript zur Vorlesung
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
7.3 Chemisches Verhalten von Stickstoff<br />
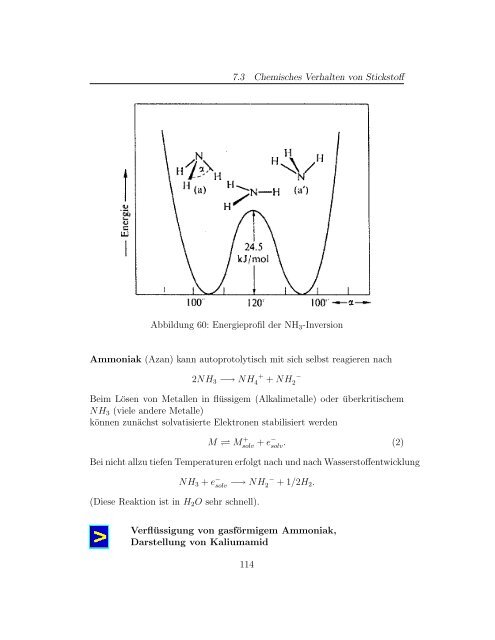
Abbildung 60: Energieprofil der NH3-Inversion<br />
Ammoniak (Azan) kann autoprotolytisch mit sich selbst reagieren nach<br />
2NH3 −→ NH +<br />
4 + NH −<br />
2<br />
Beim Lösen von Metallen in flüssigem (Alkalimetalle) oder überkritischem<br />
NH3 (viele andere Metalle)<br />
können zunächst solvatisierte Elektronen stabilisiert werden<br />
M ⇋ M +<br />
solv + e−<br />
solv . (2)<br />
Bei nicht allzu tiefen Temperaturen erfolgt nach und nach Wasserstoffentwicklung<br />
NH3 + e −<br />
−<br />
solv −→ NH2 + 1/2H2.<br />
(Diese Reaktion ist in H2O sehr schnell).<br />
Verflüssigung von gasförmigem Ammoniak,<br />
Darstellung von Kaliumamid<br />
114