- Seite 1 und 2: Inhaltsverzeichnis Skript zur Vorle
- Seite 3 und 4: INHALTSVERZEICHNIS 6.4.8 Andere Cha
- Seite 5 und 6: Abbildungsverzeichnis ABBILDUNGSVER
- Seite 7 und 8: ABBILDUNGSVERZEICHNIS 74 SO2-Emissi
- Seite 9 und 10: • Literatur - E. Riedel, Anorgani
- Seite 11 und 12: Wichtig ist in diesem Zusammenhang
- Seite 13 und 14: Tabelle 2: Elektronenaffinitäten E
- Seite 15 und 16: Vorzeichengebung nicht einheitlich
- Seite 17 und 18: 2 Hauptgruppenmetalle Bei den Haupt
- Seite 19 und 20: 2.2 Nachweis Tabelle 4: Eigenschaft
- Seite 21 und 22: Diaphragma (ringförmiges Drahtnetz
- Seite 23 und 24: 2.3.2 Sauerstoffverbindungen Abbild
- Seite 25 und 26: 2.3 Chemisches Verhalten Tabelle 5:
- Seite 27 und 28: 2.3 Chemisches Verhalten Abbildung
- Seite 29 und 30: 2.4 Anwendungen Leitfähigkeit. Lö
- Seite 31 und 32: 3 Erdalkalimetalle Die Erdalkalimet
- Seite 33 und 34: 3.1 Nachweis Auch einige Erdalkalim
- Seite 35 und 36: Strontianit SrCO3 Witherit BaCO3 C
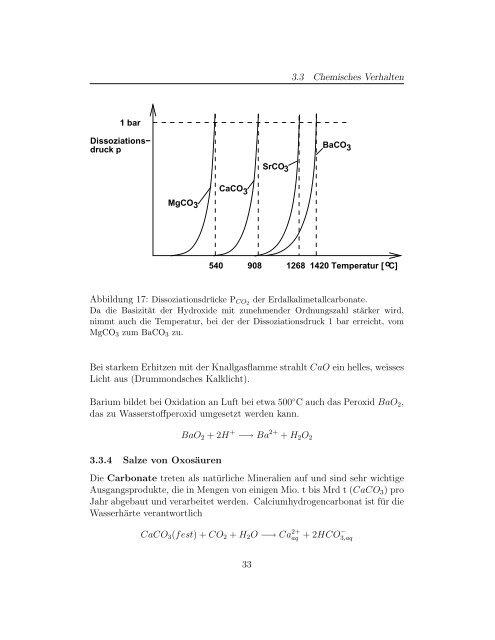
- Seite 37 und 38: 3.3 Chemisches Verhalten Wichtig da
- Seite 39: 3.3 Chemisches Verhalten Im Gegensa
- Seite 43 und 44: 3.3.5 Grignardverbindungen Verbindu
- Seite 45 und 46: 3.4 Anwendungen • Zemente (Ca-Sil
- Seite 47 und 48: Tabelle 6: Gruppeneigenschaften Bor
- Seite 49 und 50: Thalliumverbindungen sind sehr gift
- Seite 51 und 52: 4.2 Vorkommen und Darstellung Tabel
- Seite 53 und 54: 4.2 Vorkommen und Darstellung Galli
- Seite 55 und 56: 4.3 Chemisches Verhalten von Bor Li
- Seite 57 und 58: 4.3 Chemisches Verhalten von Bor Is
- Seite 59 und 60: 4.3.1 Wasserstoffverbindungen 4.3 C
- Seite 61 und 62: 4.3 Chemisches Verhalten von Bor Ab
- Seite 63 und 64: H H N B H B N H N B H H H H N B H B
- Seite 65 und 66: 4.3.4 Halogenide 4.3 Chemisches Ver
- Seite 67 und 68: 4.4 Chemisches Verhalten von Al, Ga
- Seite 69 und 70: AlF 3− 6 4.4 Chemisches Verhalten
- Seite 71 und 72: 4.4.7 Halogenide der einwertigen Me
- Seite 73 und 74: 5 Seltenerdmetalle Elemente der Gru
- Seite 75 und 76: 6 Kohlenstoffgruppe - E14 Die Eleme
- Seite 77 und 78: Fällung und Auflösung von Pb(II)
- Seite 79 und 80: 6.2 Vorkommen und Darstellung Abbil
- Seite 81 und 82: C 6 F 6.3 Chemisches Verhalten von
- Seite 83 und 84: Darstellung von Kaliumgraphit Auch
- Seite 85 und 86: 6.3 Chemisches Verhalten von Kohlen
- Seite 87 und 88: 6.3 Chemisches Verhalten von Kohlen
- Seite 89 und 90: H H H Si H H Si Si H H Si H H Si 6.
- Seite 91 und 92:
6.4 Chemisches Verhalten von Si, Ge
- Seite 93 und 94:
6.4 Chemisches Verhalten von Si, Ge
- Seite 95 und 96:
6.4 Chemisches Verhalten von Si, Ge
- Seite 97 und 98:
6.4 Chemisches Verhalten von Si, Ge
- Seite 99 und 100:
6.4 Chemisches Verhalten von Si, Ge
- Seite 101 und 102:
6.4 Chemisches Verhalten von Si, Ge
- Seite 103 und 104:
6.4 Chemisches Verhalten von Si, Ge
- Seite 105 und 106:
6.4 Chemisches Verhalten von Si, Ge
- Seite 107 und 108:
6.5 Anwendungen Talk: Papierindustr
- Seite 109 und 110:
7.1 Nachweise Tabelle 11: Einige ph
- Seite 111 und 112:
7.2 Vorkommen und Darstellungen Mit
- Seite 113 und 114:
Prot Pviolett 380◦ 200 C, Hg ◦
- Seite 115 und 116:
7.2 Vorkommen und Darstellungen As4
- Seite 117 und 118:
Mineralienbilder: • Auripigment a
- Seite 119 und 120:
Vol % NH3 100 90 80 70 60 50 40 30
- Seite 121 und 122:
7.3 Chemisches Verhalten von Sticks
- Seite 123 und 124:
Die gebildeten Metallkationen köne
- Seite 125 und 126:
explosiv! Durch Zersetzung von HN3
- Seite 127 und 128:
7.3 Chemisches Verhalten von Sticks
- Seite 129 und 130:
7.3 Chemisches Verhalten von Sticks
- Seite 131 und 132:
7.4 Verbindungen von P, As, Sb und
- Seite 133 und 134:
7.4 Verbindungen von P, As, Sb und
- Seite 135 und 136:
7.4 Verbindungen von P, As, Sb und
- Seite 137 und 138:
7.4 Verbindungen von P, As, Sb und
- Seite 139 und 140:
7.4 Verbindungen von P, As, Sb und
- Seite 141 und 142:
den). Stickstoffdünger sind essent
- Seite 143 und 144:
8.1 Nachweise Tabelle 18: Erkennung
- Seite 145 und 146:
8.2 Vorkommen und Darstellungen Tab
- Seite 147 und 148:
155 kJ/mol 92 kJ/mol 8.2 Vorkommen
- Seite 149 und 150:
8.2 Vorkommen und Darstellungen Sch
- Seite 151 und 152:
143 8.2 Vorkommen und Darstellungen
- Seite 153 und 154:
Selenitlösungen gefällt. H2SO3 +
- Seite 155 und 156:
8.3 Verbindungen des Sauerstoffs Ab
- Seite 157 und 158:
8.4 Verbindungen von S, Se, Te und
- Seite 159 und 160:
8.4 Verbindungen von S, Se, Te und
- Seite 161 und 162:
8.4 Verbindungen von S, Se, Te und
- Seite 163 und 164:
Se ❍❍ O ❆❑ O ❆ ❍ ❆✂
- Seite 165 und 166:
(Raumfahrt). 8.6 Anwendungen Schwef
- Seite 167 und 168:
9.2 Vorkommen und Darstellungen Flu
- Seite 169 und 170:
Oxidation von Halogeniden mit Halog
- Seite 171 und 172:
9.3 Verbindungen unlöslichem CaF2
- Seite 173 und 174:
9.3 Verbindungen ClO2 ist sehr expl
- Seite 175 und 176:
⊕ �� ❅ Cl �� �� ❅
- Seite 177 und 178:
9.4 Anwendungen schwächer sauer si
- Seite 179 und 180:
• Kohlevergasung unter Bildung vo
- Seite 181 und 182:
11.1 Vorkommen und Darstellungen 11
- Seite 183 und 184:
11.3 Anwendungen damit verbundenen
- Seite 185 und 186:
Cyanidlaugerei, 98 Destillation fra
- Seite 187 und 188:
Quarzdruse, 72 Quarzgläser, 98 Rak