Skript zur Vorlesung
Skript zur Vorlesung
Skript zur Vorlesung
Erfolgreiche ePaper selbst erstellen
Machen Sie aus Ihren PDF Publikationen ein blätterbares Flipbook mit unserer einzigartigen Google optimierten e-Paper Software.
6.4 Chemisches Verhalten von Si, Ge, Sn und Pb<br />
Name altern. Name Anion verkn. Verbindung<br />
Ecken<br />
Inselsilicate Nesosilicate [SiO4] 0 Zirkon / ZrSiO4<br />
Gruppensilicate Sorosilicate [Si2O7] 6− 1 Barysilit / P b3[Si2O7]<br />
Ringsilicate Cyclosilicate [Si3O9] 6− 2 Benitoit / BaT i[Si3O9]<br />
[Si6O18] 12− Beryll / Be3Al2[Si6O18]<br />
Kettensilicate Inosilicate [Si2O6] 4− 2, 3 Pyroxene<br />
(Spodumen / LiAl[Si2O6])<br />
[Si4O11] 6− Amphibole<br />
(Tremolid / Ca2Mg5[Si4O11])<br />
Schichtsilicate Phyllosilicate [Si4O10] 4− 3 Talk, Glimmer<br />
Gerüstsilicate Tektosilicate [Si4O10] 4− 4 Feldspate<br />
(Albit / Na[AlSi3O8]),<br />
Clathrasile<br />
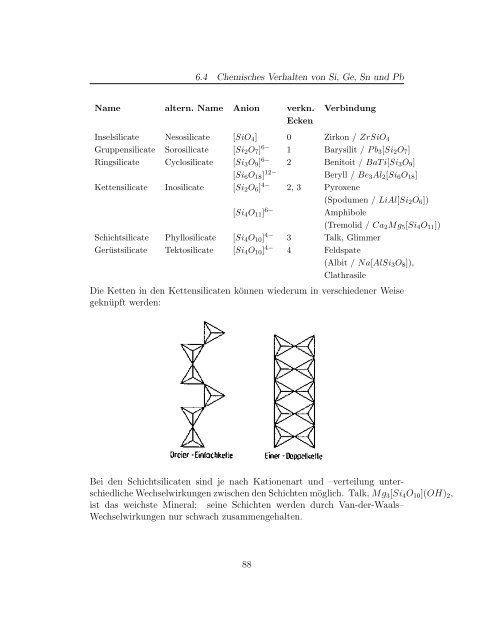
Die Ketten in den Kettensilicaten können wiederum in verschiedener Weise<br />
geknüpft werden:<br />
Bei den Schichtsilicaten sind je nach Kationenart und –verteilung unterschiedliche<br />
Wechselwirkungen zwischen den Schichten möglich. Talk, Mg3[Si4O10](OH)2,<br />
ist das weichste Mineral; seine Schichten werden durch Van-der-Waals–<br />
Wechselwirkungen nur schwach zusammengehalten.<br />
88