Methoden zur Evaluation von Zytotoxizit¨at und Struktur ... - OPUS
Methoden zur Evaluation von Zytotoxizit¨at und Struktur ... - OPUS
Methoden zur Evaluation von Zytotoxizit¨at und Struktur ... - OPUS
Sie wollen auch ein ePaper? Erhöhen Sie die Reichweite Ihrer Titel.
YUMPU macht aus Druck-PDFs automatisch weboptimierte ePaper, die Google liebt.
1.1 ”Orphan Drugs and Neglected Diseases” 13<br />
dung [167,181,233]. Diese schnelle Resistenzentwicklung ist vor allem auf den Einsatz<br />
als Breitbandantibiotika <strong>zur</strong>ückzuführen.<br />
1.1.1.2 Antibiotika die “Orphan Drugs” der Zukunft?<br />
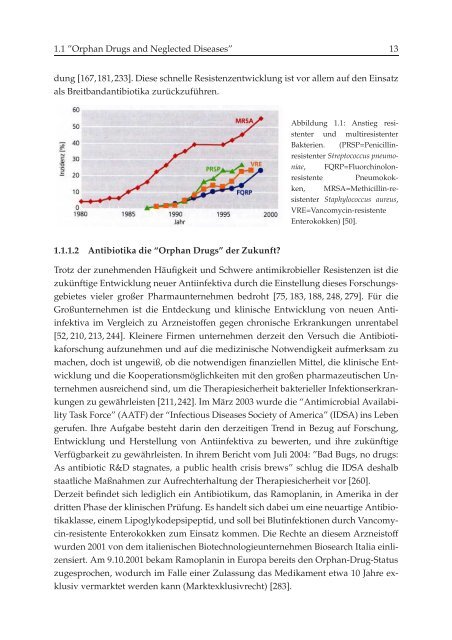
Abbildung 1.1: Anstieg resistenter<br />
<strong>und</strong> multiresistenter<br />
Bakterien. (PRSP=Penicillinresistenter<br />
Streptococcus pneumoniae,FQRP=FluorchinolonresistentePneumokokken,MRSA=Methicillin-resistenter<br />
Staphylococcus aureus,<br />
VRE=Vancomycin-resistente<br />
Enterokokken) [50].<br />
Trotz der zunehmenden Häufigkeit <strong>und</strong> Schwere antimikrobieller Resistenzen ist die<br />
zukünftige Entwicklung neuer Antiinfektiva durch die Einstellung dieses Forschungs-<br />
gebietes vieler großer Pharmaunternehmen bedroht [75, 183, 188, 248, 279]. Für die<br />
Großunternehmen ist die Entdeckung <strong>und</strong> klinische Entwicklung <strong>von</strong> neuen Anti-<br />
infektiva im Vergleich zu Arzneistoffen gegen chronische Erkrankungen unrentabel<br />
[52, 210, 213, 244]. Kleinere Firmen unternehmen derzeit den Versuch die Antibioti-<br />
kaforschung aufzunehmen <strong>und</strong> auf die medizinische Notwendigkeit aufmerksam zu<br />
machen, doch ist ungewiß, ob die notwendigen finanziellen Mittel, die klinische Ent-<br />
wicklung <strong>und</strong> die Kooperationsmöglichkeiten mit den großen pharmazeutischen Un-<br />
ternehmen ausreichend sind, um die Therapiesicherheit bakterieller Infektionserkran-<br />
kungen zu gewährleisten [211,242]. Im März 2003 wurde die “Antimicrobial Availabi-<br />
lity Task Force” (AATF) der “Infectious Diseases Society of America” (IDSA) ins Leben<br />
gerufen. Ihre Aufgabe besteht darin den derzeitigen Trend in Bezug auf Forschung,<br />
Entwicklung <strong>und</strong> Herstellung <strong>von</strong> Antiinfektiva zu bewerten, <strong>und</strong> ihre zukünftige<br />
Verfügbarkeit zu gewährleisten. In ihrem Bericht vom Juli 2004: ”Bad Bugs, no drugs:<br />
As antibiotic R&D stagnates, a public health crisis brews” schlug die IDSA deshalb<br />
staatliche Maßnahmen <strong>zur</strong> Aufrechterhaltung der Therapiesicherheit vor [260].<br />
Derzeit befindet sich lediglich ein Antibiotikum, das Ramoplanin, in Amerika in der<br />
dritten Phase der klinischen Prüfung. Es handelt sich dabei um eine neuartige Antibio-<br />
tikaklasse, einem Lipoglykodepsipeptid, <strong>und</strong> soll bei Blutinfektionen durch Vancomy-<br />
cin-resistente Enterokokken zum Einsatz kommen. Die Rechte an diesem Arzneistoff<br />
wurden 2001 <strong>von</strong> dem italienischen Biotechnologieunternehmen Biosearch Italia einli-<br />
zensiert. Am 9.10.2001 bekam Ramoplanin in Europa bereits den Orphan-Drug-Status<br />
zugesprochen, wodurch im Falle einer Zulassung das Medikament etwa 10 Jahre ex-<br />
klusiv vermarktet werden kann (Marktexklusivrecht) [283].