Хемија, уџбеник за први разред гимназије, Нови Логос
- No tags were found...
Create successful ePaper yourself
Turn your PDF publications into a flip-book with our unique Google optimized e-Paper software.
7. ХЕМИЈСКЕ РЕАКЦИЈЕ<br />
а)<br />
б)<br />
Слика 7.17. Реакција<br />
воденог раствора<br />
хлороводоничне<br />
киселине (1 mol/dm 3 ) с<br />
а) комадићем калцијум-<br />
-карбоната, б) прахом<br />
калцијум-карбоната<br />
jеднаких маса<br />
Утицај слободне површине<br />
Да би супстанце реаговале, морају бити у додиру. то је већа<br />
површина којом се супстанце додирују, то је и могућност<br />
реаговања већа, а тиме и брзина хемијске реакције. На<br />
пример, калцијум-карбонат у облику праха реагује брже с<br />
хлороводоничном киселином него једнака маса те супстанце у<br />
облику комадића слика 7.17.<br />
Највећи могући степен уситњености чврсте супстанце имају када се<br />
растворе. Због тога су реакције у растворима брже од хетерогених<br />
реакција у којима учествују супстанце различитих агрегатних<br />
стања. На пример, реакције између јона насталих растварањем<br />
чврстих супстанци у води скоро су тренутне. Разлог је максимална<br />
уситњеност супстанци на јоне, али често и привлачне силе између<br />
супротно наелектрисаних јона. За те реакције важи да је њихова<br />
енергија активације приближно једнака нули.<br />
Утицај температуре<br />
Уколико се температура реакционог суда повиси, долази до<br />
повећања брзине реакције. При повишеној температури повећава<br />
се кинетичка енергија честица, а тиме и број судара. то већи број<br />
молекула реактаната има довољну количину енергије једнаку или<br />
већу од енергије активације, то је већи и број успешних судара у<br />
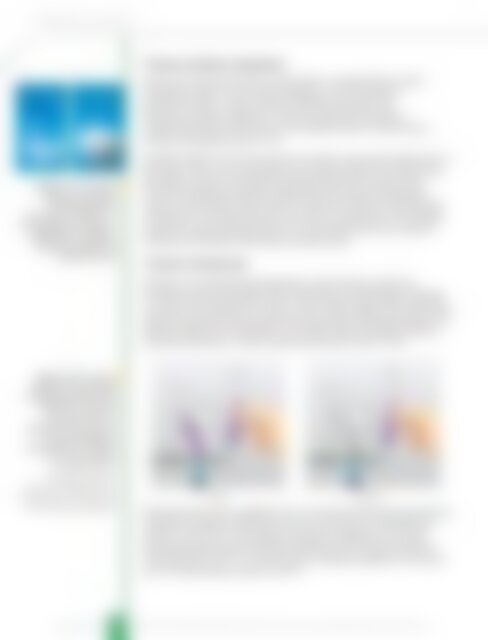
јединици времена, а тиме и брзина реакције слика 7.18.<br />
Слика 7.18. Реакција<br />
љубичастог раствора<br />
калијум-перманганата<br />
(КМnO 4 ) и оксалне<br />
киселине (Н 2 С 2 О 4 )<br />
једнаких количинских<br />
концентрација на<br />
повишеној (1) и собној<br />
(2) температури.<br />
У епрувети која се<br />
<strong>за</strong>грева долази до<br />
приметне реакције јер с<br />
повишењем температуре<br />
расте брзина реакције.<br />
1<br />
Пре<br />
2 2<br />
кспериментално је одређено да се <strong>за</strong> велики број реакција брзина<br />
хемијске реакције повећа два-три пута уколико се температура<br />
повиси <strong>за</strong> око 10 С. На пример, уколико је одређено да се при<br />
једној реакцији брзина реакције повећа два пута при повишењу<br />
температуре <strong>за</strong> 10 С, то значи да ће се брзина повећати осам пута<br />
ако се температура повиси <strong>за</strong> 30 С .<br />
1<br />
После<br />
Забрањено је репродуковање, умножавање, дистрибуција, обј<br />
ављивање, прерада и друга употреба овог ауторског дела или његових делова у било ком обиму и поступку, укључујуј<br />
ући<br />
фотокопирање, штампање, чув а208 ње<br />
у електронском облику, односно чињење дела доступним јавности жичним или бежичним путем на начин кој<br />
и омогућујуј<br />
е пој<br />
единцу индивидуални приступ делу<br />
са места и у време кој<br />
е он одабере, без писмене сагласности издавача. Свако неовлашћено коришћење овог ауторског дела представља кршење Закона о ауторском и сродним правима.